Fosforna kiselina i fosfati
Fosforne kiseline i fosfati se javljaju u raznim oblicima. Od mnogih fosfornih oksokiselina, fosforske kiseline predstavljaju najveću i najraznovrsniju grupu. Najjednostavnija u toj seriji kiselina je monofosorna (ortofosforna) kiselina, a slijede mnoge oligofosforne kiseline, kao što je difosforna (pirofosforna) kiselina i zaključuju polifosforne kiseline. Ali, jedinice fosforne kiseline se mogu vezati zajedno u prstenove ili ciklične strukture, lance ili razgranate strukture, s raznim mogućim kombinacijama. Svaki od ovih mogu formirati fosfatne soli ili estre fosforne kiseline.[1][2][3][4]
Ortofosforna kiselina[uredi | uredi izvor]
Najjednostavniji hemijski spoj u nizu 'fosfornih kiselina' se ponekad naziva zajedničkim imenom, ortofosforna kiselina, ali češće nadimcima svojih IUPAC oznaka, jednostavno fosforna kiselina, u komunikaciji neupućenih osob, pa čak i mnogiH hemičarA. Također se nazivaju i monofosforna kiselina.[5] Hemijska formula ortofosforne kiseline je H3PO4 a njena hemijska struktura je prikazana ispod. Dvije ili više molekula ortofosforne kiseline se mogu pridružiti i kondenzirati u veće molekule, eliminacijom vode. Na ovaj način, može se dobiti serija polifosfornih kiselina.
-
Porofosforna kiselina
H4P2O7 -
Tripolifosforna kiselina
H5P3O10 -
Tetrapolifosforna kiselina
H6P4O13 -
Trimetafosforna kiselina
H3P3O9 -
Fosforni anhidrid
P4O10
Ortofosfati[uredi | uredi izvor]
U svojoj strukturi, ortofosforna kiselina ima tri vodikova atoma vezana za kisik. Sva tri vodika su, u različitoj mjeri, kisela i mogu se izgubiti iz molekule kao ioni H+ (alternativno kao protoni). Kada ortofosforna kiselina izgubi sva tri H+, formira ion ortofosfata (PO43−). Ortofosfati su najjednostavniji u seriji fosfata, a obično se nazivaju samo kao fosfat, čak i u krugovima hemičara.
Zato što ortofosforna kiselina može proći čak tri disocijacije ili ionizacije (gubici H+ ions), ima tri disocijacijske konstente zvane Ka1, Ka2 i Ka3. Drugi način prikazivanja podataka o disocijacijskoj konstanti je pKa1, pKa2 i pKa3. Ortofosfat je u smislu trostruke konjugirane baze fosforne kiseline i ima tri povezane bazne konstante, Kb1, Kb2 i Kb3, koje liče na odgovarajuće vrijednosti pKb1, pKb2 i pKb3.
Polifosforne kiseline[uredi | uredi izvor]

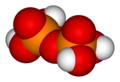
Kada se dvije ortofosforne kiseline kondenziraju u jednu molekulu, dobije se pirofosforna kiselina (H4P2O7), kako slijedi:
- 2 H3PO4 → H4P2O7 + H2O
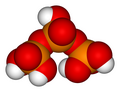
U ilustraciji je također prikazana i hemijska struktura pirofosforne kiseline. Kada se međusobno povežu tri ortofosforne kiseline, nastaje tripolifosforna kiselina (H5P3O10), koja je također prikazana. Proces kondenzacije jedinica ortofosforne kiseline se može nastaviti, kada se dobioja tetrapolifosforna kiselina (H6P4O13 itd. Svaka dodatna fosforna jedinica dodaje po jedan dodatni H (vodikoc) atoma, jedfan dodatni atom P (fosfora), i tri dodatna O (kisikova) atoma. „Okosnički lanac“ ove vrste molekula se sastoji od naizmjeničnih P i O kovalentno vezanih atoma zajedno. Molekule polifosfornih kiselina mogu imati desetine takvih fosfornih, serijski vezanih, jedinica. Opća formula za takve spojeve poli-kiselinskih spojeva je HO(PO2OH)xH, gdje je x = broj fosfornih jedinica u molekuli. Četiri atoma kisika se vežu za svaki atom fosfora, u tetrahedrnoj konfiguraciji, sa fosforom u centru tetraedra i kisikom u svakom od četiri ugla.
Polifosforne kiseline se upotrebljavaju u organskoj sintezi ciklizacije i acilacije.
Polifosfati[uredi | uredi izvor]
Linearni polifosfati[uredi | uredi izvor]
U molekuli pirofosforne kiseline, postoje četiri vodika vezana za kisik, a jedan, dva, tri ili sva četiri mogu biti izgubljeni kao ioni H+. Kada su sva četiri izgubljena, formira se ion pirofosfata. Pošto polifosforna kiselina može proći četiri disocijacije, za nju postoje četiri vrijednosti Ka, kao i četiri odgovarajuće vrijednosti pKa. Slično tome, pirofosfat je baza sa četiri Kb i, prema tome, četiri vrijednosti pKb za vraćanje H+ iona u obrnutom redoslijedu.
Situacija sa polifosfornim kiselinama i polifosfatima višeg reda se odvija na sličan način. Tripolifosforna kiselina može izgubiti i do pet iona H+ da se formira ion tripolifosfata, tetrapolifosforna kiselinom može izgubiti i do šest iona H+ da se formira tetrapolifoffat, itd. Što je više mogućih disocijacija po molekuli, intervali između pojedinih pKa i pKb vrijednosti tada počinju, u pH razmjerima, bivati manje. Kakoo molekula polifosforne kiseline postaje sve veća i kompleksnija, praktično bilo koji broj kiselih -OH grupe u njima može disocirati i postati negativno napunjeni kisik, formirajući brojne kombinacije višestruko nabijenih polifosfornih / polifosfatnih aniona. Općenito, u vodenim rastvorima, stepen ili postotak disocijacije ovisi o pH vrijednosti.
Orto–, piro– i tripolifosfatni spojevi se općenito upotrebljavaju u deterdžentima (i drugim sredstvima za čišćenje). Naprimjer, vidi Natrij-tripolifosfat. Ponekad se pirofosfat, tripolifosfat, tetrapolifosfat, itd nazivaju difosfat, trifosfat, tetrafosfat, itd, posebno kada su, u biohemiji, dio fosfata-estera Oni se koriste i za kontrolu korozije mreže za distribuciju pitke vode.[6] Kao inhibitori korozije, polifosfati stvaraju zaštitni film na unutrašnjim površinama slavina.[7]
Metafosforne kiseline i metafosfati[uredi | uredi izvor]
Jedinice polifosforne kiseline mogu se međusobno vezati u prstenove (ciklične strukture), formirajući molekule metafosforne kiseline. Najjednostavniji takav spoj je trimetafosforna kiselina ili ciklo-trifosforna kiselina, čija je formula H3P3O9. Njena struktura je prikazana na priloženoj ilustraciji. Budući da su joj krajevi kondenziran, u svojoj formuli ima manje jednu molekulu H2O (voda) nego tripolifosforna kiselina. Ono što se obično naziva trimetafosfati zapravo imaju mješavinu veličine prstena. Opća formula za takve ciklične spojeve jen(HPO3)x, gdje je x = broj fosfornih jedinica u molekuli . Nije poznato da li postoji hipotetski monomer monometafosforna kiselina (HPO3), koja bi mogla biti izovalentna sa dušičnom kiselinom. Kada ove metafosforne kiseline izgube vodik H+, formiraju se ciklični anioni pod nazivom metafosfati. Primjer spoja sa takvimm anionom je natrij-heksametafosfat (Na6P6O18), koji se upotrebljava kao sekvestrant i a prehrambeni aditiv.
Granati polifosfosfati[uredi | uredi izvor]
Treća -OH grupa na jedinici ortofosforne kiseline može se također upotrebiti za kondenzaciju sa ostalim fosfornim grupama za grananje lanaca polifosfornih/polifosfatnih lanaca. Krajnji primjer ciklične i razgranate kondenzacije će biti ciklični četverofosfat na jedinica za dvostruke grane koje čine fosforni anhidrid P4O10; vidi sliku.
Hidroliza polifosfornih kiselina/polifosfata[uredi | uredi izvor]
Ovaj niz fosfornih kiselina su tvari koje su uglavnom topive u vodi, s obzirom na polarnost molekula. Fosfati amonijaka i alkala također su dobro topivi u vodi. U Soli zemnih alkala startno postaju manje topivi, a fosfatne soli raznih drugih metala su čak i manje topive. U vodenim otopinama, voda se postupno (u toku sata) hidrolizira polifosfate u manje fosfate i konačno u orto-fosfate, uz dodatak dovoljno vode. Viša temperatura ili kiseli uvjeti mogu znatno ubrzati hidrolizu reaakcija.[8] S druge strane, polifosforne kiseline ili polifosfati često nastaju dehidracijom s otopinom fosforne kiseline; drugim riječima, često uz uklanjanje vode iz njega, zagrijavanjem i isparavanjem.
Fosfat i i fosfatni estri[uredi | uredi izvor]
Grupe -OH u fosfornim kiselinama mogu se također kondenzirati sa hidroksilnim grupama alkohola i formirati pfosfat-estere. Pošto ortofosforna kiselina ima tri -OH grupe, može esterificirati s jednom, dvije ili tri molekule alkohola da se formira mono-, di- ili triester. Vidjeti strukturu slike: generalni orto- (ili mono) fosfat ester je ispod na lijevoj strani, gdje bilo koja od R grupa može biti vodik ili organski radikal. Mogući su također i piro- (ili di-) fosfatni estri i tripolu- (ili tri-fosfatni esteri). Bilo koja-OH grupa fosfata u tim molekulama estera može izgubiti ion H+ u obliku aniona, opet ovisno o pH vrijednosti otopine. U biohemiji živih organizama, postoje mnoge vrste (mono)fosfatnih, difosfatnih i trifosfatnih spojeva (u biti estera), od kojih mnogi imaju značajnu ulogu u metabolizmu, kao što su adenozin difosfat (ADP) i trifosfat (ATP).
Ovdje bilo koji R može biti H
ili drugi organski radikal
Slično tome, fosforna kiselina se može povezati s molekulama alkohola da nastane fosfit-ester. Vidi sliku opće strukture ispod, na desnoj strani. Dvije tačkice na P predstavljaju usamljeni elektronski par u atomu fosfora.
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Atkins P., de Paula J. (2006). Physical chemistry, 8th Ed. San Francisco: W. H. Freeman. ISBN 0-7167-8759-8.
- ^ Whitten K.W., Gailey K. D. and Davis R. E. (1992). General chemistry, 4th Ed. Philadelphia: Saunders College Publishing. ISBN 0-03-072373-6.
- ^ Petrucci R. H., Harwood W. S., Herring F. G. (2002). General Chemistry, 8th Ed. New York: Prentice-Hall. ISBN 0-13-014329-4.CS1 održavanje: više imena: authors list (link)
- ^ Laidler K. J. (1978). Physical chemistry with biological applications. Benjamin/Cummings. Menlo Park. ISBN 0-8053-5680-0.
- ^ Robertson DS (2004). "A possible natural antibacterial compound in the human metabolism". Med Hypotheses. 63 (3): 554–5. doi:10.1016/j.mehy.2004.04.007. PMID 15288387. Referenca sadrži prazan nepoznati parametar:
|month=(pomoć) - ^ "Polyphosphates for scale and corrosion control". Tramfloc, INC. januar 2009. Pristupljeno 23. 12. 2010.
- ^ "Ortho-Polyphosphate Corrosion Inhibitors" (PDF). Government Engineering:The Journal for Public Infrastructure (September–October, 2006): 48–49. Arhivirano s originala (PDF), 11. 7. 2011. Pristupljeno 23. 12. 2010.
- ^ "Phosphoric acid and phosphates". Encyclopedia of Chemical Technology. New York: The Interscience Encyclopedia, Inc. 1953. str. 421.
Dopunska literatra[uredi | uredi izvor]
- Schröder HC, Kurz L, Muller WE, Lorenz B (2000). "Polyphosphate in bone" (PDF). Biochemistry (Moscow). 65 (3): 296–303. Arhivirano s originala (PDF), 25. 8. 2011. Pristupljeno 13. 7. 2016.CS1 održavanje: upotreba parametra authors (link)