Mangan peroksidaza
U enzimologiji, mangan peroksidaza (EC broj 1.11.1.13) jeste enzim koji katalizira hemijsku reakciju:
- 2 Mn(II) + 2 H+ + H2O2 2 Mn(III) + 2 H2O
Tri supstrata ovog enzima su Mn(II), H+ i H2O2, dok su njegova dva proizvoda Mn(III) i H2O.
Ovaj enzim pripada porodici oksidoreduktaza, tačnije onima koje djeluju na peroksid kao primalac (peroksidazama). Sistematsko ime ove klase enzima je Mn(II):vodik-peroksid oksidoreduktaza. Druga uobičajena imena, između ostalih, su peroksidaza-M2 i "peroksidaza zavisna od Mn" (koja oksidira NADH). Ona uključuje jedan kofaktor, hem. Za aktivnost ovog enzima neophodan je ion kalcija, Ca2+.
Neke vrste gljiva poput Cyathus stercoreus luče ovaj enzim koji im pomaže u degradaciji lignina.
Otkriće i opis[uredi | uredi izvor]
Mangan peroksidaza (često se označava skraćenicom MnP) otkrivena je 1985. godine. Otkrili su je dvije grupe naučnika okupljenih oko Michaela H. Golda[1] i Ronalda Crawforda,[2] u gljivi Phanerochaete chrysosporium. Njen protein je genetski sekvenciran 1989. u P. chrysoporium.[3] Za enzim se smatralo da je jedinstven unutar Basidiomycota, jer do tada nije otkriveno da ga prirodno ne proizvodi niti jedna vrsta bakterija, plijesni ili kvasaca.
Mehanizam reakcije[uredi | uredi izvor]
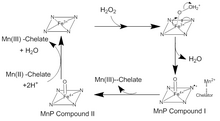
MnP kataliza se dešava u seriji nepovratnih oksidacijsko-redukcijskih reakcija (redoks reakcija) koja slijedi takozvani ping-pong mehanizam sa kinetikom drugog reda.[4] U prvom koraku katalitičkog ciklusa, vodik-peroksid H2O2 ili neki organski peroksid spaja se na aktivno mjesto na MnP. Tako se kisik iz H2O2 veže na ion željeza Fe(III) u kofaktoru hema dajuću kompleks željezo-peroksida. Dva elektrona prelaze sa iona Fe3+ na peroksid, razbijajući vezu kisik-peroksid te gradeći vodu i kompleks radikala Fe(IV) okso-porfirin. Ovaj oksidirani međuspoj poznat je kao MnP spoj I. Zatim se MnP spoj I veže s monoheliranim ionom Mn(II), koji donira elektron da bi ugasio radikal i oformio Mn(III) MnP spoj II, odnosno kompleks Fe(IV) okso-porfirina. Zatim MnP spoj II oksidira sljedeći ion Mn(II) do Mn(III) a reducira se reakcijom dva iona H+ a željezo se veže kisikom. Ovo reformira Fe(III) ion u hemu i otpušta drugu molekulu vode.[5] Postoji mnogo devijacija od ovog tradicionalnog katalitičkog ciklusa. MnP spoj I se može koristiti za oksidaciju slobodnog Mn(II), ferocijanida, kao i fenola i drugih aromatskih spojeva.[6]
Reference[uredi | uredi izvor]
- ^ Glenn JK, Gold MH (1. 11. 1985). "Purification and characterization of an extracellular Mn(II)-dependent peroxidase from the lignin-degrading basidiomycete, Phanerochaete chrysosporium". Arch. Biochem. Biophys. 242 (2): 329–41. doi:10.1016/0003-9861(85)90217-6. PMID 4062285.
- ^ Paszcynski A, Huynh V-B, Crawford R, (1. 8. 1985). "Enzymatic activities of an extracellular, manganese- dependent peroxidase from Phanerochaete chrysosporium". FEMS Microbiol. Lett. 29 (1–2): 37–41. doi:10.1111/j.1574-6968.1985.tb00831.x.CS1 održavanje: dodatna interpunkcija (link) CS1 održavanje: više imena: authors list (link)
- ^ Pribnow D, Mayfield MB, Nipper VJ, Brown JA, Gold MH (1. 3. 1989). "Characterization of a cDNA encoding a manganese peroxidase, from the lignin-degrading basidiomycete Phanerochaete chrysosporium". J. Biol. Chem. 264 (9): 5036–40. PMID 2925681.CS1 održavanje: više imena: authors list (link)[mrtav link]
- ^ Wariishi H, Valli K, Gold MH (1. 11. 1992). "Manganese(II) oxidation by manganese peroxidase from the basidiomycete Phanerochaete chrysosporium. Kinetic mechanism and role of chelators". J. Biol. Chem. 267 (33): 23688–95. PMID 1429709.CS1 održavanje: više imena: authors list (link)[mrtav link]
- ^ Hofrichter M (1. 4. 2002). "Review: lignin conversion by manganese peroxidase (MnP).". Enzyme and Microbial Technology. 30 (4): 454–66. doi:10.1016/S0141-0229(01)00528-2.
- ^ Heinfling A, Ruiz-Dueñas FJ, Martínez MJ, Bergbauer M, Szewzyk U, Martínez AT (1. 5. 1998). "A study on reducing substrates of manganese-oxidizing peroxidases from Pleurotus eryngii and Bjerkandera adusta". FEBS Lett. 428 (3): 141–6. doi:10.1016/s0014-5793(98)00512-2. PMID 9654123.CS1 održavanje: više imena: authors list (link)

