Metahromatska leukodistrofija
| Metahromatska leukodistrofija (MLD) (Nedostatak arilsulfataze A) (Nedostatak ARSA)  | |
|---|---|
| Klasifikacija i vanjski resursi | |
| ICD-10 | E75.25 |
| ICD-9 | 330.0 |
| OMIM | 250100 |
| DiseasesDB | 8080 |
| MedlinePlus | 001205 |
| eMedicine | ped/2893 |
| MeSH | D007966 |
Metakromatska leukodistrofija (MLD) je bolest lizosomskog skladištenja, koja je uobičajeno navedena u porodici leukodistrofija, kao i među sfingolipidozama, jer utiče na metabolizam sfingolipida. Leukodistrofije utiču na rast i/ ili razvoj mijelina, masnog pokrivača koji djeluje kao izolator oko nervnih vlakana kroz centralni i periferni nervni sistem. MLD uključuje akumulaciju cerebrozid-sulfata.[1] Metakromatska leukodistrofija, kao i većina enzimskih nedostataka, ima autosomno recesivni obrazac nasljeđivanja.[1]
Znaci i simptomi[uredi | uredi izvor]
Kao i mnogi drugi genetički poremećaji koji utiču na metabolizam lipida, postoji nekoliko oblika MLD-a, koji su kasni infantilni, maloljetnički i odraslih osoba.
- U „kasnom infantilnom obliku“, koji je najčešći oblik MLD (50–60%), pogođena djeca počinju imati poteškoće u hodanju nakon prve godine života, obično u dobi od 15 do 24 mjeseca. Simptomi uključuju gubitak i slabost mišića, rigidnost mišića, zastoje u razvoju, progresivni gubitak vida koji dovodi do sljepoće, konvulzije, otežano gutanje, paralizu i demenciju. Djeca mogu postati komatozna. Neliječena, većina djece s ovim oblikom MLD-a umire do 5. godine, često mnogo prije.
- Djeca s maloljetničkim oblikom MLD-a (početak između 3 i 10 godine starosti) obično počinju s smanjenim školskim uspjehom, mentalnim pogoršanjem i demencijom, zatim razvijaju simptome slične kasnom infantilnom obliku, ali sa sporijim napredovanjem. Dob pri smrti je različita, ali obično u roku od 10 do 15 godina od pojave simptoma. Neki pacijenti mogu živjeti i nekoliko decenija nakon početka. Nedavni trend je pokušaj razlikovanja rano-maloljetničkih (3–7 godina) i kasno-maloljetničkih oblika bolesti. Općenito, kod ranih maloljetnika prvi simptomi smanjuju se u motornim sposobnostima, dok kod kasnijih maloljetnika prvo opažaju kognitivni pad.
- Oblik kod odraslih obično započinje nakon 16. godine, često s početkom u 4. ili 5. deceniji života i predstavlja se kao psihijatrijski poremećaj ili progresivna demencija. MLD kod odraslih obično napreduje sporije od kasnih infantilnih i maloljetničkih oblika, s produženim tokom od jedne decenije ili više.
Palijativna njega može pomoći kod mnogih simptoma i obično poboljšava kvalitet života i dugovječnost.
Nositelji gena imaju nizak nivo enzima u poređenju sa njihovom članovima porodice ("normalni" nivoi variraju od porodice do porodice), ali čak i niski nivoi enzima su dovoljni za obradu sulfatida u tijelu.
Uzroci[uredi | uredi izvor]
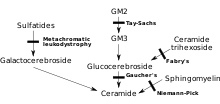
MLD je direktno uzrokovan nedostatkom enzima arilsulfataza A[2] (ARSA), a karakterizira ga enzimska aktivnost u leukocitima koja je manja od 10% normalne kontrole.[3] Međutim, samo ispitivanje aktivnosti enzima ARSA nije dovoljno za dijagnozu. Pseudodeficijencija ARSA, koju karakterizira aktivnost enzima koja iznosi 5 ~ 20% normalne kontrole, ne uzrokuje MLD.[3] Bez ovog enzima, sulfatid se nakuplja u mnogim tkivima tijela , na kraju uništavajući mijelinsku ovojnicu živčanog sistema. Mijelinska ovojnica je masni pokrov koji štiti živčana vlakna. Bez toga, živci u mozgu (centralni nervni sistem – CNS) i periferni živci (periferni nervni sistem – PNS) koji kontroliraju, između ostalog i mišiće povezane s pokretljivošću, prestaju pravilno funkcionirati.
Arilsulfatazu A aktivira saposin B (Sap B), neenzimski proteinski kofaktor.[4] Kada je nivo enzima arilsulfataze A normalan, ali sulfatidi su i dalje visoki – što znači da se ne razgrađuju jer enzim nije aktiviran – rezultirajuća bolest je nedostatak saposina B, koji je sličan MLD-u.[3] Nedostatak saposina B je vrlo rijedak, mnogo rjeđi od tradicijskog MLD-a.[3] Enzim koji je prisutan nije"osposobljen" za normalan nivo efikasnosti i ne može razgraditi sulfatide, što rezultira istim simptomima i napredovanjem MLD-a.[5]
Studija iz 2011. godine tvrdila je da sulfatid nije u potpunosti odgovoran za MLD, jer je netoksičan. Predloženo je da lizosulfatid, sulfatid kojem je uklonjena acilna grupa, ima ulogu zbog svojih citotoksičnih svojstava in vitro.[6]
Genetika[uredi | uredi izvor]

MLD ima autosomno recesivni obrazac nasleđivanja. Vjerovatnoće nasljeđivanja po rođenju su kako slijedi:
- Ako su oba roditelja nositelji:
- 25% (1 od 4) djece će imati bolest
- 50% (2 od 4) djece bit će nositelji, ali to neće ispoljavati
- 25% (1 od 4) djece neće imati MLD – dijete koje nije pogođeno i nije nositelj
- Ako je pogođen jedan roditelj, a jedan je bez MLD-a:
- 0% (0) djece će imati poremećaj - pogođen je samo jedan roditelj, drugi roditelj uvijek daje normalan gen
- 100% (4 od 4) djece bit će nositelji (ali to neće ispoljavati)
- Ako je jedan roditelj nosilac, a drugi je bez MLD-a:
- 50% (2 od 4) djece bit će nositelji (ali to neće uticati)
- 50% (2 od 4) djece neće imati MLD – dijete koje nije pogođeno i nije nositelj. Pored ovih frekvencija, postoji i 'pseudo' nedostatak koji pogađa 7-15% populacije.[7][8] Osobe sa pseudo nedostatkom nemaju problema sa MLD-om, osim ako nemaju uticaj na status. Sa sadašnjim dijagnostičkim testovima, pseudo-nedostatak izvještava o niskim nivoima enzima, ali sulfatid se normalno obrađuje, tako da nema simptoma MLD. Ova pojava obara tradicijske pristupe skrininga novorođenčadi, pa se razvijaju nove metode sselekcije . Za dalje informacije, pogledajte recesivni gen i odnos dominacije. Također, može se potražiti stranica MLD genetike na MLD Foundation.
Dijagnoza[uredi | uredi izvor]
Klinički pregled i MRI često su prvi koraci u dijagnozi MLD. MRI može biti indikativni za MLD, ali nije adekvatan kao potvrdni test. Test krvi na nivou enzima ARSA-A sa potvrdnim testom urinarnog sulfatida najbolji je biohemijski test za MLD. Potvrđivanje urinarnog sulfatida važno je za razlikovanje rezultata MLD i pseudo-MLD u krvi. Genomsko sekvenciranje takođe može potvrditi MLD, međutim, vjerovatno je više mutacija od preko 200 već poznatih da uzrokuju MLD koji još nisu pripisani MLD-, a koji uzrokuju MLD tako da je u tim slučajevima biohemijski test još uvijek potreban.
Liječenje[uredi | uredi izvor]
Još uvijek ne postoji terapija ili lijek za MLD kod kasno infantilnih pacijenata koji imaju simptome ili kod maloljetnika i odraslih s naprednim simptomima. Ovi pacijenti obično primaju klinički tretman usmjeren na upravljanje bolovima i simptomima.
Pre-simptomatski kasno infantilni MLD pacijenti, kao i oni sa maloljetničkom ili kod odraslih sa MLD koji su ili presimptomatski ili pokazuju blage simptome, mogu razmotriti transplantaciju koštane srži (uključujući transplantaciju matičnih ćelija), što može usporiti progresija bolesti u centralnom nervnom sistemu. Međutim, rezultati u perifernom živčanom sistemu bili su manje dramatični i dugoročni rezultati ovih terapija bili su mješoviti. Nedavni uspjeh uključivao je uzimanje matičnih ćelija iz koštane srži djece s poremećajem i zarazu ćelija retrovirusima, zamjenjujući mutirani gen matičnih ćelija popravljenim genom prije ponovnog ubrizgavanja u pacijenta gdje se umnožavaju. Djeca do pete godine bila su sva u dobroj kondiciji i išla su u vrtić kada djeca koja boluju od te dobi obično ne mogu ni govoriti.[9]
Istražuje nekoliko terapijskih mogućnosti koristeći klinička ispitivanja, prvenstveno kod kasno infantilnih pacijenata. Te terapije uključuju gensku, enzimsku (ERT), supstrat-redukcijsku (SRT) i terapiju za pojačavanje enzima (EET).
Genska terapija predata je EMA-i na verifikaciju u decembru 2019.[10] The trial sponsor has indicated they will are targeting submission for US FDA review during 1st half 2021.[11]
Dana 15. oktobra 2020. Komitet za lijekove za ljudsku upotrebu (CHMP) Evropske agencije za lijekove (EMA) usvojio je pozitivno mišljenje, preporučujući davanje odobrenja za stavljanje u promet lijeka Libmeldy (autologna populacija obogaćena CD34 + ćelijama koja sadrži hematopoetske matične i progenitorne ćelije transducirane ex vivo upotrebom lentivirusnog vektora koji kodira ljudski gen arilsulfataza A), gensku terapiju za liječenje „kasno infantilne“ djece (LI) ili „ranihm maloljetnika“ ( EJ) sa oblicima metahromatske leukodistrofije (MLD).[12] Aktivna supstanca Libmeldyja sastoji se od dječijih matičnih ćelija koje su modificirane tako da sadrže aktivne kopije gena ARSA.[12] Libmeldy was approved for medical use in the EU in December 2020.[13]
Libmeldy je indiciran za upotrebu kod djece s 'kasno infantilnim' ili 'ranojuvenilnim' oblicima MLD-a, koja su identificirani kao nositelji oštećenog gena, ali još uvijek nisu razvili simptome.[14] Također je indiciran kod djece kojoj je dijagnosticiran rani juvenilni oblik i kod koje su se počeli razvijati simptomi, ali još uvijek mogu samostalno hodati i prije početka kognitivnog opadanja.< ref name = "EMA PR"/> Libmeldy je lijek za gensku terapiju, za koji se CD34 + hematopoetske matične i matične ćelije prikupljaju ili iz koštane srži pacijenta ili iz mobilizirane periferne krvi.[14] Ove ćelije modificirane su tako da ubace funkcionalni gen za proizvodnju enzima ARSA.[14] Kada se ubrizgaju natrag pacijentu kao jednokratna infuzija, očekuje se da počnu proizvoditi ARSA enzim koji razgrađuje nakupljanje sulfatida u nervnim ćelijama i drugim ćelijama pacijentovog tijela.[14]
Epidemiologija[uredi | uredi izvor]
Procjenjuje se da se učestalost metahromatske leukodistrofije javlja kod 1 /40.000 do 1/160.000 jedinki širom svijeta. U nekim genetički izoliranim populacijama, kao što je npr. 1/75 u Habbanita (maloj grupi Jevreja koji su se doselili u Izrael iz južne Arabije), 1/2500 u zapadnom dijelu poplacije Navaho( i 1/8.000 među arapskim grupama u Izraelu.[15]
Kao autosomno recesivna bolest, 1/40 000 odgovara 1:100 nositelja u općoj populaciji.[16]
Procjenjuje se da se godišnje rodi 3.600 MLD, s 1.900 živih u SAD-u, 3.100 u Europi i 49.000 MLD živih širom svijeta.
MLD se smatra rijetkom bolešću u SAD-u i drugim zemljama.
See also[uredi | uredi izvor]
Referenc[uredi | uredi izvor]
- ^ a b Le, Tao; Bhushan, Vikas; Hofmann, Jeffrey (2012). First Aid for the USMLE Step 1. McGraw-Hill. str. 117.
- ^ Poeppel P, Habetha M, Marcao A, Büssow H, Berna L, Gieselmann V (mart 2005). "Missense mutations as a cause of metachromatic leukodystrophy, Degradation of arylsulfatase A in the endoplasmic reticulum". FEBS J. 272 (5): 1179–88. doi:10.1111/j.1742-4658.2005.04553.x. PMID 15720392. S2CID 9371615.
- ^ a b c d Fluharty, Arvan. "Arylsulfatase A Deficiency: Metachromatic Leukodystrophy, ARSA Deficiency". GeneReviews, 2006
- ^ Kishimoto Y, Hiraiwa M, O'Brien JS (Sep 1992). "Saposins: structure, function, distribution, and molecular genetics". J. Lipid Res. 33 (9): 1255–67. PMID 1402395.CS1 održavanje: više imena: authors list (link)
- ^ "Genetics". MLD Foundation. Arhivirano s originala, 22. 12. 2014. Pristupljeno 28. 5. 2017.
- ^ Blomqvist, M.; Gieselmann, V.; Mansson, J. E. (2011). "Accumulation of lysosulfatide in the brain of arylsulfatase A-deficient mice". Lipids in Health and Disease. 10 (1): 28. doi:10.1186/1476-511X-10-28. PMC 3041674. PMID 21299873.
- ^ Hohenschutz, C; Eich P; Friedl W; Waheed A; Conzelmann E; Propping P. (april 1989). "Pseudodeficiency of arylsulfatase A". Human Genetics. 82 (1): 45–8. doi:10.1007/bf00288270. PMID 2565866. S2CID 32274162.
- ^ Herz, Barbara; Bach, G. (1984). "Arylsulfatase A in pseudodeficiency". Human Genetics. 66 (2–3): 147–150. doi:10.1007/BF00286589. PMID 6143719. S2CID 2349721.
- ^ Biffi A, Montini E, Lorioli L, et al. (2013). "Lentiviral hematopoietic stem cell gene therapy benefits metachromatic leukodystrophy". Science. 341 (6148): 1233158. doi:10.1126/science.1233158. PMID 23845948. S2CID 206546808.
- ^ American, Pharmaceutical Review. "Orchard Therapeutics Announces MAA Filing of Metachromatic Leukodystrophy Treatment". American Pharmaceutical Review. CompareNetworks. Pristupljeno 3. 12. 2019.
- ^ Globe, NewsWire. "Orchard Therapeutics Outlines Business Impact of COVID-19". GlobeNewsWire. GlobeNewsWire. Pristupljeno 31. 3. 2020.
- ^ a b "Libmeldy: Pending EC decision". European Medicines Agency (EMA). 16. 10. 2020. Arhivirano s originala, 17. 10. 2020. Pristupljeno 16. 10. 2020. Text was copied from this source which is © European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ^ "Libmeldy EPAR". European Medicines Agency (EMA). 13. 10. 2020. Pristupljeno 22. 12. 2020.
- ^ a b c d "New gene therapy to treat rare genetic disorder metachromatic leukodystrophy". European Medicines Agency (EMA) (Press release). 16. 10. 2020. Pristupljeno 16. 10. 2020. Tekst je kopiran iz ovog izvora koji je © Europska agencija za lijekove. Reprodukcija je odobrena pod uslovom da je naveden izvor.
- ^ Metachromatic leukodystrophy at Genetics Home Reference. Reviewed September 2007
- ^ "MLD 101: Genetics". www.mldfoundation.org. 6. 1. 2017. Arhivirano s originala, 30. 12. 2013. Pristupljeno 6. 1. 2017.
- Neki dijelovi ovog članka objavljeni su u tekstu iz javnog domena koji je dostupan u Nacionalnom institutu za neurološke poremećaje i moždani udar:
- "NINDS Metachromatic Leukodystrophy Information Page". Arhivirano s originala, 3. 6. 2009. Pristupljeno 7. 6. 2009.
