Metiltransferaza

Prema PDB], strana 4J83.)
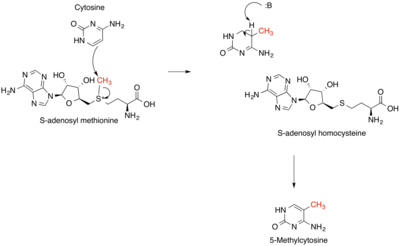
Za pojednostavljenje, prikazani su samo SAM kofaktor i citozin ska baza.
Metiltransferaze su velika grupa enzima, od kojih svi metiliraju svoje podloge, ali se, na osnovu strukturnih karakteristika, mogu podijeliti u nekoliko potklasa, Najčešća klasa metiltransferaza je klasa I, u kojoj sve sadrže Rossmanov nabor za vezivanje S-adenozil metionina (SAM). Klasa II metiltransferaza sadrže SET domen, naprimer SET domen su histonske metiltransferaze , a klas III metiltransferaza su vezane za membranu.[1][2]
Metiltransferaza se mogu grupirati na različite vrste , koje koriste različite podloge u reakcijama prijenosa metila. Ove vrste uključuju protein metiltransferaza, DNK metiltransferaze, prirodni proizvod metiltransferaza i ne-SAM ovisna metiltransferaza. SAM je klasični metil donor za metiltrasferaze, međutim, u prirodi su nađeni i primjeri drugih donora. Opći mehanizam za prijenos metila je SN2 – kao nukleofilni napad, gdje metionin sumpor služi kao nukleofil da prenosi metil grupu podloge enzima. Tokom ovog procesa, SAM se pretvara u S-adenozil homocistein (SAH) tokom ovog procesa. Razgradnja SAM-metil veza i formiranje metil veza podloge dogoditi gotovo istovremeno. Ove enzimskih reakcija su umiješane u mnoge putetev i upleteni u genetičke bolesti, rak i metaboličke bolesti.[3]
Funkcije[uredi | uredi izvor]
Genetika[uredi | uredi izvor]
Metilacija, kao i druge epigenetičke modifikacije, utiče na transkripciju, gensku stabilnost i roditeljsko utiskivanje. To direktno utiče na strukturu hromatina i mogu modulirati transkripciju gena, ili čak potpuno utišati funkciju gena ili aktivirati gen, bez mutacija samog gena. Iako su mehanizmi ove genetičke kontrole složeni, u mnoge bolesti su uključene hipo- i hipermetilacija DNK.[4][5][6]
Regulacija proteina[uredi | uredi izvor]
Metilacije proteina ima regulacijsku ulogu u interakcijama protein-protein, protein-DNK i aktivaciji proteina.
Primjeri: RCC1, važan mitotski protein, je metilizizan tako da može komunicirati sa centromerama hromosoma. Ovo je primjer regulacije interakcije protein-protein, kako metilacija regulira pričvršćivanje RCC1 na histonske proteine H2A i H2B. Interakcija RCC1-hromatina je također primjer interakcije protein-DNK, kao još jedan domen RCC1 komuniciranja direktno sa DNK kada se ovaj protein metilizira. Kada RCC1 nije metil, dijeljenjem ćelije imaju više polova vretena i obično ne mogu preživjeti.
p53 metilacija lizina regulira aktiviranje i interakciju s drugim proteinima u odgovoru na oštećenja DNK. Ovo je primjer regulacije interakcije protein-protein i aktivacije proteina. p53 je poznat tumor supresor koji aktivira puteve popravka DNK , inicira apoptozu, i pauzira ćelijski ciklus. Sve u svemu, on je odgovaran za mutacije u DNK, signalizirajući ćeliji da ih popravi ili da se pokrene ćelijska, tako da ove mutacije ne mogu doprinijeti pojavi raka.
NF-kB (protein uključen u upale) je poznata metilacijska meta metiltransferaza SETD6, što isključuje N-kB signalizaciju, inhibirajući jednu od njegovih podjedinica, Rela. Time se smanjuje transkripcijsko aktiviranje i upalni odgovor, što znači da je metilacijski NF-kB regulatorni proces stsignaliziranja kroz ovaj put reduciran.
Prirodni metiltransferazni proizvodi pružaju razne ulaza u metaboličke puteva, uključujući dostupnost kofaktora, signalnih molekula i metabolita. Ovo regulira različite ćelijski puteve, putem kontrole aktivnosti proteina.[7][8]
Primjeri[uredi | uredi izvor]
Primjeri su:
- Katehol-O-metil transferaza;
- DNK metiltransferaza
- Histon metiltransferaza
- 5-Metiltetrahidrofolat-homocistein metiltransferaza
- O-metiltransferaza
- Metionin sintaza
- 5-Metiltetrahidrofolat:corrinoid/željezo-sumpor protein ko-metiltransferaza
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Kapur Pojskić L. (2014). Uvod u genetičko inženjerstvo i biotehnologiju, 2. izdanje. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo. ISBN 978-9958-9344-8-3.
- ^ Hadžiselimović R., Pojskić N. (2005). Uvod u humanu imunogenetiku. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo. ISBN 9958-9344-3-4.
- ^ Katz, J. E.; Dlakic, M; Clarke S (18. 7. 2003). "Automated identification of putative methyltransferases from genomic open reading frames". Molecular & Cellular Proteomics. doi:10.1074/mcp.M300037-MCP200.
- ^ Siedlecki, Zielenkiewicz: "Mammalian DNA methyltransferases", Acta Biochim. Pol., 2006
- ^ Voet D., Voet J. G. Biochemistry, 3rd Ed.[publisher= Wiley. ISBN 978-0-471-19350-0.
- ^ Bajrović K, Jevrić-Čaušević A., Hadžiselimović R., Eds. (2005). Uvod u genetičko inženjerstvo i biotehnologiju. Institut za genetičko inženjerstvo i biotehnologiju (INGEB) Sarajevo. ISBN 9958-9344-1-8.CS1 održavanje: više imena: authors list (link)
- ^ http://www.phosphosite.org/proteinAction.do?id=5489 RCC1.
- ^ Levy, Dan; et al. (5. 12. 2010). "Lysine methylation of the NF-κB subunit RelA by SETD6 couples activity of the histone methyltransferase GLP at chromatin to tonic repression of NF-κB signaling". Nature Immunology. 12 (1): 29–36. doi:10.1038/ni.1968.
Vanjski linkovi[uredi | uredi izvor]
Methyltransferases na US National Library of Medicine Medical Subject Headings (MeSH)
3-D Structure of DNA Methyltransferase Arhivirano 4. 3. 2016. na Wayback Machine
A novel methyltransferase : the 7SK snRNA Methylphosphate Capping Enzyme as seen on Flintbox
"The Role of Methylation in Gene Expression" on Nature Scitable
"Nutrition and Depression: Nutrition, Methylation, and Depression" on Psychology Today
"DNA Methylation - What is DNA Methylation?" from News-Medical.net
"Histone Lysine Methylation" Genetic pathways involving Histone Methyltransferases from Cell Signaling Technology
