Razlika između verzija stranice "Glicin"
| [pregledana izmjena] | [pregledana izmjena] |
m →top: de-Yahadzizacija, replaced: |palac| → |mini| (2), replaced: mini|mini → mini (2) |
No edit summary |
||
| Red 1: | Red 1: | ||
{{Čišćenje}}{{Preuređivanje}} |
|||
{{Infokutija hemijski spoj |
{{Infokutija hemijski spoj |
||
| Strukturna formula = NCC(O)=O |
| Strukturna formula = NCC(O)=O |
||
| Hemijski spoj =Glicin |
| Hemijski spoj =Glicin |
||
| Druga imena = |
| Druga imena = Aminoetanska kiselina<br/>Aminosirćetna kiselina |
||
| Sumarna formula =C=2 H=5 N=1 O=2<br>C<sub>2</sub>H<sub>5</sub>NO<sub>2</sub> |
| Sumarna formula =C=2 H=5 N=1 O=2<br>C<sub>2</sub>H<sub>5</sub>NO<sub>2</sub> |
||
| CAS registarski broj =56-40-6 |
| CAS registarski broj =56-40-6 |
||
Verzija na dan 20 juni 2017 u 19:23
Ovaj članak zahtijeva čišćenje. |
Ovom članku potrebna je jezička standardizacija, preuređivanje ili reorganizacija. |
| Glicin | |
|---|---|
| NCC(O)=O | |
| Općenito | |
| Hemijski spoj | Glicin |
| Druga imena | Aminoetanska kiselina Aminosirćetna kiselina |
| Molekularna formula | C=2 H=5 N=1 O=2 C2H5NO2 |
| CAS registarski broj | 56-40-6 |
| Kratki opis | Bijela supstanca |
| Osobine1 | |
| Molarna masa | 75.07 |
| Gustoća | 1.1607 g/cm3 |
| Tačka topljenja | 233 °C (razlaže se) |
| Rastvorljivost | Rastvorljiv u etanolu i piridinu: 25 g/100 mL Nerastvorljiv u eteru |
| 1 Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
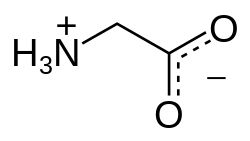

Glicin (Gly i G) ili α-aminosirćetna kiselina je najjednostavnija, od 20 aminokiselina koje ulaze u sastav proteinskih lanaca. U strukturi nema nijedan asimetrični atom ugljika. U organizmu se može proizvesti iz drugih aminokiselina, tako da ne spada u esencijalne aminokiseline.[1]
Sinteza
Glicin se nastaje od serina i treonina, te iz glioksalne kiseline i sarkozina.
- Najvažniji put sinteze glicina je transformacija serina. Reakcija se odvija uz katalitičko djelovanje enzima zvanog serin hidroksimetiltransferaza, čija aktivnost zahtijeva učešće vitamin B6 (piridoksal fosfat). Za tu reakciju je neophodna tetrahidrofolna kiselina od koje, nekon rekcije, nastaje metilen tetrahidrofolna kiselina.
- Glicin može nastati i iz glioksalne kiseline, pod uticajem enzima glicin aminitransferaza. Taj enzim prenosi amino grupu sa glutaminske kiseline na glioksalnu kiselinu kao primatelja, pri čemu nastaju glicin i α-ketoglutarna kiselina.
- Iz sarkozin (metil-glicina) katalizom enzima sarkozin oksidaza nastaje glicin, a izdvaja se formaldehid.
- Glicin može nastati i iz aminokiseline treonina, pod uticajem enzima treonin aldolaza, ali je značaj ove reakcije mali.
Razgradnja
- Od glicina i metilen tetrahidrofolne kiseline nastaje serin (obrnuta rekcija od one u sintezi). Razgradnjom serina stvara se pirogrožđana kiselina, po čemu se glicin svrstava u glikogene aminokiseline.
- Transaminacijom glicina sa α-ketoglutarnom kiselinom nastaju glioksalna i glutaminska kiselina. Zatim, oksidacijom glioksalne, nastaje oksalna kiselina. Oksalna kiselina može uzrokovati pojavu oksalatnih bubrežnih kamenaca.
- Jedan od najvažnijih puteva razgradnje glicina je cijepanje na ugljen dioksid, amonijev ion i metilen grupu koja se veže za tetrahidrofolnu kiselinu. U toj reakciji, koju katalizira enzimski kompleks glicin sintaza , stvara se metilen tetrahidrofolna kiselina
Kiselinsko-bazna svojstva i strukture
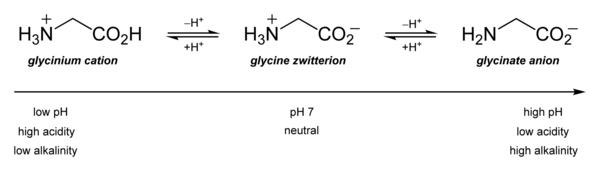
U vodenom rastvoru, glicin je amfoteričan: pri niskom pH molekule mogu imati pKa od oko 2.4, a na visokom pH gube proton pri pKa od oko 9.6 (preciznije pKa zavisi od temperature i ionske snage). Priroda glicina u vodenoj otopini je istraživana i teorijskim metodima.[2] Ispostavilo se da je u rastvoru odnos koncentracija dva izomera nezavisan i od analitičke koncentracije i od pH. Ovaj odnos je jednostavna ravnotežna konstanta za izomerizaciju:
Uočeno je, putem mikrotalasne spektroskopije, da su oba izomera glicina u plinskoj fazi.[3] Struktura čvrstog stanja je detaljno analizirana.[4]
Uloga
- Glicin učestvuje u sintezi proteina i raznih drugih jedinjenja:
- Kreatina;
- Porfirina;
- Purina;
- glikoholne kiseline:
- hipurne kiseline;
- Serina.
- Žučne kiseline proizvedene u jetri konjugiraju sa glicinom i taurinom, pri čemu nastaju odgovarajuće (koljugirane) kiseline: glikoholna, glikohenodokesiholna, tauroholna i taurohenodeoskiholna kiselina.
- Glicin je, u nervnom sistemu, značajan inhibitorni neurotransmiter.
Poremećaji
- Glicinurija je povećano izlučivanje glicina u mokraći. Javlja se kod osoba sa poremećajima trasporta glicina tubulskom sloju u bubrega.
- Hiperglicinemija se ispoljava u povećanoj koncentraciji glicaina u krvi. Uzrok te pojave poremećaj u enzimskom sistemu procesa razgradnje glicina.
- Hiperoksalurija je pojačano izlučivanje oskalne kiseline u mokraći, zbog čega se vrlo rano, u dječijm uzrastu, javljaju bibrežni kamenci i infekcije, kao i bubrežna insuficijencija.
- Hipersarkozinemija nastaje zbog manjka enzima sarkozin oksidaze u organizmu, usljed čega se sarkozin prekomjerno nagomilava. Ovo oboljenje uzrokuje do mentalne retardacije.
Također pogledajte
Reference
- ^ Hall John E., Guyton A. C. (2006): Textbook of medical physiology, 11th edition. Elsevier Saunders, St. Louis, Mo, ISBN 0-7216-0240-1.
- ^ Bonaccorsi, R.; Palla, P.; Tomasi, J. (1984). "Conformational energy of glycine in aqueous solutions and relative stability of the zwitterionic and neutral forms. An ab initio study". J. Amer. Chem. Soc. 106 (7): 1945–1950. doi:10.1021/ja00319a008.
- ^ Suenram R. D., Lovas F. J. (1980): Millimeter wave spectrum of glycine. A new conformer. J. Amer. Chem. Soc., 102 (24): 7180–7184.
- ^ Jönsson P.-G., Kvick Å. (1972): Precision neutron diffraction structure determination of protein and nucleic acid components. III. The crystal and molecular structure of the amino acid -glycine Precision neutron diffraction structure determination of protein and nucleic acid components. III. The crystal and molecular structure of the amino acid -glycine, B28 (6): 1827–1833.
Vanjski linkovi
- Portal|Hemija
| Commons ima datoteke na temu: Glicin |

![{\displaystyle K=\mathrm {\frac {[H_{3}N^{+}CH_{2}CO_{2}^{-}]}{[H_{2}NCH_{2}CO_{2}H]}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/80281edf6f4791a13bbe2bd60977ae8cb2e970e0)
