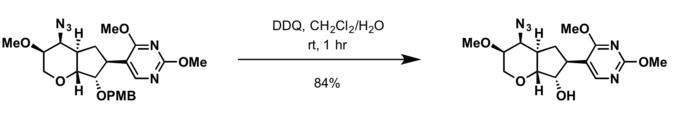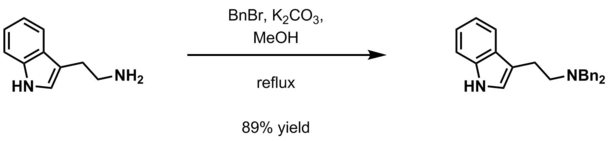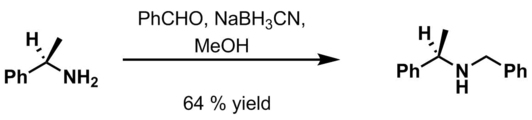Razlika između verzija stranice "Benzil grupa"
| [pregledana izmjena] | [pregledana izmjena] |
No edit summary |
No edit summary |
||
| Red 1: | Red 1: | ||
{{Preuređivanje}}{{Čišćenje}} |
|||
| ⚫ | |||
| ⚫ | '''Benzil grupa''' ili '''benzil''' je |
||
| ⚫ | |||
==Nomenklatura== |
|||
| ⚫ | '''Benzil grupa''' ili '''benzil''' je [[supstituent]] ili molekulski fragment koji ima strukturu C<sub>6</sub>H<sub>5</sub>CH<sub>2</sub>–. Benzilska svojstva [[benzen]]skog prstena vezana su za CH<sub>2</sub> grupu.<ref>{{cite book|last=Carey |first=F. A. |last2=Sundberg |first2=R. J. |title=Advanced Organic Chemistry, Part A: Structure and Mechanisms |edition=5th |publisher=Springer |location=New York, NY |date=2008 |pages=806–808, 312–313 |ISBN=9780387448978}}</ref> |
||
| ⚫ | |||
| ⚫ | |||
== |
== Nomenklatura == |
||
| ⚫ | |||
| ⚫ | Skraćenica |
||
| ⚫ | Naziv '''benzilski''' je upotrijebljen za opis položaja prvog [[ugljik]]a koji je vezan za benzen ili drugi [[aromatičnost|aromatski]] prsten. Naprimjer, [[molekula]] koja se ponaša kao "benzilski" karbokation. Benzilski [[slobodni radikal]] ima formulu {{chem|C|6|H|5|CH|2|•}}. Benzilski [[karbokation]] ima formulu {{chem|C|6|H|5|CH|2|+}}, a [[karbanion]]: {{chem|C|6|H|5|CH|2|−}}. Nijedna od ovih vrsta ne može nastati u značajnoj količini pod normalnim okolnostima, ali su upotrebljivi u diskusiji o [[mehanizam reakcije|mehanizmima reakcije]]. |
||
=== Skraćenice === |
|||
| ⚫ | Skraćenica "Bn" se često upotrebljava za označavanje benzil groupa u nomenklaturi i prikazima strukture [[Hemijski spojevi|hemijskih spojeva]]. Naprimjer, [[benzil alkohol]] može biti predstavljen kao BnOH. Ova skraćenica se ne treba miješati sa "Bz", koja se odnosi n [[benzoil]] grupu C<sub>6</sub>H<sub>5</sub>C(O)– ili [[fenil grupa|fenil grupu]] C<sub>6</sub>H<sub>5</sub>, skraćeno "Ph". |
||
== Reaktivnost benzilskih centara == |
== Reaktivnost benzilskih centara == |
||
Poboljšana |
Poboljšana reaktivnost benzilskih mjesta pripisuje se niskoj [[energija disocijacije veze|energiji razlaganja veze]] za benzilsku C-H vezu. Naime, veza C<sub>6</sub>H<sub>5</sub>CH<sub>2</sub>−H je oko 10-15% slabija u odnosu na druge vrste C-H veza. Susjedni aromatski prsten stabilizuje benzil radikale. U sljedećoj tabeli su upoređeni podaci o benzilskim C-H vezama u odnosu na njihovu snagu. |
||
{| class="wikitable" style = "text-align:center" |
{| class="wikitable" style = "text-align:center" |
||
|- |
|- |
||
| Red 26: | Red 26: | ||
|90 |
|90 |
||
|377 |
|377 |
||
| |
|Benzilske do alilske C−H veze<br> (takve veze pokazuju poboljšanu reaktivnost) |
||
|- |
|- |
||
|H<sub>3</sub>C−H |
|H<sub>3</sub>C−H |
||
| Red 44: | Red 44: | ||
|113 |
|113 |
||
|473 |
|473 |
||
| |
|Uporediva sa vinil radikalom, rijetka |
||
|- |
|- |
||
|CH<sub>2</sub>=CHCH<sub>2</sub>−H |
|CH<sub>2</sub>=CHCH<sub>2</sub>−H |
||
| Red 54: | Red 54: | ||
|} |
|} |
||
Najslabija od |
Najslabija od C−H veza odražava stabilnost benzilnih radikala. Iz povezanih razloga, benzilski supstituenti ispoljavaju poboljšanu reaktivnost kao u [[KMnO4 # Organska hemija|oksidaciji]], [[halogenacija slobodnih radikala|halogenaciji slobodnih radikala]] ili [[hidrogenoliza|hidrogenolizi]]. Kao praktičan primjer može biti kada, u prisutnosti odgovarajućih katalizatora, ''P''-[[ksilen]] oksidira isključivo na benzilnim mjestima i daje [[tereftalna kiselina|tereftalnu kiselinu]]: |
||
:CH<sub>3</sub>C<sub>6</sub>H<sub>4</sub>CH<sub>3</sub> + 3 O<sub>2</sub> → HO<sub>2</sub>CC<sub>6</sub>H<sub>4</sub>CO<sub>2</sub>H + 2 H<sub>2</sub>O. |
:CH<sub>3</sub>C<sub>6</sub>H<sub>4</sub>CH<sub>3</sub> + 3 O<sub>2</sub> → HO<sub>2</sub>CC<sub>6</sub>H<sub>4</sub>CO<sub>2</sub>H + 2 H<sub>2</sub>O. |
||
Ovom metodom, godišnje se proizvedu milioni tona tereftalne kiseline.<ref>Richard J. Sheehan: Terephthalic Acid, Dimethyl Terephthalate, and Isophthalic Acid; doi: 10.1002/14356007.a26_193.</ref> |
|||
==Kao zaštitna grupa == |
== Kao zaštitna grupa == |
||
=== |
=== Zaštita alkohola === |
||
[[Datoteka:BenzylEther.png|thumb|171x171px|Benzil grupa štiti |
[[Datoteka:BenzylEther.png|thumb|171x171px|Benzil grupa štiti [[alkohol]].]] |
||
Benzil, |
Benzil, skraćeno kao '''Bn''', obično se upotrebljava u organskoj sintezi robusne zaštitne grupe za [[alkohol]]e i [[karboksilne kiseline]]. |
||
==== |
==== Najčešće metode zaštite ==== |
||
* Tretman alkohola jakom bazom, kao što su u prahu [[kalij-hidroksid]] |
* Tretman alkohola jakom [[Baza (hemija)|bazom]], kao što su one u prahu poput: [[kalij-hidroksid]], [[natrij-hidrid]], benzil halid ([[benzil hlorid | BnCl]] i [[benzil bromid|BnBr]]).<ref name=":0">{{Cite book|url=http://doi.wiley.com/10.1002/0470053488|title=Greene's Protective Groups in Organic Synthesis|edition=4th|publisher=Wiley Online Library|last=Wuts|first=Peter G. M.|last2=Greene|first2=Theodora W.|doi=10.1002/0470053488}}</ref><ref>{{Cite journal|last=Fukuzawa|first=Akio|last2=Sato|first2=Hideaki|last3=Masamune|first3=Tadashi|date=1987-01-01|title=Synthesis of (±)-prepinnaterpene, a bromoditerpene from the red alga Yamada|url=http://www.sciencedirect.com/science/article/pii/S0040403900964918|journal=Tetrahedron Letters|volume=28|issue=37|pages=4303–4306|doi=10.1016/S0040-4039(00)96491-8}}</ref> |
||
*:[[Datoteka:BnProtectedalcohol.png|none|455x455px]] |
*:[[Datoteka:BnProtectedalcohol.png|none|455x455px]] |
||
* Monobenzilacija [[diol]]a može se postići upotrebom |
* Monobenzilacija [[diol]]a može se postići upotrebom [[srebro|Ag<sub>2</sub>O]] u [[dimetilformamid]]u (DMF) u uslovima povišenih [[temperatura]].<ref>{{Cite journal|last=Van Hijfte|first=Luc|last2=Little|first2=R. Daniel|date=1985-10-01|title=Intramolecular 1,3-diyl trapping reactions. A formal total synthesis of (±)-coriolin|url=http://dx.doi.org/10.1021/jo00220a058|journal=The Journal of Organic Chemistry|volume=50|issue=20|pages=3940–3942|doi=10.1021/jo00220a058|issn=0022-3263}}</ref> |
||
* [[Primarni alkohol]]i mogu se selektivno |
* [[Primarni alkohol]]i mogu se selektivno benzilirati u prisustvu fenolnih funkcijskih grupa, upotrebom [[Metal-acetilacetonat|Cu(acac)<sub>2</sub>]]<ref>{{Cite journal|last=Sirkecioglu|first=Okan|last2=Karliga|first2=Bekir|last3=Talinli|first3=Naciye|date=2003-11-10|title=Benzylation of alcohols by using bis[acetylacetonato]copper as catalyst|url=http://www.sciencedirect.com/science/article/pii/S004040390302224X|journal=Tetrahedron Letters|volume=44|issue=46|pages=8483–8485|doi=10.1016/j.tetlet.2003.09.106}}</ref> |
||
==== Najčešći metodi otklanjanja zaštite==== |
==== Najčešći metodi otklanjanja zaštite ==== |
||
Benzil etri mogu se ukloniti |
Benzil etri mogu se ukloniti pod ''[[redoks|redukcijskim]] i [[oksidacija|oksidacijskim uslovima]], kao i upotrebom ''Lewisovih kiselina''.<ref name=":0" /> |
||
=====Redukcijski |
===== Redukcijski uslovi ===== |
||
* Za otklanjanje se upotrebljava |
* Za otklanjanje se upotrebljava [[hidrogenoliza]].<ref>{{Cite journal|last=Smith|first=Amos B.|last2=Zhu|first2=Wenyu|last3=Shirakami|first3=Shohei|last4=Sfouggatakis|first4=Chris|last5=Doughty|first5=Victoria A.|last6=Bennett|first6=Clay S.|last7=Sakamoto|first7=Yasuharu|date=2003-03-01|title=Total Synthesis of (+)-Spongistatin 1. An Effective Second-Generation Construction of an Advanced EF Wittig Salt, Fragment Union, and Final Elaboration|url=http://dx.doi.org/10.1021/ol034037a|journal=Organic Letters|volume=5|issue=5|pages=761–764|doi=10.1021/ol034037a|issn=1523-7060}}</ref> |
||
*:[[Datoteka:BnEtherExample.png|none|626x626px]] |
*:[[Datoteka:BnEtherExample.png|none|626x626px]] |
||
* Jednostruki |
* Jednostruki elektronski proces sa [[natrij|Na]]/[[amonijak|NH<sub>3</sub>]] ili [[litij|Li]]/NH<sub>3</sub> |
||
=====Oksidacijski |
===== Oksidacijski uslovi ===== |
||
* Benzilske zaštitne grupe mogu se ukloniti upotrebom širokog izbora oksidacijskih |
* Benzilske zaštitne grupe mogu se ukloniti upotrebom širokog izbora oksidacijskih agensa, uključujući: |
||
** [[hrom-trioksid|CrO<sub>3</sub>]]/[[acetatna kiselina]] |
** [[hrom-trioksid|CrO<sub>3</sub>]]/[[acetatna kiselina]] na sobnoj temperaturi; |
||
** [[Ozon]]; |
** [[Ozon]]; |
||
** [[N-Bromosukcinimid|''N''-Bromosukcinimid]] (NBS); |
** [[N-Bromosukcinimid|''N''-Bromosukcinimid]] (NBS); |
||
** ''N''-Jodosukcinimid (NIS); |
** ''N''-Jodosukcinimid (NIS); |
||
=====Na bazi [[Lewisove kiseline]]===== |
===== Na bazi [[Lewisove kiseline]] ===== |
||
* [[Trimetilsilil]] jodid (Me<sub>3</sub>SiI) u [[dihlorometan]]u na sobnoj temperaturi ( |
* [[Trimetilsilil]] jodid (Me<sub>3</sub>SiI) u [[dihlorometan]]u na sobnoj temperaturi (selektivnost se postiže pod posebnim uslovima); |
||
===Zaštitna |
=== Zaštitna ''p''-metoksibenzil grupa === |
||
''p''-Metoksibenzil ('''PMB''') |
''p''-Metoksibenzil ('''PMB''') se upotrebljava kao [[zaštitna grupa]] za [[alkohol]]e u [[organska sinteza|organskoj sintezi]]. |
||
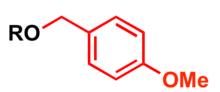
[[Datoteka:PMB_Ether.png|thumb|Zaštitna |
[[Datoteka:PMB_Ether.png|thumb|Zaštitna ''p''-metoksibenzil grupa.]] |
||
==== |
==== Najčešće zaštitne metode ==== |
||
* Jake |
* Jake baze, kao što su ojačani [[natrij-hidroksid]] ili [[kalij-hidrid]] i ''p''-metoksibenzil halid (hlorid ili bromid)<ref>{{Cite journal|last=Marco|first=José L.|last2=Hueso-Rodríguez|first2=Juan A.|date=1988-01-01|title=Synthesis of optically pure 1-(3-furyl)-1,2-dihydroxyethane derivatives|url=http://www.sciencedirect.com/science/article/pii/S0040403900879071|journal=Tetrahedron Letters|volume=29|issue=20|pages=2459–2462|doi=10.1016/S0040-4039(00)87907-1}}</ref><ref>{{Cite journal|last=Takaku|first=Hiroshi|last2=Kamaike|first2=Kazuo|last3=Tsuchiya|first3=Hiromichi|date=1984-01-01|title=Oligonucleotide synthesis. Part 21. Synthesis of ribooligonucleotides using the 4-methoxybenzyl group as a new protecting group for the 2′-hydroxyl group|url=http://dx.doi.org/10.1021/jo00175a010|journal=The Journal of Organic Chemistry|volume=49|issue=1|pages=51–56|doi=10.1021/jo00175a010|issn=0022-3263}}</ref>; |
||
* 4-metoksibenzil-2,2,2-trihloroacetimidat može se |
* 4-metoksibenzil-2,2,2-trihloroacetimidat može se upotrijebiti za instaliranje grupe PMB u prisustvu: |
||
** [[Skandij (III) trifluorometanesulfonat|Scandiij (III) triflata]] (Sc(OTf)<sub>3</sub>) u toluenu na |
** [[Skandij (III) trifluorometanesulfonat|Scandiij (III) triflata]] (Sc(OTf)<sub>3</sub>) u toluenu na 0 °C<ref>{{Cite journal|last=Trost|first=Barry M.|last2=Waser|first2=Jerome|last3=Meyer|first3=Arndt|date=2007-11-01|title=Total Synthesis of (−)-Pseudolaric Acid B|url=http://dx.doi.org/10.1021/ja076165q|journal=Journal of the American Chemical Society|volume=129|issue=47|pages=14556–14557|doi=10.1021/ja076165q|issn=0002-7863|pmc=2535803|pmid=17985906}}</ref>; |
||
** [[Trifluorometanesulfonatna kiseliina]] (TfOH) u [[dihlorometan]]u na 0 °C<ref>{{Cite journal|last=Mukaiyama|first=Teruaki|last2=Shiina|first2=Isamu|last3=Iwadare|first3=Hayato|last4=Saitoh|first4=Masahiro|last5=Nishimura|first5=Toshihiro|last6=Ohkawa|first6=Naoto|last7=Sakoh|first7=Hiroki|last8=Nishimura|first8=Koji|last9=Tani|first9=Yu-ichirou|date=1999-01-04|title=Asymmetric Total Synthesis of Taxol\R|url=http://onlinelibrary.wiley.com/doi/10.1002/(SICI)1521-3765(19990104)5:13.0.CO;2-O/abstract|journal=Chemistry – A European Journal|language=en|volume=5|issue=1|pages=121–161|doi=10.1002/(SICI)1521-3765(19990104)5:13.0.CO;2-O|issn=1521-3765}}</ref>. |
** [[Trifluorometanesulfonatna kiseliina]] (TfOH) u [[dihlorometan]]u na 0 °C<ref>{{Cite journal|last=Mukaiyama|first=Teruaki|last2=Shiina|first2=Isamu|last3=Iwadare|first3=Hayato|last4=Saitoh|first4=Masahiro|last5=Nishimura|first5=Toshihiro|last6=Ohkawa|first6=Naoto|last7=Sakoh|first7=Hiroki|last8=Nishimura|first8=Koji|last9=Tani|first9=Yu-ichirou|date=1999-01-04|title=Asymmetric Total Synthesis of Taxol\R|url=http://onlinelibrary.wiley.com/doi/10.1002/(SICI)1521-3765(19990104)5:13.0.CO;2-O/abstract|journal=Chemistry – A European Journal|language=en|volume=5|issue=1|pages=121–161|doi=10.1002/(SICI)1521-3765(19990104)5:13.0.CO;2-O|issn=1521-3765}}</ref>. |
||
**:[[Datoteka:PMBAlcohol.png|none|676x676px]] |
**:[[Datoteka:PMBAlcohol.png|none|676x676px]] |
||
==== |
==== Najčešće metode uklanjanja zaštite ==== |
||
* 2,3-Dihloro-5,6-dicijano-''p''-benzokvinon (DDQ)<ref>{{Cite journal|last=Hanessian|first=Stephen|last2=Marcotte|first2=Stéphane|last3=Machaalani|first3=Roger|last4=Huang|first4=Guobin|date=2003-11-01|title=Total Synthesis and Structural Confirmation of Malayamycin A: A Novel Bicyclic ''C''-Nucleoside from Streptomyces malaysiensis|url=http://dx.doi.org/10.1021/ol030095k|journal=Organic Letters|volume=5|issue=23|pages=4277–4280|doi=10.1021/ol030095k|issn=1523-7060}}</ref>; |
* 2,3-Dihloro-5,6-dicijano-''p''-benzokvinon (DDQ)<ref>{{Cite journal|last=Hanessian|first=Stephen|last2=Marcotte|first2=Stéphane|last3=Machaalani|first3=Roger|last4=Huang|first4=Guobin|date=2003-11-01|title=Total Synthesis and Structural Confirmation of Malayamycin A: A Novel Bicyclic ''C''-Nucleoside from Streptomyces malaysiensis|url=http://dx.doi.org/10.1021/ol030095k|journal=Organic Letters|volume=5|issue=23|pages=4277–4280|doi=10.1021/ol030095k|issn=1523-7060}}</ref>; |
||
*:[[Datoteka:PMBDeprotection.png|none|674x674px]] |
*:[[Datoteka:PMBDeprotection.png|none|674x674px]] |
||
* |
* Uslovi za uklanjanje zaštite benzil grupe su primjenljivi razlaganjem zaštitne grupe PMB. |
||
=== Zaštita amina=== |
=== Zaštita amina === |
||
[[Datoteka:Benzyl_protective_group.png|thumb|Benzil grupa štiti |
[[Datoteka:Benzyl_protective_group.png|thumb|Benzil grupa štiti [[amin (hemija)|amin]].]] |
||
Benzil grupa se |
Benzil grupa se dosta primjenjuje kao [[zaštitna grupa]] za [[amin (hemija)|amine]], u [[organska sinteza|organskoj sintezi]]. |
||
==== |
==== Najčešće metode zaštite amina ==== |
||
* Vodeni [[kalij-karbonat]] i benzil halid ([[benzil-hlorid|BnCl]], [[benzil-bromid|BnBr]]) u [[metanol]]u<ref>{{Cite journal|last=Kuehne|first=Martin E.|last2=Xu|first2=Feng|date=1993-12-01|title=Total synthesis of strychnan and aspidospermatan alkaloids. 3. The total synthesis of (±)-strychnine|url=http://dx.doi.org/10.1021/jo00078a030|journal=The Journal of Organic Chemistry|volume=58|issue=26|pages=7490–7497|doi=10.1021/jo00078a030|issn=0022-3263}}</ref>; |
* Vodeni [[kalij-karbonat]] i benzil halid ([[benzil-hlorid|BnCl]], [[benzil-bromid|BnBr]]) u [[metanol]]u<ref>{{Cite journal|last=Kuehne|first=Martin E.|last2=Xu|first2=Feng|date=1993-12-01|title=Total synthesis of strychnan and aspidospermatan alkaloids. 3. The total synthesis of (±)-strychnine|url=http://dx.doi.org/10.1021/jo00078a030|journal=The Journal of Organic Chemistry|volume=58|issue=26|pages=7490–7497|doi=10.1021/jo00078a030|issn=0022-3263}}</ref>; |
||
*:[[Datoteka:Bn_protection_with_bnbr.png|none|609x609px]] |
*:[[Datoteka:Bn_protection_with_bnbr.png|none|609x609px]] |
||
| Red 113: | Red 113: | ||
*:[[Datoteka:Bn_protection_with_benzaldehyde.png|none|532x532px]] |
*:[[Datoteka:Bn_protection_with_benzaldehyde.png|none|532x532px]] |
||
==== |
==== Najčešće metode uklanjanja zaštite amina ==== |
||
* [[Hidrogenacija]] u prisustvu [[katalizator]]a [[paladij]]a<ref>{{Cite journal|last=Zhou|first=Hao|last2=Liao|first2=Xuebin|last3=Cook|first3=James M.|date=2004-01-01|title=Regiospecific, Enantiospecific Total Synthesis of the 12-Alkoxy-Substituted Indole Alkaloids, (+)-12-Methoxy-Na-methylvellosimine, (+)-12-Methoxyaffinisine, and (−)-Fuchsiaefoline|url=http://dx.doi.org/10.1021/ol0362212|journal=Organic Letters|volume=6|issue=2|pages=249–252|doi=10.1021/ol0362212|issn=1523-7060}}</ref> |
* [[Hidrogenacija]] u prisustvu [[katalizator]]a [[paladij]]a<ref>{{Cite journal|last=Zhou|first=Hao|last2=Liao|first2=Xuebin|last3=Cook|first3=James M.|date=2004-01-01|title=Regiospecific, Enantiospecific Total Synthesis of the 12-Alkoxy-Substituted Indole Alkaloids, (+)-12-Methoxy-Na-methylvellosimine, (+)-12-Methoxyaffinisine, and (−)-Fuchsiaefoline|url=http://dx.doi.org/10.1021/ol0362212|journal=Organic Letters|volume=6|issue=2|pages=249–252|doi=10.1021/ol0362212|issn=1523-7060}}</ref> |
||
Verzija na dan 12 april 2019 u 22:16

R = heteroatom, alkil, aril, alil itd. ili ostali supstituenti.
Benzil grupa ili benzil je supstituent ili molekulski fragment koji ima strukturu C6H5CH2–. Benzilska svojstva benzenskog prstena vezana su za CH2 grupu.[1]
Nomenklatura
U IUPAC nomenklaturi prefiks benzil odnosi se na C6H5CH2 supstituent, naprimjer benzil hlorid ili benzil benzoat. Benzil ne treba brkati sa fenil sa formulom C6H5.
Naziv benzilski je upotrijebljen za opis položaja prvog ugljika koji je vezan za benzen ili drugi aromatski prsten. Naprimjer, molekula koja se ponaša kao "benzilski" karbokation. Benzilski slobodni radikal ima formulu C6H5CH•
2. Benzilski karbokation ima formulu C6H5CH+
2, a karbanion: C6H5CH−
2. Nijedna od ovih vrsta ne može nastati u značajnoj količini pod normalnim okolnostima, ali su upotrebljivi u diskusiji o mehanizmima reakcije.
Skraćenice
Skraćenica "Bn" se često upotrebljava za označavanje benzil groupa u nomenklaturi i prikazima strukture hemijskih spojeva. Naprimjer, benzil alkohol može biti predstavljen kao BnOH. Ova skraćenica se ne treba miješati sa "Bz", koja se odnosi n benzoil grupu C6H5C(O)– ili fenil grupu C6H5, skraćeno "Ph".
Reaktivnost benzilskih centara
Poboljšana reaktivnost benzilskih mjesta pripisuje se niskoj energiji razlaganja veze za benzilsku C-H vezu. Naime, veza C6H5CH2−H je oko 10-15% slabija u odnosu na druge vrste C-H veza. Susjedni aromatski prsten stabilizuje benzil radikale. U sljedećoj tabeli su upoređeni podaci o benzilskim C-H vezama u odnosu na njihovu snagu.
| Veza | Veza | Energija razlaganja veze | Kommentar | |
|---|---|---|---|---|
| (kcal/mol) | (kJ/mol) | |||
| C6H5CH2−H | Benzilska C−H veza | 90 | 377 | Benzilske do alilske C−H veze (takve veze pokazuju poboljšanu reaktivnost) |
| H3C−H | Metil C−H veza | 105 | 439 | Jedna od najjačih alifatskih C−H veza |
| C2H5−H | Etil C−H veza | 101 | 423 | Nešto slabija nego H3C−H |
| C6H5−H | Fenil C−H veza | 113 | 473 | Uporediva sa vinil radikalom, rijetka |
| CH2=CHCH2−H | Alilska C–H veza | 89 | 372 | Ovakve veze ispoljavaju poboljšanu reaktivnost |
Najslabija od C−H veza odražava stabilnost benzilnih radikala. Iz povezanih razloga, benzilski supstituenti ispoljavaju poboljšanu reaktivnost kao u oksidaciji, halogenaciji slobodnih radikala ili hidrogenolizi. Kao praktičan primjer može biti kada, u prisutnosti odgovarajućih katalizatora, P-ksilen oksidira isključivo na benzilnim mjestima i daje tereftalnu kiselinu:
- CH3C6H4CH3 + 3 O2 → HO2CC6H4CO2H + 2 H2O.
Ovom metodom, godišnje se proizvedu milioni tona tereftalne kiseline.[2]
Kao zaštitna grupa
Zaštita alkohola

Benzil, skraćeno kao Bn, obično se upotrebljava u organskoj sintezi robusne zaštitne grupe za alkohole i karboksilne kiseline.
Najčešće metode zaštite
- Tretman alkohola jakom bazom, kao što su one u prahu poput: kalij-hidroksid, natrij-hidrid, benzil halid ( BnCl i BnBr).[3][4]
- Monobenzilacija diola može se postići upotrebom Ag2O u dimetilformamidu (DMF) u uslovima povišenih temperatura.[5]
- Primarni alkoholi mogu se selektivno benzilirati u prisustvu fenolnih funkcijskih grupa, upotrebom Cu(acac)2[6]
Najčešći metodi otklanjanja zaštite
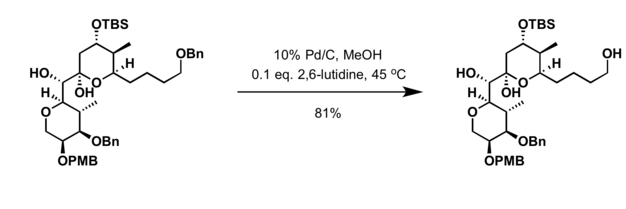
Benzil etri mogu se ukloniti pod redukcijskim i oksidacijskim uslovima, kao i upotrebom Lewisovih kiselina.[3]
Redukcijski uslovi
- Za otklanjanje se upotrebljava hidrogenoliza.[7]
- Jednostruki elektronski proces sa Na/NH3 ili Li/NH3
Oksidacijski uslovi
- Benzilske zaštitne grupe mogu se ukloniti upotrebom širokog izbora oksidacijskih agensa, uključujući:
- CrO3/acetatna kiselina na sobnoj temperaturi;
- Ozon;
- N-Bromosukcinimid (NBS);
- N-Jodosukcinimid (NIS);
Na bazi Lewisove kiseline
- Trimetilsilil jodid (Me3SiI) u dihlorometanu na sobnoj temperaturi (selektivnost se postiže pod posebnim uslovima);
Zaštitna p-metoksibenzil grupa
p-Metoksibenzil (PMB) se upotrebljava kao zaštitna grupa za alkohole u organskoj sintezi.
Najčešće zaštitne metode
- Jake baze, kao što su ojačani natrij-hidroksid ili kalij-hidrid i p-metoksibenzil halid (hlorid ili bromid)[8][9];
- 4-metoksibenzil-2,2,2-trihloroacetimidat može se upotrijebiti za instaliranje grupe PMB u prisustvu:
- Scandiij (III) triflata (Sc(OTf)3) u toluenu na 0 °C[10];
- Trifluorometanesulfonatna kiseliina (TfOH) u dihlorometanu na 0 °C[11].
Najčešće metode uklanjanja zaštite
- 2,3-Dihloro-5,6-dicijano-p-benzokvinon (DDQ)[12];
- Uslovi za uklanjanje zaštite benzil grupe su primjenljivi razlaganjem zaštitne grupe PMB.
Zaštita amina

Benzil grupa se dosta primjenjuje kao zaštitna grupa za amine, u organskoj sintezi.
Najčešće metode zaštite amina
- Vodeni kalij-karbonat i benzil halid (BnCl, BnBr) u metanolu[13];
- Benzaldehid, 6 M HCl i NaBH3CN u metanolu[14].
Najčešće metode uklanjanja zaštite amina
- Hidrogenacija u prisustvu katalizatora paladija[15]
Također pogledajte
Reference
- ^ Carey, F. A.; Sundberg, R. J. (2008). Advanced Organic Chemistry, Part A: Structure and Mechanisms (5th izd.). New York, NY: Springer. str. 806–808, 312–313. ISBN 9780387448978.
- ^ Richard J. Sheehan: Terephthalic Acid, Dimethyl Terephthalate, and Isophthalic Acid; doi: 10.1002/14356007.a26_193.
- ^ a b Wuts, Peter G. M.; Greene, Theodora W. Greene's Protective Groups in Organic Synthesis (4th izd.). Wiley Online Library. doi:10.1002/0470053488.
- ^ Fukuzawa, Akio; Sato, Hideaki; Masamune, Tadashi (1987-01-01). "Synthesis of (±)-prepinnaterpene, a bromoditerpene from the red alga Yamada". Tetrahedron Letters. 28 (37): 4303–4306. doi:10.1016/S0040-4039(00)96491-8.
- ^ Van Hijfte, Luc; Little, R. Daniel (1985-10-01). "Intramolecular 1,3-diyl trapping reactions. A formal total synthesis of (±)-coriolin". The Journal of Organic Chemistry. 50 (20): 3940–3942. doi:10.1021/jo00220a058. ISSN 0022-3263.
- ^ Sirkecioglu, Okan; Karliga, Bekir; Talinli, Naciye (2003-11-10). "Benzylation of alcohols by using bis[acetylacetonato]copper as catalyst". Tetrahedron Letters. 44 (46): 8483–8485. doi:10.1016/j.tetlet.2003.09.106.
- ^ Smith, Amos B.; Zhu, Wenyu; Shirakami, Shohei; Sfouggatakis, Chris; Doughty, Victoria A.; Bennett, Clay S.; Sakamoto, Yasuharu (2003-03-01). "Total Synthesis of (+)-Spongistatin 1. An Effective Second-Generation Construction of an Advanced EF Wittig Salt, Fragment Union, and Final Elaboration". Organic Letters. 5 (5): 761–764. doi:10.1021/ol034037a. ISSN 1523-7060.
- ^ Marco, José L.; Hueso-Rodríguez, Juan A. (1988-01-01). "Synthesis of optically pure 1-(3-furyl)-1,2-dihydroxyethane derivatives". Tetrahedron Letters. 29 (20): 2459–2462. doi:10.1016/S0040-4039(00)87907-1.
- ^ Takaku, Hiroshi; Kamaike, Kazuo; Tsuchiya, Hiromichi (1984-01-01). "Oligonucleotide synthesis. Part 21. Synthesis of ribooligonucleotides using the 4-methoxybenzyl group as a new protecting group for the 2′-hydroxyl group". The Journal of Organic Chemistry. 49 (1): 51–56. doi:10.1021/jo00175a010. ISSN 0022-3263.
- ^ Trost, Barry M.; Waser, Jerome; Meyer, Arndt (2007-11-01). "Total Synthesis of (−)-Pseudolaric Acid B". Journal of the American Chemical Society. 129 (47): 14556–14557. doi:10.1021/ja076165q. ISSN 0002-7863. PMC 2535803. PMID 17985906.
- ^ Mukaiyama, Teruaki; Shiina, Isamu; Iwadare, Hayato; Saitoh, Masahiro; Nishimura, Toshihiro; Ohkawa, Naoto; Sakoh, Hiroki; Nishimura, Koji; Tani, Yu-ichirou (1999-01-04). "Asymmetric Total Synthesis of Taxol\R". Chemistry – A European Journal (jezik: engleski). 5 (1): 121–161. doi:10.1002/(SICI)1521-3765(19990104)5:13.0.CO;2-O. ISSN 1521-3765.
- ^ Hanessian, Stephen; Marcotte, Stéphane; Machaalani, Roger; Huang, Guobin (2003-11-01). "Total Synthesis and Structural Confirmation of Malayamycin A: A Novel Bicyclic C-Nucleoside from Streptomyces malaysiensis". Organic Letters. 5 (23): 4277–4280. doi:10.1021/ol030095k. ISSN 1523-7060.
- ^ Kuehne, Martin E.; Xu, Feng (1993-12-01). "Total synthesis of strychnan and aspidospermatan alkaloids. 3. The total synthesis of (±)-strychnine". The Journal of Organic Chemistry. 58 (26): 7490–7497. doi:10.1021/jo00078a030. ISSN 0022-3263.
- ^ Cain, Christian M.; Cousins, Richard P. C.; Coumbarides, Greg; Simpkins, Nigel S. (1990-01-01). "Asymmetric deprotonation of prochiral ketones using chiral lithium amide bases". Tetrahedron. 46 (2): 523–544. doi:10.1016/S0040-4020(01)85435-1.
- ^ Zhou, Hao; Liao, Xuebin; Cook, James M. (2004-01-01). "Regiospecific, Enantiospecific Total Synthesis of the 12-Alkoxy-Substituted Indole Alkaloids, (+)-12-Methoxy-Na-methylvellosimine, (+)-12-Methoxyaffinisine, and (−)-Fuchsiaefoline". Organic Letters. 6 (2): 249–252. doi:10.1021/ol0362212. ISSN 1523-7060.
Vanjski linkovi
| Commons ima datoteke na temu: Benzil grupa |