Razlika između verzija stranice "Hemijska formula"
| [pregledana izmjena] | [nepregledana izmjena] |
m Automatsko dodavanje sekcije "Također pogledajte" |
No edit summary |
||
| Red 1: | Red 1: | ||
==Pregled== |
|||
{{Nedostaju izvori}} |
|||
'''Hemijska formula''' je zapis sastava [[hemijski spoj|hemijskog spoja]] pomoću [[hemija|hemijskih]] [[simbol]]a. Hemijska formula može biti: |
'''Hemijska formula''' je zapis sastava [[hemijski spoj|hemijskog spoja]] pomoću [[hemija|hemijskih]] [[simbol]]a. Hemijska formula može biti: |
||
* '' |
* '''[[Empirijska formula]]''', koja navodi [[hemijski element|elemente]] spoja u njihovom međusobnom omjeru. Primjer: C<sub>n</sub>H<sub>2n</sub>; u spoju označava omjer [[vodonik]]a i [[ugljik]]a 1:2. Spojevi s takvim sastavom su obično veliki, npr. svi alkeni ili cikloalkani. |
||
{{Glavni|Empirijska formula}} |
{{Glavni|Empirijska formula}} |
||
* '' |
* '''[[Strukturna formula]]''', koja uz omjer pojedinog spoja navodi [[valencija (hemija)|valenciju]] i razpored [[atom]]a u [[molekula|molekuli]]. (CH<sub>3</sub>CH<sub>2</sub>CH<sub>2</sub>CH<sub>3</sub>) |
||
* |
*'''Molekulska formula''', koja navodi broj atoma elementa u pojedinom spoju. Primjer: [[butan (plin)|butan]] - C<sub>4</sub>H<sub>10</sub> |
||
==Definicija== |
|||
{{Infokutija |
|||
| title = Al<sub>2</sub>(SO<sub>4</sub>)<sub>3</sub> |
|||
| data2 = [[Aluminij-sulfat]] ima hemijsku formulu Al<sub>2</sub>(SO<sub>4</sub>)<sub>3</sub>. Oblik aluminij-sulfat heksadekahidrata je {{nowrap|Al<sub>2</sub>(SO<sub>4</sub>)<sub>3</sub>·16 [[pitka voda|H<sub>2</sub>O]]}}. |
|||
}} |
|||
{{Infokutija |
|||
| title = <chem>H-\overset{\displaystyle H \atop |}{\underset{| \atop \displaystyle H}{C}}-\overset{\displaystyle H \atop |}{\underset{| \atop \displaystyle H}{C}}-\overset{\displaystyle H \atop |}{\underset{| \atop \displaystyle H}{C}}-\overset{\displaystyle H \atop |}{\underset{| \atop \displaystyle H}{C}}-H</chem> |
|||
| data2 = [[Strukturna formula]] [[butan]]a. Primjeri drugih hemijskih formula za butan su C<sub>2</sub>H<sub>5</sub>, molekulska formula C<sub>4</sub>H<sub>10</sub> i kondenzirana (ili semistrukturna) formula CH<sub>3</sub>CH<sub>2</sub>CH<sub>2</sub>CH<sub>3</sub>.}} |
|||
'''Hemijska formula''' je jedan od načina predstavljanja informacija o hemijskim proporcijama [[atom]]a koji čine određeni [[hemijski spoj]] ili molekulu, koristeći simbole [[hemijski element|hemijskih elemenata]], brojeve, a ponekad i druge simbole, poput umetanja, crtica, zagrada, zareza i znakova ''plus'' (+) i ''minus'' (–). Oni su ograničeni na jednu tipografsku liniju simbola, koja može uključivati indekse i natpise. Hemijska formula nije [[hemijska nomenklatura | hemijski naziv]] i ne sadrži riječi. Iako hemijska formula može podrazumijevati određene jednostavne hemijske strukture, to nije isto što i puna hemijska [[strukturna formula]]. Hemijske formule mogu u potpunosti odrediti strukturu samo najjednostavnijih [[molekula]] i [[hemijska supstanca|hemijskih supstanci]], i uglavnom su ograničenije snage hemijskih imena i strukturnih formula. |
|||
Najjednostavnije vrste hemijskih formula nazivaju se ''[[empirijske formule]]'', koje koriste slova i brojeve koji označavaju numeričke ''proporcije'' atoma svake vrste. '''Molekulske formule''' označavaju jednostavne brojeve svake vrste atoma u molekulu, bez podataka o strukturi. Naprimjer, empirijska formula za [[glukoza|glukozu]] je CH<sub>2</sub>O(dvostruko više atoma vodika od ugljika i kisika), dok je njegova molekulska formula. |
|||
Tako npr. formula H<sub>2</sub>O označava molekulu vode, koja se sastoji od dvaju atoma vodika (H) i jednog atoma kisika (O). |
|||
==Tipovi hemijskih formula== |
|||
Hemijske formule razlikuju se prema informacijama koje pružaju. |
|||
*'''Formula elementarne tvari''' predočuje molekulu odnosno skup istovrsnih atoma koji se nalaze u molekuli [[elementarne tvari]] (H<sub>2</sub>, P<sub>4</sub>, S<sub>8</sub>) |
|||
*'''Empirijska formula''' pokazuje samo relativne omjere broja pojedinih atoma u jedinki, a određuje se na temelju masenih udjela pojedinih elemenata u spoju dobivenih elementarnom analizom. |
|||
*'''Molekulska formula''' pokazuje tačan broj atoma u spoju (molekuli), a određuje se iz empirijske formule i poznate molekulske mase. |
|||
*'''Strukturna formula''' prikazuje način povezivanja atoma u molekuli, a određuje se nakon identifikacije [[Funkcionalna grupaa|funkcionalnih skupina]] molekule (alkoholna, aldehidna, kiselinska, aminska i dr.), najčešće spektroskopskim tehnikama. |
|||
*'''Sažeta strukturna formula''' je strukturna formula napisana jednostavnije, često u jednom redu, prikazane su atomske grupe i atomi ali način njihovog povezivanja nije posve jasan. |
|||
*'''Stereohemijska formula''' prikazuje prostornu orijentaciju atoma u molekuli različitim tipovima projekcija koje uključuju mnoge dodatne konvencije. Prostorni raspored atoma izravno se određuje difrakcijskim metodima strukturne analize. |
|||
{| class="wikitable" |
|||
!Spoj||Empirijska formula||Molekulska formula||Sažeta strukturna formula||Strukturna formula||Projekcijska formula |
|||
|- |
|||
|[[Hlorovodik]]||HCl||HCl||HCl||align="center"|HCl|| |
|||
|- |
|||
|[[Acetatna kiselina]]||CH<sub>2</sub>O||C<sub>2</sub>H<sub>4</sub>O<sub>2</sub>||CH<sub>3</sub>-CO-OH||align="center"|[[slika:Acetic acid 2.svg|100px]]|| |
|||
|- |
|||
|[[Etin]]||CH||C<sub>2</sub>H<sub>2</sub>||HCΞCH||align="center"|H-CΞC-H|| |
|||
|- |
|||
|[[Benzen]]||CH||C<sub>6</sub>H<sub>6</sub>||[[Datoteka:Benzene circle.png]]||align="center"|[[slika:Benz1.png|100px]]|| |
|||
|- |
|||
|[[Etanol]]||C<sub>2</sub>H<sub>6</sub>O||C<sub>2</sub>H<sub>6</sub>O||CH<sub>3</sub>-CH<sub>2</sub>-OH||align="center"|[[slika:Ethanol-2D-flat.png|100px]]|| |
|||
|- |
|||
|[[Metoksimetan]]||C<sub>2</sub>H<sub>6</sub>O||C<sub>2</sub>H<sub>6</sub>O||CH<sub>3</sub>-O-CH<sub>3</sub>||align="center"|[[slika:Dimethylether.PNG|100px]]|| |
|||
|- |
|||
|[[Mliiječna kiselina]]||CH<sub>2</sub>O||C<sub>3</sub>H<sub>6</sub>O<sub>3</sub>||CH<sub>3</sub>-CH(OH)-COOH||[[slika:Milchsäure Enantiomerenpaar.svg]]|| |
|||
|- |
|||
|[[Glukoza]]||CH<sub>2</sub>O||C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>||HOCH<sub>2</sub>-[CH(OH)]<sub>4</sub>-CHO||[[slika:D-glucose chain (Fischer).svg]]Fischerova||[[slika:Beta-D-Glucopyranose.svg]] |
|||
|} |
|||
==Formulska jedinica== |
|||
'''Formulsku jedinica''' je najmanji omjer broja [[anion]]a i [[kation]]a u ionskom spoju koji prikazujemo formulom spoja. |
|||
Ionska tvar je ogroman skup aniona i kationa koji su povezani [[Ionska veza|ionskom vezom]] (elektrostatskom). U ionskoj tvari naizmjenično su raspoređeni anioni i kationi, odnosno svaki anion je okružen određenim brojem kationa i obrnuto. Ne postoji molekula ionskog spoja već je cijeli spoj jedna „velika molekula”. Zato formula ionskog spoja ima samo najmanji omjer broja aniona i kationa u spoju, odnosno prikazuje formulsku jedinku. Formula CaCl<sub>2</sub> govori da se u [[kalcij-hlorid]]u kationi (Ca<sup>2+</sup>) i anioni (Cl<sup>–</sup>) nalaze u omjeru 1:2 te je CaCl<sub>2</sub> formulska jedinka kalcij-hlorida. |
|||
U najširem smislu svaka formula predstavlja formulsku jedinku. |
|||
==Formule hidratnih soli== |
|||
[[Kristali]] hidratnih soli imaju u sastavu vezanu [[Kristalna voda|kristalnu vodu]]. Formula spoja se piše, naprimjer: CuSO<sub>4</sub>∙5H<sub>2</sub>O. Tačka u formuli ne predstavlja znak množenja već je znak sabiranja (plus). Voda je uklopljena u kristalnu strukturu spoja. Napisana formula je sažeti oblik pisanja. Zapravo formulu bi pravilnije trebalo pisati kao: [Cu(H<sub>2</sub>O)<sub>4</sub>]SO<sub>4</sub>∙H<sub>2</sub>O. Četiri molekule vode se koordiniraju s ionom bakra, dok je peta molekula vode povezana sa sulfatnim ionom. Također, MgSO<sub>4</sub>∙7H<sub>2</sub>O zapravo je [Mg(H<sub>2</sub>O)<sub>6</sub>]SO<sub>4</sub>∙H<sub>2</sub>O. Uglaste zagrade u pisanju koriste se za kreiranje formula kompleksnih spojeva. |
|||
==Formule kompleksnih spojeva== |
|||
Formule [[Kompleksni spojevi|kompleksnih spojeva]], sažeto se pišu kao u prethodnim primjerima, ali najprizornije je formulu prikazati „trodimenzijski”. |
|||
<gallery> |
|||
Tetraminkupfersulfathydrat.png|Bakar-tetraaminosulfat hidtat [Cu(NH<sub>3</sub>)<sub>4</sub>]SO<sub>4</sub>·H<sub>2</sub>O |
|||
(RhA5Cl)Cl2.png|Rodijev pentaminotriklorid [Rh(NH<sub>3</sub>)<sub>5</sub>Cl]Cl<sub>2</sub> |
|||
M(edds).png|Kompleks kationa [[metal]]a i [[EDTA]]. |
|||
</gallery> |
|||
==Reference== |
|||
{{reflist}} |
|||
[[Kategorija:Hemija]] |
|||
[[Kategorija:Opća hemija]] |
|||
[[Kategorija:Hemijska terminologija]] |
|||
'''Hemijska formula''' je jedan od načina predstavljanja informacija o hemijskim proporcijama [[atom]]a koji čine određeni [[hemijski spoj]] ili molekulu, koristeći simbole [[hemijski element|hemijskih elemenata]], brojeve, a ponekad i druge simbole, poput umetanja, crtica, zagrada, zareza i znakova ''plus'' (+) i ''minus'' (–). Oni su ograničeni na jednu tipografsku liniju simbola, koja može uključivati indekse i natpise. Hemijska formula nije [[hemijska nomenklatura | hemijski naziv]] i ne sadrži riječi. Iako hemijska formula može podrazumijevati određene jednostavne hemijske strukture, to nije isto što i puna hemijska [[strukturna formula]]. Hemijske formule mogu u potpunosti odrediti strukturu samo najjednostavnijih [[molekula]] i [[hemijska supstanca|hemijskih supstanci]], i uglavnom su ograničenije snage hemijskih imena i strukturnih formula. |
|||
Najjednostavnije vrste hemijskih formula nazivaju se ''[[empirijske formule]]'', koje koriste slova i brojeve koji označavaju numeričke ''proporcije'' atoma svake vrste. '''Molekulske formule''' označavaju jednostavne brojeve svake vrste atoma u molekulu, bez podataka o strukturi. Naprimjer, empirijska formula za [[glukoza|glukozu]] je CH<sub>2</sub>O(dvostruko više atoma vodika od ugljika i kisika), dok je njegova molekulska formula. |
|||
CH<sub>3</sub>-CH<sub>2</sub>-OH or CH<sub>3</sub>CH<sub>2</sub>OH. However, even a condensed chemical formula is necessarily limited in its ability to show complex bonding relationships between atoms, especially atoms that have bonds to four or more different [[substituent]]s. |
|||
Since a chemical formula must be expressed as a single line of chemical element symbols, it often cannot be as informative as a true structural formula, which is a graphical representation of the spatial relationship between atoms in chemical compounds (see for example the figure for butane structural and chemical formulae, at right). For reasons of structural complexity, a single condensed chemical formula (or semi-structural formula) may correspond to different molecules, known as [[isomer]]s. For example glucose shares its [[molecular formula]] [[C6H12O6|C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>]] with a number of other [[sugar]]s, including [[fructose]], [[galactose]] and [[mannose]]. Linear equivalent chemical ''names'' exist that can and do specify uniquely any complex structural formula (see [[chemical nomenclature]]), but such names must use many terms (words), rather than the simple element symbols, numbers, and simple typographical symbols that define a chemical formula. |
|||
Tako npr. formula H<sub>2</sub>O označuje molekulu vode, koja se sastoji od dvaju atoma vodika (simbol H) i jednog atoma kisika (simbol O). |
|||
==Tipovi hemijskih formula== |
|||
Hemijske formule razlikuju se prema informacijama koje pružaju. |
|||
*''Formula elementarne tvari'' predočuje molekulu odnosno skup istovrsnih atoma koji se nalaze u molekuli [[elementarne tvari]] (H<sub>2</sub>, P<sub>4</sub>, S<sub>8</sub>) |
|||
*''Empirijska formula'' pokazuje samo relativne omjere broja pojedinih atoma u jedinki, a određuje se na temelju masenih udjela pojedinih elemenata u spoju dobivenih elementarnom analizom. |
|||
*''Molekulska formula'' pokazuje tačan broj atoma u spoju (molekuli), a određuje se iz empirijske formule i poznate molekulske mase. |
|||
*''Strukturna formula'' prikazuje način povezivanja atoma u molekuli, a određuje se nakon identifikacije [[Funkcionalna grupaa|funkcionalnih skupina]] molekule (alkoholna, aldehidna, kiselinska, aminska i dr.), najčešće spektroskopskim tehnikama. |
|||
*''Sažeta strukturna formula'' je strukturna formula napisana jednostavnije, često u jednom redu, prikazane su atomske grupe i atomi ali način njihovog povezivanja nije posve jasan. |
|||
*''Stereohemijska formula'' prikazuje prostornu orijentaciju atoma u molekuli različitim tipovima projekcija koje uključuju mnoge dodatne konvencije. Prostorni raspored atoma izravno se određuje difrakcijskim metodima strukturne analize. |
|||
{| class="wikitable" |
|||
!Spoj||Empirijska formula||Molekulska formula||Sažeta strukturna formula||Strukturna formula||Projekcijska formula |
|||
|- |
|||
|[[Hlorovodik]]||HCl||HCl||HCl||align="center"|HCl|| |
|||
|- |
|||
|[[Acetatna kiselina]]||CH<sub>2</sub>O||C<sub>2</sub>H<sub>4</sub>O<sub>2</sub>||CH<sub>3</sub>-CO-OH||align="center"|[[slika:Acetic acid 2.svg|100px]]|| |
|||
|- |
|||
|[[Etin]]||CH||C<sub>2</sub>H<sub>2</sub>||HCΞCH||align="center"|H-CΞC-H|| |
|||
|- |
|||
|[[Benzen]]||CH||C<sub>6</sub>H<sub>6</sub>||[[Datoteka:Benzene circle.png]]||align="center"|[[slika:Benz1.png|100px]]|| |
|||
|- |
|||
|[[Etanol]]||C<sub>2</sub>H<sub>6</sub>O||C<sub>2</sub>H<sub>6</sub>O||CH<sub>3</sub>-CH<sub>2</sub>-OH||align="center"|[[slika:Ethanol-2D-flat.png|100px]]|| |
|||
|- |
|||
|[[Metoksimetan]]||C<sub>2</sub>H<sub>6</sub>O||C<sub>2</sub>H<sub>6</sub>O||CH<sub>3</sub>-O-CH<sub>3</sub>||align="center"|[[slika:Dimethylether.PNG|100px]]|| |
|||
|- |
|||
|[[Mliiječna kiselina]]||CH<sub>2</sub>O||C<sub>3</sub>H<sub>6</sub>O<sub>3</sub>||CH<sub>3</sub>-CH(OH)-COOH||[[slika:Milchsäure Enantiomerenpaar.svg]]|| |
|||
|- |
|||
|[[Glukoza]]||CH<sub>2</sub>O||C<sub>6</sub>H<sub>12</sub>O<sub>6</sub>||HOCH<sub>2</sub>-[CH(OH)]<sub>4</sub>-CHO||[[slika:D-glucose chain (Fischer).svg]]Fischerova||[[slika:Beta-D-Glucopyranose.svg]] |
|||
|} |
|||
==Formulska jedinica== |
|||
'''Formulsku jedinica''' je najmanji omjer broja [[anion]]a i [[kation]]a u ionskom spoju koji prikazujemo formulom spoja. |
|||
Ionska tvar je ogroman skup aniona i kationa koji su povezani [[Ionska veza|ionskom vezom]] (elektrostatskom). U ionskoj tvari naizmjenično su raspoređeni anioni i kationi, odnosno svaki anion je okružen određenim brojem kationa i obrnuto. Ne postoji molekula ionskog spoja već je cijeli spoj jedna „velika molekula”. Zato formula ionskog spoja ima samo najmanji omjer broja aniona i kationa u spoju, odnosno prikazuje formulsku jedinku. Formula CaCl<sub>2</sub> govori da se u [[kalcij-hlorid]]u kationi (Ca<sup>2+</sup>) i anioni (Cl<sup>–</sup>) nalaze u omjeru 1:2 te je CaCl<sub>2</sub> formulska jedinka kalcij-hlorida. |
|||
U najširem smislu svaka formula predstavlja formulsku jedinku. |
|||
==Formule hidratnih soli== |
|||
[[Kristali]] hidratnih soli imaju u sastavu vezanu [[Kristalna voda|kristalnu vodu]]. Formula spoja se piše, naprimjer: CuSO<sub>4</sub>∙5H<sub>2</sub>O. Tačka u formuli ne predstavlja znak množenja već je znak sabiranja (plus). Voda je uklopljena u kristalnu strukturu spoja. Napisana formula je sažeti oblik pisanja. Zapravo formulu bi pravilnije trebalo pisati kao: [Cu(H<sub>2</sub>O)<sub>4</sub>]SO<sub>4</sub>∙H<sub>2</sub>O. Četiri molekule vode se koordiniraju s ionom bakra, dok je peta molekula vode povezana sa sulfatnim ionom. Također, MgSO<sub>4</sub>∙7H<sub>2</sub>O zapravo je [Mg(H<sub>2</sub>O)<sub>6</sub>]SO<sub>4</sub>∙H<sub>2</sub>O. Uglaste zagrade u pisanju koriste se za kreiranje formula kompleksnih spojeva. |
|||
==Formule kompleksnih spojeva== |
|||
Formule [[Kompleksni spojevi|kompleksnih spojeva]], sažeto se pišu kao u prethodnim primjerima, ali najprizornije je formulu prikazati „trodimenzijski”. |
|||
<gallery> |
|||
Tetraminkupfersulfathydrat.png|Bakar-tetraaminosulfat hidtat [Cu(NH<sub>3</sub>)<sub>4</sub>]SO<sub>4</sub>·H<sub>2</sub>O |
|||
(RhA5Cl)Cl2.png|Rodijev pentaminotriklorid [Rh(NH<sub>3</sub>)<sub>5</sub>Cl]Cl<sub>2</sub> |
|||
M(edds).png|Kompleks kationa [[metal]]a i [[EDTA]]. |
|||
</gallery> |
|||
== Također pogledajte == |
== Također pogledajte == |
||
* [[Periodni sistem elemenata]] |
* [[Periodni sistem elemenata]] |
||
==Reference== |
|||
{{Stub-hem}} |
|||
{{reflist}} |
|||
[[Kategorija:Hemija]] |
|||
[[Kategorija:Opća hemija]] |
|||
[[Kategorija:Hemijska terminologija]] |
|||
[[Kategorija:Hemijska nomenklatura]] |
[[Kategorija:Hemijska nomenklatura]] |
||
Verzija na dan 10 februar 2021 u 01:35
Pregled
Hemijska formula je zapis sastava hemijskog spoja pomoću hemijskih simbola. Hemijska formula može biti:
- Empirijska formula, koja navodi elemente spoja u njihovom međusobnom omjeru. Primjer: CnH2n; u spoju označava omjer vodonika i ugljika 1:2. Spojevi s takvim sastavom su obično veliki, npr. svi alkeni ili cikloalkani.
- Strukturna formula, koja uz omjer pojedinog spoja navodi valenciju i razpored atoma u molekuli. (CH3CH2CH2CH3)
- Molekulska formula, koja navodi broj atoma elementa u pojedinom spoju. Primjer: butan - C4H10
Definicija
| Aluminij-sulfat ima hemijsku formulu Al2(SO4)3. Oblik aluminij-sulfat heksadekahidrata je Al2(SO4)3·16 H2O. |
| Strukturna formula butana. Primjeri drugih hemijskih formula za butan su C2H5, molekulska formula C4H10 i kondenzirana (ili semistrukturna) formula CH3CH2CH2CH3. |
Hemijska formula je jedan od načina predstavljanja informacija o hemijskim proporcijama atoma koji čine određeni hemijski spoj ili molekulu, koristeći simbole hemijskih elemenata, brojeve, a ponekad i druge simbole, poput umetanja, crtica, zagrada, zareza i znakova plus (+) i minus (–). Oni su ograničeni na jednu tipografsku liniju simbola, koja može uključivati indekse i natpise. Hemijska formula nije hemijski naziv i ne sadrži riječi. Iako hemijska formula može podrazumijevati određene jednostavne hemijske strukture, to nije isto što i puna hemijska strukturna formula. Hemijske formule mogu u potpunosti odrediti strukturu samo najjednostavnijih molekula i hemijskih supstanci, i uglavnom su ograničenije snage hemijskih imena i strukturnih formula.
Najjednostavnije vrste hemijskih formula nazivaju se empirijske formule, koje koriste slova i brojeve koji označavaju numeričke proporcije atoma svake vrste. Molekulske formule označavaju jednostavne brojeve svake vrste atoma u molekulu, bez podataka o strukturi. Naprimjer, empirijska formula za glukozu je CH2O(dvostruko više atoma vodika od ugljika i kisika), dok je njegova molekulska formula.
Tako npr. formula H2O označava molekulu vode, koja se sastoji od dvaju atoma vodika (H) i jednog atoma kisika (O).
Tipovi hemijskih formula
Hemijske formule razlikuju se prema informacijama koje pružaju.
- Formula elementarne tvari predočuje molekulu odnosno skup istovrsnih atoma koji se nalaze u molekuli elementarne tvari (H2, P4, S8)
- Empirijska formula pokazuje samo relativne omjere broja pojedinih atoma u jedinki, a određuje se na temelju masenih udjela pojedinih elemenata u spoju dobivenih elementarnom analizom.
- Molekulska formula pokazuje tačan broj atoma u spoju (molekuli), a određuje se iz empirijske formule i poznate molekulske mase.
- Strukturna formula prikazuje način povezivanja atoma u molekuli, a određuje se nakon identifikacije funkcionalnih skupina molekule (alkoholna, aldehidna, kiselinska, aminska i dr.), najčešće spektroskopskim tehnikama.
- Sažeta strukturna formula je strukturna formula napisana jednostavnije, često u jednom redu, prikazane su atomske grupe i atomi ali način njihovog povezivanja nije posve jasan.
- Stereohemijska formula prikazuje prostornu orijentaciju atoma u molekuli različitim tipovima projekcija koje uključuju mnoge dodatne konvencije. Prostorni raspored atoma izravno se određuje difrakcijskim metodima strukturne analize.
| Spoj | Empirijska formula | Molekulska formula | Sažeta strukturna formula | Strukturna formula | Projekcijska formula |
|---|---|---|---|---|---|
| Hlorovodik | HCl | HCl | HCl | HCl | |
| Acetatna kiselina | CH2O | C2H4O2 | CH3-CO-OH |  |
|
| Etin | CH | C2H2 | HCΞCH | H-CΞC-H | |
| Benzen | CH | C6H6 | 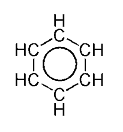 |
 |
|
| Etanol | C2H6O | C2H6O | CH3-CH2-OH |  |
|
| Metoksimetan | C2H6O | C2H6O | CH3-O-CH3 |  |
|
| Mliiječna kiselina | CH2O | C3H6O3 | CH3-CH(OH)-COOH | 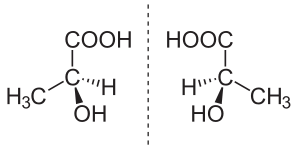 |
|
| Glukoza | CH2O | C6H12O6 | HOCH2-[CH(OH)]4-CHO | 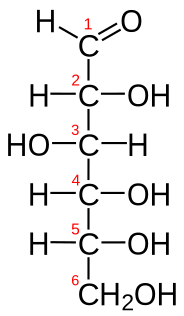 Fischerova Fischerova |

|
Formulska jedinica
Formulsku jedinica je najmanji omjer broja aniona i kationa u ionskom spoju koji prikazujemo formulom spoja. Ionska tvar je ogroman skup aniona i kationa koji su povezani ionskom vezom (elektrostatskom). U ionskoj tvari naizmjenično su raspoređeni anioni i kationi, odnosno svaki anion je okružen određenim brojem kationa i obrnuto. Ne postoji molekula ionskog spoja već je cijeli spoj jedna „velika molekula”. Zato formula ionskog spoja ima samo najmanji omjer broja aniona i kationa u spoju, odnosno prikazuje formulsku jedinku. Formula CaCl2 govori da se u kalcij-hloridu kationi (Ca2+) i anioni (Cl–) nalaze u omjeru 1:2 te je CaCl2 formulska jedinka kalcij-hlorida.
U najširem smislu svaka formula predstavlja formulsku jedinku.
Formule hidratnih soli
Kristali hidratnih soli imaju u sastavu vezanu kristalnu vodu. Formula spoja se piše, naprimjer: CuSO4∙5H2O. Tačka u formuli ne predstavlja znak množenja već je znak sabiranja (plus). Voda je uklopljena u kristalnu strukturu spoja. Napisana formula je sažeti oblik pisanja. Zapravo formulu bi pravilnije trebalo pisati kao: [Cu(H2O)4]SO4∙H2O. Četiri molekule vode se koordiniraju s ionom bakra, dok je peta molekula vode povezana sa sulfatnim ionom. Također, MgSO4∙7H2O zapravo je [Mg(H2O)6]SO4∙H2O. Uglaste zagrade u pisanju koriste se za kreiranje formula kompleksnih spojeva.
Formule kompleksnih spojeva
Formule kompleksnih spojeva, sažeto se pišu kao u prethodnim primjerima, ali najprizornije je formulu prikazati „trodimenzijski”.
-
Bakar-tetraaminosulfat hidtat [Cu(NH3)4]SO4·H2O
-
Rodijev pentaminotriklorid [Rh(NH3)5Cl]Cl2
Reference
Hemijska formula je jedan od načina predstavljanja informacija o hemijskim proporcijama atoma koji čine određeni hemijski spoj ili molekulu, koristeći simbole hemijskih elemenata, brojeve, a ponekad i druge simbole, poput umetanja, crtica, zagrada, zareza i znakova plus (+) i minus (–). Oni su ograničeni na jednu tipografsku liniju simbola, koja može uključivati indekse i natpise. Hemijska formula nije hemijski naziv i ne sadrži riječi. Iako hemijska formula može podrazumijevati određene jednostavne hemijske strukture, to nije isto što i puna hemijska strukturna formula. Hemijske formule mogu u potpunosti odrediti strukturu samo najjednostavnijih molekula i hemijskih supstanci, i uglavnom su ograničenije snage hemijskih imena i strukturnih formula.
Najjednostavnije vrste hemijskih formula nazivaju se empirijske formule, koje koriste slova i brojeve koji označavaju numeričke proporcije atoma svake vrste. Molekulske formule označavaju jednostavne brojeve svake vrste atoma u molekulu, bez podataka o strukturi. Naprimjer, empirijska formula za glukozu je CH2O(dvostruko više atoma vodika od ugljika i kisika), dok je njegova molekulska formula.
CH3-CH2-OH or CH3CH2OH. However, even a condensed chemical formula is necessarily limited in its ability to show complex bonding relationships between atoms, especially atoms that have bonds to four or more different substituents.
Since a chemical formula must be expressed as a single line of chemical element symbols, it often cannot be as informative as a true structural formula, which is a graphical representation of the spatial relationship between atoms in chemical compounds (see for example the figure for butane structural and chemical formulae, at right). For reasons of structural complexity, a single condensed chemical formula (or semi-structural formula) may correspond to different molecules, known as isomers. For example glucose shares its molecular formula C6H12O6 with a number of other sugars, including fructose, galactose and mannose. Linear equivalent chemical names exist that can and do specify uniquely any complex structural formula (see chemical nomenclature), but such names must use many terms (words), rather than the simple element symbols, numbers, and simple typographical symbols that define a chemical formula. Tako npr. formula H2O označuje molekulu vode, koja se sastoji od dvaju atoma vodika (simbol H) i jednog atoma kisika (simbol O).
Tipovi hemijskih formula
Hemijske formule razlikuju se prema informacijama koje pružaju.
- Formula elementarne tvari predočuje molekulu odnosno skup istovrsnih atoma koji se nalaze u molekuli elementarne tvari (H2, P4, S8)
- Empirijska formula pokazuje samo relativne omjere broja pojedinih atoma u jedinki, a određuje se na temelju masenih udjela pojedinih elemenata u spoju dobivenih elementarnom analizom.
- Molekulska formula pokazuje tačan broj atoma u spoju (molekuli), a određuje se iz empirijske formule i poznate molekulske mase.
- Strukturna formula prikazuje način povezivanja atoma u molekuli, a određuje se nakon identifikacije funkcionalnih skupina molekule (alkoholna, aldehidna, kiselinska, aminska i dr.), najčešće spektroskopskim tehnikama.
- Sažeta strukturna formula je strukturna formula napisana jednostavnije, često u jednom redu, prikazane su atomske grupe i atomi ali način njihovog povezivanja nije posve jasan.
- Stereohemijska formula prikazuje prostornu orijentaciju atoma u molekuli različitim tipovima projekcija koje uključuju mnoge dodatne konvencije. Prostorni raspored atoma izravno se određuje difrakcijskim metodima strukturne analize.
| Spoj | Empirijska formula | Molekulska formula | Sažeta strukturna formula | Strukturna formula | Projekcijska formula |
|---|---|---|---|---|---|
| Hlorovodik | HCl | HCl | HCl | HCl | |
| Acetatna kiselina | CH2O | C2H4O2 | CH3-CO-OH |  |
|
| Etin | CH | C2H2 | HCΞCH | H-CΞC-H | |
| Benzen | CH | C6H6 |  |
 |
|
| Etanol | C2H6O | C2H6O | CH3-CH2-OH |  |
|
| Metoksimetan | C2H6O | C2H6O | CH3-O-CH3 |  |
|
| Mliiječna kiselina | CH2O | C3H6O3 | CH3-CH(OH)-COOH | 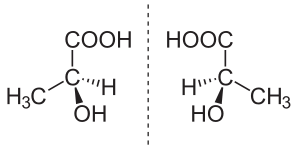 |
|
| Glukoza | CH2O | C6H12O6 | HOCH2-[CH(OH)]4-CHO |  Fischerova Fischerova |

|
Formulska jedinica
Formulsku jedinica je najmanji omjer broja aniona i kationa u ionskom spoju koji prikazujemo formulom spoja. Ionska tvar je ogroman skup aniona i kationa koji su povezani ionskom vezom (elektrostatskom). U ionskoj tvari naizmjenično su raspoređeni anioni i kationi, odnosno svaki anion je okružen određenim brojem kationa i obrnuto. Ne postoji molekula ionskog spoja već je cijeli spoj jedna „velika molekula”. Zato formula ionskog spoja ima samo najmanji omjer broja aniona i kationa u spoju, odnosno prikazuje formulsku jedinku. Formula CaCl2 govori da se u kalcij-hloridu kationi (Ca2+) i anioni (Cl–) nalaze u omjeru 1:2 te je CaCl2 formulska jedinka kalcij-hlorida.
U najširem smislu svaka formula predstavlja formulsku jedinku.
Formule hidratnih soli
Kristali hidratnih soli imaju u sastavu vezanu kristalnu vodu. Formula spoja se piše, naprimjer: CuSO4∙5H2O. Tačka u formuli ne predstavlja znak množenja već je znak sabiranja (plus). Voda je uklopljena u kristalnu strukturu spoja. Napisana formula je sažeti oblik pisanja. Zapravo formulu bi pravilnije trebalo pisati kao: [Cu(H2O)4]SO4∙H2O. Četiri molekule vode se koordiniraju s ionom bakra, dok je peta molekula vode povezana sa sulfatnim ionom. Također, MgSO4∙7H2O zapravo je [Mg(H2O)6]SO4∙H2O. Uglaste zagrade u pisanju koriste se za kreiranje formula kompleksnih spojeva.
Formule kompleksnih spojeva
Formule kompleksnih spojeva, sažeto se pišu kao u prethodnim primjerima, ali najprizornije je formulu prikazati „trodimenzijski”.
-
Bakar-tetraaminosulfat hidtat [Cu(NH3)4]SO4·H2O
-
Rodijev pentaminotriklorid [Rh(NH3)5Cl]Cl2


![Bakar-tetraaminosulfat hidtat [Cu(NH3)4]SO4·H2O](http://upload.wikimedia.org/wikipedia/commons/thumb/2/2f/Tetraminkupfersulfathydrat.png/120px-Tetraminkupfersulfathydrat.png)
![Rodijev pentaminotriklorid [Rh(NH3)5Cl]Cl2](http://upload.wikimedia.org/wikipedia/commons/thumb/8/8d/%28RhA5Cl%29Cl2.png/120px-%28RhA5Cl%29Cl2.png)
