Racemizacija
Racemizacija – u hemiji – odnosi se na konverziju enantiomerne čiste smjese (u kojoj je prisutan samo jedan enantomer) – mješavinu u kojoj se javlja više od jednog enantiomera. Enantiomer je poznat i kao optički izomer stereoizomernog para molekula koje nemaju svojstvo međusobne superpozicije, kao slike u ogledalu. Ako su rezultati racemizacije u smjesi u kojoj su prisutni D i L rotirani enantiomeri u jednakim količinama, rezultirajući uzorak je opisan kao racem, racemska mješavina ili racemat.[1][2]
Stereohemija[uredi | uredi izvor]
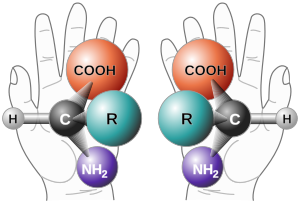
Hiralne molekule imaju va oblika (na svakoj tački asimetrije), koji se razlikuju u optičkim karakteristikama: lijevorotirajući kao (–)-forma) rotira ravan polarizacije snopa svjetlosti na lijevu stranu, dok desnorotirajući oblik, dok će (+)-forma rotirati ravan polarizacije zrake svetlosti u desno.
Za dva oblika, koji su ne prepokrivaju kada se rotiraju u 3-dimenzionalnom prostoru, kaže se da su enantiomeri . Ova oznaka se ne treba miješati sa D i L imenovanja molekula koji se odnosi na sličnosti u strukturi u D-gliceraldehidu i L-gliceraldehidu. Također, R(+) i S (–), odnose se na hemijske strukture molekula na osnovu Kan-Ingold-Prelogovim pravilima prioriteta imenovanja, a ne rotaciju svjetlosti.[3] [4]
Racemizacija se javlja kada se jedan čisti oblik enantiomera pretvara u jednak udio oba enantiomera, formirajući racemat. Kada postoje i jednak broj dekstrorotatirajućih i lijevorotirajućih molekula, neto optička rotacija racemata je nula. Enantiomere treba razlikovati od diastereoizomera koji su vrsta stereoizomera sa različiteim molekulskim strukturama oko stereocentara i ne odnose se kao odrazi slike u ogledalu .
Fizičke osobenosti[uredi | uredi izvor]
Racemati mogu imati različite fizičke osobine, od bilo kojeg čistog enantiomera zbog diferencijalnih intermolekulskih interakcija (vidjeti odjeljak ovog članka: Biološki značaj). Promjena čistog enantiomera u racemat može promijeniti gustoću, tačku topljenja, topivost, toplina topljenjs, indeks prelamanjai njegove razne spektre. Kristalizacija racemat može dovesti do pojave odvojenih (+) i (–) formi ili jednog racematnog spoja.[5][6]
Biološki značaj[uredi | uredi izvor]
Općenito, većina biohemijskih reakcija du stereoselektivne, tako da će samo jedan stereoizomer proizvesti ciljni produkt, dok drugi u tome jednostavno ne učestvuje ili izaziva postrani efekt. Treba napomenuti da L forma aminokiselina i D forme šećera (primarno glukoza) su obično biološki reaktivni oblici. Činjenica je da su mnoge biološke molekule hiralne čije reakcije sa specifičnim enantiomerima proizvode čiste stereoizomere.[7][8][9][10]
Osim toga, mnogi psihotropni lijekovi pokazuju različite aktivnosti ili efikasnosti između izomera, npr amfetamini se često se izdaju kao racemske soli, dok je aktivaniji dekstroamfetamin rezerviran za vatrostalne slučajeve ili više ozbiljne indikacije. Još jedan primjer je metadon, kod kojeg jedan izomer ima aktivnost kao agonist opioida i drugi kao NMDA antagonist.
Racemizacija farmaceutskih preparata može doći i in vivo. Talidomid kao ( R ) enantiomer je efikasan protiv jutarnje mučnine, dok je (S) enantiomer teratogen, uzrokujući urođene mahane kada se uzima u prvom tromjesečju trudnoće. Ako se primjenjuje samo jedan enantiomer se na ljudski subjekt, u krvnom serumu se kasnije mogu naći oba oblika. Lijek se stoga ne smatra sigurnim za korištenje za žene u fertilnoj dobi, a dok ima druge svrhe, njegova upotreba je pod strogom kontrolom. Talidomid se može koristiti za liječenje multiplog mieloma.[11][12]
Još jedan često upotrebljavani lijek – Ibuprofen, čiji je jedan od enantiomera samo anti-upalni, dok je drugi biološki inertan. Isto tako, (S) stereoizomer je mnogo reaktivniji nego (R) dok je aktivan enantiomer u Citalopramu (Celex), antidepresiv koji inhibira preuzimanja serotonina. Studije enantiomera u farmaceutskoj industriji se nazivaju hiralna organska sinteza. Također je primjetan i činjenica da su svi aminokiselinski ostataka u L obliku. Međutim, bakterije proizvode ostatake D-amino kiselina koje polimeriziraju u kratke polipeptide koji se mogu naći na njihovim ćelijskim zidovima. Ovi polipeptidi su manje razgradivi peptidazom i sintetiziraju bakterijske enzime umjesto prevođenja iRNK, koji bi normalno proizvodili L-aminokiseline.
Formiranje racemske mješavine[uredi | uredi izvor]
Racemizacija se može postići jednostavnim miješanjem jednake količine dva čista enantiomera, a također se može javiti u hemijskoj interkonverziji. Naprimjer, kada se rstvara (R)-3-fenil-2-butanon u vodenom etanolu koji sadrži NaOH ili HCl, formira se racemat. Racemizacija nastaje putem međuprodukta enolnog oblika, u kojem bivši stereocenter postaje planarni i stoga ahiralan.[13] Dolazna grupa može prići s obje strane površine, tako da je jednaka vjerovatnoća reverzne protonacije na hiralni keton i nastanka bilo R ili S forme, što rezultira stvaranjem racemata.
Racemizacija se može javiti u jednom od slijedećih procesa:
- Zamjenske reakcije koje nastaviljaju u slobodnim karbokationskim međuproduktima kao što su reakcije jednomolekulskih supstitucija, koje dovode do ne-stereospecifičnih dodavanja supstituenata što rezultira racemizacijama.
- Iako se reakcija jednomolekulske eliminacije nastavlja preko karbokations, oni ne rezultiraju u hiralni centar. Umjesto da se dovode u set geometrijske izomere u trans/cis (E/Z), proizvode se ovi oblici, a ne racemati.
- U unimolekulskim alifatskim reakcijama elektrofilne zamjene, ako je karbanion planaran ili ako ne može održavati piramidnu strukturu, onda bi trebalo da dođe do racemizacije, iako ne uvijek.
- Ako se reakcija zamjena slobodnih radikala, odvija na hiralnom ugljiku, onda se gotovu uvijek dobije acemizacija. Stopa racemizacije (L-forme mješavine L-forme i D-forme) se koristi kao način analize biološkikih uzoraka tkiva sa sporim stopama prometa, forenzičkih uzoraka i fosila u geološkim depozitima. Ova tehnika je poznata kao aminokiselinsko datiranje.[14]
Otkriće optčke aktivnosti[uredi | uredi izvor]
Louis Pasteur je 1843. Otkrio optičku aktivnost paratartarata ili racemata – soli vinske kisline. Mogao je razdvojiti enantiomerne kristale koji su rotirali polariziranu svjetlost u suprostom smjeru.
Također pogledajte[uredi | uredi izvor]
Referencee[uredi | uredi izvor]
- ^ Streitwieser A., Clayton H. Heathcock C. H. (1985): Introduction to organic chemistry, 6th Ed. Maxwell MacMillan, ISBN 0029467209 .
- ^ Nelson D. L., Cox M. M. (2013): Lehninger principles of biochemistry. W.H. Freeman, New York, ISBN 1429234148.
- ^ Voet D., Voet J. (1995): Biochemistry, 2nd Ed. Wiley, http://www.wiley.com/college/math/chem/cg/sales/voet.html.
- ^ Bugg T. (1997): An introduction to enzyme and coenzyme chemistry. Blackwell Science, Oxford, ISBN 0-86542-793-3.
- ^ Lindhorst T. (2007): Essentials of carbohydrate chemistry and biochemistry. Wiley-VCH, 3527315284}}
- ^ Robyt F. (1997): Essentials of carbohydrate chemistry. Springer, ISBN 0387949518.
- ^ Laidler K. J. (1978): Physical chemistry with biological applications. Benjamin/Cummings, Menlo Park, ISBN 0-8053-5680-0.
- ^ Bajrović K, Jevrić-Čaušević A., Hadžiselimović R., Ed. (2005): Uvod u genetičko inženjerstvo i biotehnologiju. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-1-8.
- ^ Hunter G. K. (2000): Vital Forces. The discovery of the molecular basis of life. Academic Press, London 2000, ISBN 0-12-361811-8.
- ^ Nelson D. L., Cox M. M. (2013): Lehninger principles of biochemistry. W. H. Freeman and Co., ISBN 978-1-4641-0962-1.
- ^ Arnold L., Wender P. H., McCloskey K., Snyder S. H. (1972): Levoamphetamine and Dextroamphetamine: Comparative efficacy in the iyperkinetic syndrome: Assessment by target symptoms. Arch Gen Psychiatry, 27 (6): 816-822. doi:10.1001/archpsyc.1972.01750300078015.
- ^ Teo S. K. Et al. (2004): Clinical pharmacokinetics of thalidomide. Clin. Pharmacokinet., 43 (5): 311–327.
- ^ Streitwieser A., Heathcock C. H. (1985): Introduction to organic chemistry, 3rd Ed. Maxwell MacMillan, ISBN 0029467209.
- ^ March J. (1985): Advanced organic chemistry: reactions, mechanisms, and structure, 3rd Ed. John Wiley & Sons, ISBN 0-471-85472-7.
Vanjski linkovi[uredi | uredi izvor]
- http://www.who.int/lep/research/thalidomide/en/index.html Arhivirano 29. 9. 2010. na Wayback Machine, WHO.
- http://www.nytimes.com/1998/07/17/us/thalidomide-approved-to-treat-leprosy-with-other-uses-seen.html, Thalidomide approved to treat leprosy, with other uses see, New York Times, Sheryl Gay Stolberg.
- http://www.who.int/lep/research/thalidomide/en/index.html Arhivirano 29. 9. 2010. na Wayback Machine
