Svegenomska studija asocijacije
U genomici, svegenomska studija asocijacije ili studija asocijacije širom genoma (GWA studija ili GWAS), poznata i kao cjelogenomska studija pridruživanja, je opservacijska studija skupa genoma za cjelovite genetičke varijante kod različitih jedinki, kako bi se provjerilo je li neka varijanta povezana sa osobinom. GWA-studije se obično fokusiraju na povezanost jednonukleotidnih polimorfizama (SNP) i osobina poput velikih ljudskih bolesti, ali se jednako mogu primijeniti na bilo koje druge genetičke varijante i bilo koje druge organizme.
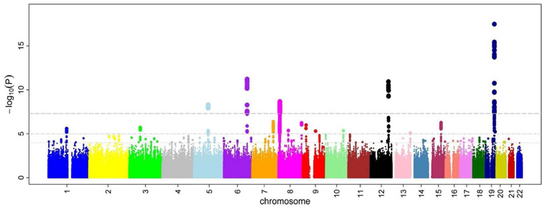
Manhattanski prikaz a GWAS-a
Kada se primijene na podatke o ljudima, GWA studije porede DNK sudionika s različitim fenotipom za određenu osobinu ili bolest. Ti sudionici mogu biti osobe s bolešću (slučajevi) i slične osobe bez bolesti (kontrole), ili mogu biti ljudi s različitim fenotipovima za određenu osobinu, naprimjer krvni pritisak. Ovaj pristup je poznat kao prvi s fenotipom, u kojem se sudionici prvo klasificiraju prema kliničkim manifestacijama, za razliku od pristupa prvi genotip. Svaka osoba daje uzorak DNK iz kojeg se čitaju milioni jednonukleotidnih polimorfizama , odnosno genetićke varijante pomoću sekvenciSNP-ova. Ako je jedan tip varijante (jedan alel) češći u ljudi s bolešću, kaže se da je varijanta „povezana“ s bolešću. Smatra se da povezani SNP-ovi označavaju područje ljudskog genoma koje može uticati na rizik od bolesti.
GWA studije istražuju cijeli genom, za razliku od metoda koji posebno testiraju mali broj unaprijed određenih genetičkih regija. Dakle, GWAS je pristup koji nije vođen kandidatima, za razliku od genetički specifične studije zasnovane na kandidatima. GWA studije identificiraju SNP-ove i druge varijante u DNK povezane s bolešću, ali ne mogu same odrediti koji su geni uzročni.[2][3][4]
Prvi uspješni GWAS objavljen 2002. godine proučavao je infarkt miokarda.[5] Ovaj dizajn studije zatim je implementiran u značajnu studiju GWA 2005. koja je istraživala pacijente sa starosnom makulskom degeneracijom i pronašao je dva SNP-a sa značajno izmijenjenom učestalosti alela u poređenju sa zdravim kontrolnim osobama.[6] Od 2017., više od 3.000 GWA studija na ljudima ispitalo je preko 1.800 bolesti i osobina, a pronađeno je na hiljade pridruženih SNP.[7] Osim u slučaju rijetkih nasljednih bolesti, ove asocijacije su vrlo slabe, ali iako ne mogu objasniti veliki rizik, pružaju uvid u gene i puteve koji mogu biti važni.
Osnovi[uredi | uredi izvor]

Bilo koja dva ljudska genoma razlikuju se na milione različitih načina. Postoje male varijacije u pojedinačnim nukleotidima genoma (SNP-ovi), kao i mnoge veće varijacije, poput delecija, insercija i varijacija broja kopija. Bilo koji od ovih može uzrokovati promjene osobina ili fenotipa, što može biti bilo šta, od rizika od bolesti do fizičkih svojstava, poput tjelesne visine.[9] Oko 2000., prije uvođenja GWA studija, primarni metod istraživanja bila je putem studija nasljeđivanja genetičke vezanosti u porodicama. Ovaj se pristup pokazao vrlo korisnim za poremećaje s jednim genom.[9][10][11] Međutim, za uobičajene i složene bolesti pokazalo se da su rezultati genetičkih veza teško reproducirani.[9][11] Predložena alternativa studijama povezivanja bila je studija genetičke pridruženosti. Ovaj tip studije pita da li se alel genetičke varijante nalazi češće nego što se očekivalo kod osoba sa fenotipom od interesa (npr. sa proučavanom bolešću). Rani proračuni o statističkoj moći pokazali su da bi ovaj pristup mogao biti bolji od studija povezivanja u otkrivanju slabih genetičkih efekata.[12]
Osim konceptnog okvira, nekoliko dodatnih faktora omogućilo je GWA studije. Jedan je bio pojavljivanje biobanki, skladišta ljudskog genetičkog materijala, koje su uveliko smanjile troškove i poteškoće u prikupljanju dovoljnog broja bioloških uzoraka za proučavanje.[13] Drugi je bio Međunarodni projekt HapMap, koji je od 2003. identificirao većinu uobičajenih SNP-ova ispitanih u studiji GWA.[14] Struktura haplobloka. identificirana HapMap projektom također je omogućila fokus na podskup SNP-ova koji bi opisali većinu varijacija. Također, razvoj metoda genotipizacije svih ovih SNP-ova korištenjem nizova genotipizacije bio je važan preduvjet.[15]
Metodi[uredi | uredi izvor]

Najčešći pristup GWA studija je postavka slučaj-kontrola, koja poredi dvije velike grupe osoba, jednu kontrolnu grupu zdravih i jednu grupu slučajeva zahvaćenih bolešću. Sve osobe, u svakoj grupi genotipizirane su za većinu poznatih SNP-ova. Tačan broj SNP-ova zavisi od tehnologije genotipizacije, ali je tipski milion ili više.[8] Za svaki od ovih SNP-ova tada se istražuje je li frekvencija alela značajno promijenjena između slučaja i kontrolne grupe.[17] U takvim postavkama, osnovna jedinica za izvještavanje o veličini efekata je omjer vjerovatnoća. Odnos omjera je omjer dvije šanse, koje su u kontekstu GWA studija šanse za jedinke koje imaju određeni alel, a šanse za jedinke koji nemaju isti alel.
Kao primjer, pretpostavla se da postoje dva alela, T i C. Broj jedinki u grupi slučajeva koji ima alel T predstavljen je s 'A', a broj jedinki u kontrolnoj grupi s alelom T predstavljen je sa 'B' . Slično tom, broj jedinki u grupi slučajeva koja ima alel C predstavljen je sa 'X', a broj jedinki u kontrolnoj grupi sa alelom C predstavljen je sa 'Y'. U ovom slučaju omjer šanse za alel T je A: B (što znači 'A do B', u standardnoj terminologiji koeficijenata) podijeljen sa , što je u matematičkom zapisu jednostavno ().
Kada je učestalost alela u grupi slučajeva mnogo veća nego u kontrolnoj grupi, omjer šanse je veći od 1, i obrnuto za nižu frekvenciju alela. Dodatno, P-vrijednost za značajnost omjera šanse obično se izračunava pomoću jednostavnog hi-kvadrat testa. Pronalaženje omjera vjerovatnoće koji se značajno razlikuju od 1 cilj je GWA studije jer to pokazuje da je SNP povezan s bolešću.[17] Budući da se testira toliko varijanti, standardna je praksa zahtijevati da p-vrijednost bude manja od 5−8, kako bi se varijanta smatrala značajnom.
Postoji nekoliko varijacija ovog pristupa kontrole slučaja. Uobičajena alternativa GWA studija kontrole slučaja je analiza kvantitativnih fenotipskih podataka, npr. visine ili koncentracije ili čak ekspresije gena. Slično tome, mogu se koristiti alternativne statistike dizajnirane za uzorke dominacije ili recesivne penetracije.[17] Proračuni se obično rade pomoću softvera za bioinformatiku, kao što su SNPTEST i PLINK, koji također uključuju podršku za mnoge od ovih alternativnih statistika.[16][18] GWAS se fokusira na učinak pojedinih SNP-ova. Međutim, moguće je i da složene interakcije između dva ili više SNP-ova, kao što je epistaza, mogu doprinijeti složenim bolestima. Zbog potencijalno eksponencijalnog broja interakcija, otkrivanje statistički značajnih interakcija u GWAS podacima je i računski i statistički izazov. Ovaj je zadatak riješen u postojećim publikacijama koje koriste algoritme inspirisane rudarenjem podataka.[19] Štaviše, istraživači pokušavaju integrirati GWA podatke s drugim biološkim podacima, poput mreža interakcija protein-protein kako bi izvukli više informativnih rezultata.[20][21]
Ključni korak u većini GWA studija je imputacija genotipova u SNP-a koji nisu na čipu genotipa koji se koristi u studiji.[22] Ovaj proces uveliko povećava broj SNP-ova koji se mogu testirati na povezanost, povećava snagu studije i olakšava metaanalizu GWAS-a u različitim kohortama. Imputiranje genotipa provodi se statističkim metodima koji kombiniraju GWAS-podatke zajedno s referentnom tablom haplotipova. Ovi metodi koriste prednosti dijeljenja haplotipova između jedinki na kratkim nizovima sekvence za imputiranje alela. Postojeći softverski paketi za imputaciju genotipa uključuju IMPUTE2,[23] Minimac, Beagle[24] i MaCH.[25]
Osim izračunavanja povezanosti, uobičajeno je uzeti u obzir sve varijable koje bi potencijalno mogle unijeti zbunjenost u rezultate. Spol i dob uobičajeni su primjeri zbunjujućih varijabli. Štaviše, također je poznato da su mnoge genetičke varijacije povezane s geografskim i povijesnim populacijama, u kojima su se mutacije prvi put pojavile.[26] Zbog ove povezanosti, studije moraju uzeti u obzir geografsko i etničko porijeklo učesnika kontrolišući ono što se naziva raslojavanje populacije. Ako to ne učine, ove studije mogu dati lažno pozitivne rezultate.[27]
Nakon što su omjeri šanse i p-vrijednosti izračunati za sve SNP-ove, uobičajen pristup je stvaranje Manhattan plota. U kontekstu GWA studija, ovaj grafikon prikazuje negativni logaritam p-vrijednosti u funkciji genomske lokacije. Tako se SNP-ovi s najznačajnijom asocijacijom ističu na plotu, obično kao gomile bodova zbog strukture haplobloka. Važno je da se prag p-vrijednosti korigira za probleme višestrukog testiranja. Tačan prag varira ovisno o studiji,[28] ali konvencijski prag je 5−8 da bude značajan u odnosu na stotine hiljada do miliona testiranih SNP-ova.[8][17][29] GWA studije obično provode prvu analizu u otkrivenih kohorti, nakon čega slijedi validacija najznačajnijih SNP-ova u nezavisnoj kohorti za validaciju.[30]
Rezultati[uredi | uredi izvor]

Ovaj tip plohe sličan je Manhattan plotu u vodećem odjeljku, ali za ograničeniji dio genoma. struktura haplobloka vizualizira se ljestvicom boja, a razina asocijacija je zadana lijevom Y osi. Tačka koja predstavlja rs73015013 SNP (u gornjem vrhu) ima lokaciju visoke Y osi jer ovaj SNP-a objašnjava neke varijacije u LDL-holesterolu.[31]
Učinjeni su pokušaji stvaranja sveobuhvatnih kataloga SNP-a koji su identificirani iz studija GWA.[32] Od 2009. godine SNP-ovi povezani sa bolestima broje se u hiljadama.[33]
Prva studija GWA, provedena 2005., poredila je 96 pacijenata sa starosnom makulskom degeneracijom (ARMD) sa grupom od50 zdravih kontrolnih osoba.[34] Identificirana su dva SNP-a sa značajno promijenjenom frekvencijom alela između dvije grupe. Ovi SNP-apovi locirani su u genu koji kodira faktor komplementa H, što je bio neočekivan nalaz u istraživanju ARMD-a. Nalazi iz ovih prvih GWA studija kasnije su podstaknuli daljnja funkcionalna istraživanja prema terapijskoj manipulaciji komplementnog sistema u ARMD-u.[35] Još jedna značajna publikacija u historiji GWA studija bila je Wellcome Trust Case Control Consortium (WTCCC) studija, najveća GWA studija ikada sprovedena u vrijeme objavljivanja 2007. WTCCC je obuhvatio 14.000 slučajeva sedam uobičajenih bolesti (~2000 osoba za svaku od sljedećih bolesti: koronarna bolesti srca, dijabetes tipa 1, dijabetes tip 2, reumatoidni artritis, Crohnova bolest, bipolarni poremećaj i hipertenzija) i 3.000 zajedničkih kontrola.[16] This study was successful in uncovering many new disease genes underlying these diseases.[16][36]
Od ovih prvih značajnih GWA studija, postojala su dva opća trenda.[37] Jedan je bio usmjeren na sve veće uzorke. U 2018. nekoliko studija o asocijaciji na čitavom genomu dostiglo je ukupnu veličinu uzorka od preko milion sudionika, uključujući 1,1 milion u studiji obrazovnih postignuća u širom genoma [38] i studija o nesanici koja sadrži 1,3 miliona osoba.[39] Razlog je težnja ka pouzdanom otkrivanju SNP-a od rizika koji imaju manji omjeri vjerovatnoće i nižu frekvenciju alela. Drugi trend bio je prema korištenju usko definiranih fenotipova, kao što su lipidi u krvi, proinsulin ili slični biomarkeri.[40][41] Oni se nazivaju "intermedijarni fenotipovi", a njihove analize mogu biti od vrijednosti funkcionalnim istraživanjima biomarkera.[42] Varijacija GWAS-a koristi učesnike koji su „srodnici“ prvog stepena ljudi sa bolešću. Ovaj tip proksi istraživanja nazvan je studija asocijacije na čitav genom (GWAX).[43]
Centralna tačka rasprave o GWA studijama bila je da je većina varijacija SNP-a koje su pronađene GWA studijama povezana samo sa malim povećanim rizikom od bolesti i da imaju samo malu prediktivnu vrijednost. Srednji omjer šanse je 1,33 po SNP-u rizika, sa samo nekoliko koji pokazuju omjer šanse iznad 3,0.[2][44] These magnitudes are considered small because they do not explain much of the heritable variation. This heritable variation is estimated from heritability studies based on monozygotic twins.[45] Naprimjer, poznato je da se 80-90% varijance u visini može objasniti nasljednim razlikama, ali studije GWA objašnjavaju samo manji dio ove varijance.[45]
Kliničke aplikacije[uredi | uredi izvor]
Izazov za buduću uspješnu studiju GWA-a je primijena nalaze na način koji ubrzava razvoj lijekova i dijagnostike, uključujući bolju integraciju genetičkih studija u proces razvoja lijekova i fokus na ulogu genetičkih varijacija u očuvanju zdravlja kao nacrt za osmišljavanje novih lijekova i dijagnostike.[46] Nekoliko studija je razmatralo upotrebu markera rizika SNP-a kao sredstvo za direktno poboljšanje tačnosti prognoze. Neki su otkrili da se tačnost prognoze poboljšava,[47] dok drugi prijavljuju samo manje koristi od ove upotrebe.[48] Općenito, problem sa ovim direktnim pristupom su male veličine uočenih efekata. Mali učinak na kraju pretvara se u loše odvajanje slučajeva i kontrola, a time i samo malo poboljšanje tačnosti prognoze. Alternativna primjena je stoga potencijal GWA studija da razjasne patofiziološke promjene.[49]
Jedan takav uspjeh studija GWA povezan je s identifikacijom genetičke varijante povezane s odgovorom na liječenje virusom anti-hepatitisa C. Kenotip 1 hepatitisa C liječen je pegiliranim interferonom-alfa-2a ili pegiliranim interferonom-alfa-2b, u kombinaciji s ribavirinom[50] pokazao je da su SNP u blizini ljudskog gena IL28B, koji kodira interferon lambda 3, povezani sa značajnim razlikama u odgovoru na liječenje. Kasniji izvještaj pokazao je da su iste genetičke varijante povezane i s prirodnim uklanjanjem virusa hepatitisa C genotipa 1.[51] Ovi glavni nalazi olakšali su razvoj personalizirane medicine i omogućili ljekarima da prilagode medicinske odluke na osnovu genotipa pacijenta.[52]
Cilj razjašnjenja patofizioloških promjena također je doveo do povećanog interesa za povezanost rizika-SNP-a i ekspresije gena u blizini datog gena, takozvanih ekspresijskih lokusa kvantitativnih svojstava (eQTL).[53] Razlog je u tome što GWAS studije identificiraju rizične [[SNP[]]-ove, ali ne i rizične gene, a specifikacija gena je korak bliže djelovanju na ciljeve lijekova. Kao rezultat toga, velike GWA studije do 2011. obično su uključivale opsežnu eQTL analizu..[54][55][56] Jedan od najjačih efekata eQTL-a uočenih za rizične SNP identificiran sa GWA je lokus SORT1.[40] Funkcionalne dodatne studije ovog lokusa korištenjem male interferirajuće RNK i nokaut-miševa bacili su svjetlo na metabolizam lipoproteina niske gustoće, koji imaju važne kliničke implikacije za kardiovaskularne bolesti.[40][57][58]
Fino mapiranje[uredi | uredi izvor]
Genotipski nizovi dizajnirani za GWAS oslanjaju se na neravnotežu vezanja, kako bi osigurali pokrivanje cijelog genoma genotipizacijom podskupa varijanti. Zbog toga je malo vjerovatno da će prijavljene povezane varijante biti stvarne uzročne varijante. Pridružene regije mogu sadržavati stotine varijanti koje obuhvaćaju velike regije i obuhvataju mnogo različitih gena, što otežava biološku interpretaciju GWAS lokusa. Fino mapiranje je proces poboljšanja ovih lista povezanih varijanti u vjerodostojan skup koji će najvjerovatnije uključivati uzročnu varijantu.
Fino mapiranje zahtijeva da sve varijante u pridruženom području budu genotipizirane ili imputirane (gusta pokrivenost), vrlo stroga kontrola kvaliteta, koja rezultira visokokvalitetnim genotipovima i velike veličine uzorka, dovoljne za odvajanje visoko koreliranih signala. Postoji nekoliko različitih metoda za izvođenje finog mapiranja, a sve proizvode zadnju vjerovatnoću da je varijanta u tom lokusu uzročna. Budući da je zahtjeve često teško zadovoljiti, još uvijek postoje ograničeni primjeri općenitije primjene ovih metoda.
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Ikram MK, Sim X, Xueling S, Jensen RA, Cotch MF, Hewitt AW, et al. (oktobar 2010). McCarthy MI (ured.). "Four novel Loci (19q13, 6q24, 12q24, and 5q14) influence the microcirculation in vivo". PLOS Genetics. 6 (10): e1001184. doi:10.1371/journal.pgen.1001184. PMC 2965750. PMID 21060863.
- ^ a b Manolio TA (juli 2010). "Genomewide association studies and assessment of the risk of disease". The New England Journal of Medicine. 363 (2): 166–76. doi:10.1056/NEJMra0905980. PMID 20647212.
- ^ Pearson TA, Manolio TA (mart 2008). "How to interpret a genome-wide association study". JAMA. 299 (11): 1335–44. doi:10.1001/jama.299.11.1335. PMID 18349094.
- ^ "Genome-Wide Association Studies". National Human Genome Research Institute.
- ^ Ozaki K, Ohnishi Y, Iida A, Sekine A, Yamada R, Tsunoda T, et al. (decembar 2002). "Functional SNPs in the lymphotoxin-alpha gene that are associated with susceptibility to myocardial infarction". Nature Genetics. 32 (4): 650–4. doi:10.1038/ng1047. PMID 12426569. S2CID 21414260.
- ^ Klein RJ, Zeiss C, Chew EY, Tsai JY, Sackler RS, Haynes C, et al. (april 2005). "Complement factor H polymorphism in age-related macular degeneration". Science. 308 (5720): 385–9. Bibcode:2005Sci...308..385K. doi:10.1126/science.1109557. PMC 1512523. PMID 15761122.
- ^ "GWAS Catalog: The NHGRI-EBI Catalog of published genome-wide association studies". European Molecular Biology Laboratory. European Molecular Biology Laboratory. Pristupljeno 18. 4. 2017.
- ^ a b c Bush WS, Moore JH (2012). Lewitter F, Kann M (ured.). "Chapter 11: Genome-wide association studies". PLOS Computational Biology. 8 (12): e1002822. Bibcode:2012PLSCB...8E2822B. doi:10.1371/journal.pcbi.1002822. PMC 3531285. PMID 23300413.
- ^ a b c Strachan T, Read A (2011). Human Molecular Genetics (4th izd.). Garland Science. str. 467–495. ISBN 978-0-8153-4149-9.
- ^ "Online Mendelian Inheritance in Man". Arhivirano s originala, 5. 12. 2011. Pristupljeno 6. 12. 2011.
- ^ a b Altmüller J, Palmer LJ, Fischer G, Scherb H, Wjst M (novembar 2001). "Genomewide scans of complex human diseases: true linkage is hard to find". American Journal of Human Genetics. 69 (5): 936–50. doi:10.1086/324069. PMC 1274370. PMID 11565063.
- ^ Risch N, Merikangas K (septembar 1996). "The future of genetic studies of complex human diseases". Science. 273 (5281): 1516–7. Bibcode:1996Sci...273.1516R. doi:10.1126/science.273.5281.1516. PMID 8801636. S2CID 5228523.
- ^ Greely HT (2007). "The uneasy ethical and legal underpinnings of large-scale genomic biobanks". Annual Review of Genomics and Human Genetics. 8: 343–64. doi:10.1146/annurev.genom.7.080505.115721. PMID 17550341.
- ^ The International HapMap Project, Gibbs RA, Belmont JW, Hardenbol P, Willis TD, Yu F, Yang H, Ch'Ang LY, Huang W (decembar 2003). "The International HapMap Project" (PDF). Nature. 426 (6968): 789–96. Bibcode:2003Natur.426..789G. doi:10.1038/nature02168. hdl:2027.42/62838. PMID 14685227. S2CID 4387110.
- ^ Schena M, Shalon D, Davis RW, Brown PO (oktobar 1995). "Quantitative monitoring of gene expression patterns with a complementary DNA microarray". Science. 270 (5235): 467–70. Bibcode:1995Sci...270..467S. doi:10.1126/science.270.5235.467. PMID 7569999. S2CID 6720459.
- ^ a b c d Wellcome Trust Case Control Consortium, Burton PR (juni 2007). "Genome-wide association study of 14,000 cases of seven common diseases and 3,000 shared controls". Nature[]. 447 (7145): 661–78. Bibcode:2007Natur.447..661B. doi:10.1038/nature05911. PMC 2719288. PMID 17554300.
- ^ a b c d Clarke GM, Anderson CA, Pettersson FH, Cardon LR, Morris AP, Zondervan KT (februar 2011). "Basic statistical analysis in genetic case-control studies". Nature Protocols. 6 (2): 121–33. doi:10.1038/nprot.2010.182. PMC 3154648. PMID 21293453.
- ^ Purcell S, Neale B, Todd-Brown K, Thomas L, Ferreira MA, Bender D, et al. (septembar 2007). "PLINK: a tool set for whole-genome association and population-based linkage analyses". American Journal of Human Genetics. 81 (3): 559–75. doi:10.1086/519795. PMC 1950838. PMID 17701901.
- ^ Llinares-López F, Grimm DG, Bodenham DA, Gieraths U, Sugiyama M, Rowan B, Borgwardt K (juni 2015). "Genome-wide detection of intervals of genetic heterogeneity associated with complex traits". Bioinformatics. 31 (12): i240-9. doi:10.1093/bioinformatics/btv263. PMC 4559912. PMID 26072488.
- ^ Ayati M, Erten S, Chance MR, Koyutürk M (decembar 2015). "MOBAS: identification of disease-associated protein subnetworks using modularity-based scoring". EURASIP Journal on Bioinformatics & Systems Biology. 2015 (1): 7. doi:10.1186/s13637-015-0025-6. PMC 5270451. PMID 28194175.
- ^ Ayati M, Koyutürk M (1. 1. 2015). "Assessing the Collective Disease Association of Multiple Genomic Loci". Proceedings of the 6th ACM Conference on Bioinformatics, Computational Biology and Health Informatics. BCB '15. New York, NY, USA: ACM. str. 376–385. doi:10.1145/2808719.2808758. ISBN 978-1-4503-3853-0. S2CID 5942777.
- ^ Marchini J, Howie B (juli 2010). "Genotype imputation for genome-wide association studies". Nature Reviews Genetics. 11 (7): 499–511. doi:10.1038/nrg2796. PMID 20517342. S2CID 1465707.
- ^ Howie B, Marchini J, Stephens M (novembar 2011). "Genotype imputation with thousands of genomes". G3. 1 (6): 457–70. doi:10.1534/g3.111.001198. PMC 3276165. PMID 22384356.
- ^ Browning BL, Browning SR (februar 2009). "A unified approach to genotype imputation and haplotype-phase inference for large data sets of trios and unrelated individuals". American Journal of Human Genetics. 84 (2): 210–23. doi:10.1016/j.ajhg.2009.01.005. PMC 2668004. PMID 19200528.
- ^ Li Y, Willer CJ, Ding J, Scheet P, Abecasis GR (decembar 2010). "MaCH: using sequence and genotype data to estimate haplotypes and unobserved genotypes". Genetic Epidemiology. 34 (8): 816–34. doi:10.1002/gepi.20533. PMC 3175618. PMID 21058334.
- ^ Novembre J, Johnson T, Bryc K, Kutalik Z, Boyko AR, Auton A, Indap A, King KS, Bergmann S, Nelson MR, Stephens M, Bustamante CD (novembar 2008). "Genes mirror geography within Europe". Nature. 456 (7218): 98–101. Bibcode:2008Natur.456...98N. doi:10.1038/nature07331. PMC 2735096. PMID 18758442.
- ^ Charney E (januar 2017). "Genes, behavior, and behavior genetics". Wiley Interdisciplinary Reviews. Cognitive Science. 8 (1–2): e1405. doi:10.1002/wcs.1405. hdl:10161/13337. PMID 27906529.
- ^ Wittkowski KM, Sonakya V, Bigio B, Tonn MK, Shic F, Ascano M, Nasca C, Gold-Von Simson G (januar 2014). "A novel computational biostatistics approach implies impaired dephosphorylation of growth factor receptors as associated with severity of autism". Translational Psychiatry. 4 (1): e354. doi:10.1038/tp.2013.124. PMC 3905234. PMID 24473445.
- ^ Barsh GS, Copenhaver GP, Gibson G, Williams SM (juli 2012). "Guidelines for genome-wide association studies". PLOS Genetics. 8 (7): e1002812. doi:10.1371/journal.pgen.1002812. PMC 3390399. PMID 22792080.
- ^ Smith SM, Douaud G, Chen W, Hanayik T, Alfaro-Almagro F, Sharp K, Elliott LT (2021). "An expanded set of genome-wide association studies of brain imaging phenotypes in UK Biobank". Nat Neurosci. 24 (5): 737–745. doi:10.1038/s41593-021-00826-4. PMC 7610742. PMID 33875891.CS1 održavanje: više imena: authors list (link)
- ^ Sanna S, Li B, Mulas A, Sidore C, Kang HM, Jackson AU, et al. (juli 2011). Gibson G (ured.). "Fine mapping of five loci associated with low-density lipoprotein cholesterol detects variants that double the explained heritability". PLOS Genetics. 7 (7): e1002198. doi:10.1371/journal.pgen.1002198. PMC 3145627. PMID 21829380.
- ^ Hindorff LA, Sethupathy P, Junkins HA, Ramos EM, Mehta JP, Collins FS, Manolio TA (juni 2009). "Potential etiologic and functional implications of genome-wide association loci for human diseases and traits". Proceedings of the National Academy of Sciences of the United States of America. 106 (23): 9362–7. Bibcode:2009PNAS..106.9362H. doi:10.1073/pnas.0903103106. PMC 2687147. PMID 19474294.
- ^ Johnson AD, O'Donnell CJ (januar 2009). "An open access database of genome-wide association results". BMC Medical Genetics. 10: 6. doi:10.1186/1471-2350-10-6. PMC 2639349. PMID 19161620.
- ^ Haines JL, Hauser MA, Schmidt S, Scott WK, Olson LM, Gallins P, Spencer KL, Kwan SY, Noureddine M, Gilbert JR, Schnetz-Boutaud N, Agarwal A, Postel EA, Pericak-Vance MA (april 2005). "Complement factor H variant increases the risk of age-related macular degeneration". Science. 308 (5720): 419–21. Bibcode:2005Sci...308..419H. doi:10.1126/science.1110359. PMID 15761120. S2CID 32716116.
- ^ Fridkis-Hareli M, Storek M, Mazsaroff I, Risitano AM, Lundberg AS, Horvath CJ, Holers VM (oktobar 2011). "Design and development of TT30, a novel C3d-targeted C3/C5 convertase inhibitor for treatment of human complement alternative pathway-mediated diseases". Blood. 118 (17): 4705–13. doi:10.1182/blood-2011-06-359646. PMC 3208285. PMID 21860027.
- ^ "Largest ever study of genetics of common diseases published today" (Press release). Wellcome Trust Case Control Consortium. 6. 6. 2007. Arhivirano s originala, 4. 6. 2008. Pristupljeno 19. 6. 2008.
- ^ Ioannidis JP, Thomas G, Daly MJ (maj 2009). "Validating, augmenting and refining genome-wide association signals". Nature Reviews Genetics. 10 (5): 318–29. doi:10.1038/nrg2544. PMC 7877552. PMID 19373277. S2CID 6463743.
- ^ Lee JJ, Wedow R, Okbay A, Kong E, Maghzian O, Zacher M, Nguyen-Viet TA, Bowers P, Sidorenko J, Karlsson Linnér R, et al. (juli 2018). "Gene discovery and polygenic prediction from a genome-wide association study of educational attainment in 1.1 million individuals". Nature Genetics. 50 (8): 1112–1121. doi:10.1038/s41588-018-0147-3. PMC 6393768. PMID 30038396.
- ^ Jansen PR, Watanabe K, Stringer S, Skene N, Bryois J, Hammerschlag AR, et al. (januar 2018). "Genome-wide Analysis of Insomnia (N=1,331,010) Identifies Novel Loci and Functional Pathways". doi:10.1101/214973. journal zahtijeva
|journal=(pomoć) - ^ a b c Kathiresan S, Willer CJ, Peloso GM, Demissie S, Musunuru K, Schadt EE, et al. (januar 2009). "Common variants at 30 loci contribute to polygenic dyslipidemia". Nature Genetics. 41 (1): 56–65. doi:10.1038/ng.291. PMC 2881676. PMID 19060906.
- ^ Strawbridge RJ, Dupuis J, Prokopenko I, Barker A, Ahlqvist E, Rybin D, et al. (oktobar 2011). "Genome-wide association identifies nine common variants associated with fasting proinsulin levels and provides new insights into the pathophysiology of type 2 diabetes". Diabetes. 60 (10): 2624–34. doi:10.2337/db11-0415. PMC 3178302. PMID 21873549.
- ^ Danesh J, Pepys MB (novembar 2009). "C-reactive protein and coronary disease: is there a causal link?". Circulation. 120 (21): 2036–9. doi:10.1161/CIRCULATIONAHA.109.907212. PMID 19901186.
- ^ Liu JZ, Erlich Y, Pickrell JK (mart 2017). "Case-control association mapping by proxy using family history of disease". Nature Genetics. 49 (3): 325–331. doi:10.1038/ng.3766. PMID 28092683. S2CID 5598845.
- ^ Ku CS, Loy EY, Pawitan Y, Chia KS (april 2010). "The pursuit of genome-wide association studies: where are we now?". Journal of Human Genetics. 55 (4): 195–206. doi:10.1038/jhg.2010.19. PMID 20300123.
- ^ a b Maher B (novembar 2008). "Personal genomes: The case of the missing heritability". Nature. 456 (7218): 18–21. doi:10.1038/456018a. PMID 18987709.
- ^ Iadonato SP, Katze MG (septembar 2009). "Genomics: Hepatitis C virus gets personal". Nature. 461 (7262): 357–8. Bibcode:2009Natur.461..357I. doi:10.1038/461357a. PMID 19759611. S2CID 7602652.Šablon:Closed access
- ^ Muehlschlegel JD, Liu KY, Perry TE, Fox AA, Collard CD, Shernan SK, Body SC (septembar 2010). "Chromosome 9p21 variant predicts mortality after coronary artery bypass graft surgery". Circulation. 122 (11 Suppl): S60–5. doi:10.1161/CIRCULATIONAHA.109.924233. PMC 2943860. PMID 20837927.
- ^ Paynter NP, Chasman DI, Paré G, Buring JE, Cook NR, Miletich JP, Ridker PM (februar 2010). "Association between a literature-based genetic risk score and cardiovascular events in women". JAMA. 303 (7): 631–7. doi:10.1001/jama.2010.119. PMC 2845522. PMID 20159871.
- ^ Couzin-Frankel J (juni 2010). "Major heart disease genes prove elusive". Science. 328 (5983): 1220–1. Bibcode:2010Sci...328.1220C. doi:10.1126/science.328.5983.1220. PMID 20522751.Šablon:Closed access
- ^ Ge D, Fellay J, Thompson AJ, Simon JS, Shianna KV, Urban TJ, Heinzen EL, Qiu P, Bertelsen AH, Muir AJ, Sulkowski M, McHutchison JG, Goldstein DB (septembar 2009). "Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance". Nature. 461 (7262): 399–401. Bibcode:2009Natur.461..399G. doi:10.1038/nature08309. PMID 19684573. S2CID 1707096.
- ^ Thomas DL, Thio CL, Martin MP, Qi Y, Ge D, O'Huigin C, Kidd J, Kidd K, Khakoo SI, Alexander G, Goedert JJ, Kirk GD, Donfield SM, Rosen HR, Tobler LH, Busch MP, McHutchison JG, Goldstein DB, Carrington M (oktobar 2009). "Genetic variation in IL28B and spontaneous clearance of hepatitis C virus". Nature. 461 (7265): 798–801. Bibcode:2009Natur.461..798T. doi:10.1038/nature08463. PMC 3172006. PMID 19759533.
- ^ Lu YF, Goldstein DB, Angrist M, Cavalleri G (juli 2014). "Personalized medicine and human genetic diversity". Cold Spring Harbor Perspectives in Medicine. 4 (9): a008581. doi:10.1101/cshperspect.a008581. PMC 4143101. PMID 25059740.
- ^ Folkersen L, van't Hooft F, Chernogubova E, Agardh HE, Hansson GK, Hedin U, Liska J, Syvänen AC, Paulsson-Berne G, Paulssson-Berne G, Franco-Cereceda A, Hamsten A, Gabrielsen A, Eriksson P (august 2010). "Association of genetic risk variants with expression of proximal genes identifies novel susceptibility genes for cardiovascular disease". Circulation: Cardiovascular Genetics. 3 (4): 365–73. doi:10.1161/CIRCGENETICS.110.948935. PMID 20562444.
- ^ Bown MJ, Jones GT, Harrison SC, Wright BJ, Bumpstead S, Baas AF, et al. (novembar 2011). "Abdominal aortic aneurysm is associated with a variant in low-density lipoprotein receptor-related protein 1". American Journal of Human Genetics. 89 (5): 619–27. doi:10.1016/j.ajhg.2011.10.002. PMC 3213391. PMID 22055160.
- ^ Coronary Artery Disease (C4D) Genetics Consortium (mart 2011). "A genome-wide association study in Europeans and South Asians identifies five new loci for coronary artery disease". Nature Genetics. 43 (4): 339–44. doi:10.1038/ng.782. PMID 21378988. S2CID 39712343.[mrtav link]Šablon:Closed access
- ^ Johnson T, Gaunt TR, Newhouse SJ, Padmanabhan S, Tomaszewski M, Kumari M, et al. (decembar 2011). "Blood pressure loci identified with a gene-centric array". American Journal of Human Genetics. 89 (6): 688–700. doi:10.1016/j.ajhg.2011.10.013. PMC 3234370. PMID 22100073.
- ^ Dubé JB, Johansen CT, Hegele RA (juni 2011). "Sortilin: an unusual suspect in cholesterol metabolism: from GWAS identification to in vivo biochemical analyses, sortilin has been identified as a novel mediator of human lipoprotein metabolism". BioEssays. 33 (6): 430–7. doi:10.1002/bies.201100003. PMID 21462369.Šablon:Closed access
- ^ Bauer RC, Stylianou IM, Rader DJ (april 2011). "Functional validation of new pathways in lipoprotein metabolism identified by human genetics". Current Opinion in Lipidology. 22 (2): 123–8. doi:10.1097/MOL.0b013e32834469b3. PMID 21311327. S2CID 24020035.Šablon:Closed access
External links[uredi | uredi izvor]
| Commons ima datoteke na temu: Svegenomska studija asocijacije |
- Genotype-phenotype interaction software tools and databases on omicX[mrtav link]
- Statistical Methods for the Analysis of Genome-Wide Association Studies [video lecture series]
- Whole genome association studies — by the National Human Genome Research Institute
- GWAS Central — a central database of summary-level genetic association findings
- Barrett, Jeff (18. 7. 2010). "How to read a genome-wide association study". Genomes Unzipped. Arhivirano s originala, 24. 9. 2020. Pristupljeno 24. 9. 2021.
- Consortia of genome-wide association studies (GWAS) Arhivirano 26. 2. 2018. na Wayback Machine — by Bennett SN, Caporaso, NE, et al.
- PLINK — whole genome association analysis toolset
- ENCODE threads explorer Impact of functional information on understanding variation. *Nature



