Hibridizacija orbitala
Ovaj članak ili neki od njegovih odlomaka nije dovoljno potkrijepljen izvorima (literatura, veb-sajtovi ili drugi izvori). |
Hibridizacija orbitala u hemiji je koncept miješanja atomskih orbitala, pri čemu nastaju hibridne orbitale. Hibridne orbitale u sklopu teorije valentne veze objašnjavaju oblik molekulskih orbitala kod molekula.
Historija[uredi | uredi izvor]
Pojam hibridizacije orbitala je uveo Linus Pauling, prilikom objašnjenja strukture molekule metana CH4. Koncept koji je razvijen na tako jednostavnoj molekuli je kasnije primijenjen i na druge organske molekule. Osim toga, hibridizacijom orbitala se objašnjava struktura kompleksnih spojeva.
sp3 hibridizacija[uredi | uredi izvor]
Elektronska konfiguracija ugljika je 1s2 2s2 2px1 2py1 i to se može prikazati:
U prvom koraku hibridizacije dolazi do ekscitacije elektrona iz 2s u 2p orbitalu.
Miješanjem 2s i 2p orbitala nastaju četiri hibridne sp3 orbitale:
One se prekrivaju sa 1s orbitalama iz vodonikovih atoma pa nastaje tetraedarska struktura.
-
Nastajanje sp3 hibridnih orbitala u molekuli metana
-
Struktura molekule metana
sp2 hibridizacija[uredi | uredi izvor]
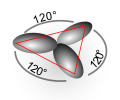
Miješanjem dvije p orbitale sa s orbitalom nastaju tri hibridne sp2 orbitale, koje leže u jednoj ravni pod uglom 120°. Elektroni ovih orbitala formiraju σ-vezu, a preostali p-elektroni daju π-vezu. Ovaj tip hibridizacije je prisutan u molekuli etena.
-
sp2 hibridizacija
sp hibridizacija[uredi | uredi izvor]
Ovaj tip je prisutan kod alkina. Jedna p orbitala se miješa sa jednom s orbitalom dajući dvije hibridne sp-orbitale. Preostali p-elektroni daju dvije π-veze, pa nastaje trostruka veza. Nastale hibridne orbitale leže pod uglom 180°, pa je molekula linearna.
sp3d i sp3d2 hibridizacija[uredi | uredi izvor]
Miješanjem s i p orbitala mogu nastati maksimalno četiri hibridne orbitale, koje popunjava osam elektrona. U nekim slučajevima dolazi do stvaranja više od četiri veze, pa u tom slučaju u hibridizaciju ulaze i d orbitale. Hibridne sp3d orbitale daju oblik trigonske bipiramide (npr. molekula PCl5). Hibridne sp3d2 orbitale daju oblik oktaedra (npr. SF6).
Također pogledajte[uredi | uredi izvor]
![]() Nedovršeni članak Hibridizacija orbitala koji govori o hemiji treba dopuniti. Dopunite ga prema pravilima Wikipedije.
Nedovršeni članak Hibridizacija orbitala koji govori o hemiji treba dopuniti. Dopunite ga prema pravilima Wikipedije.