Permanganat
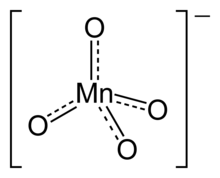
Permanganati je opći naziv za hemijske spojeve koji sadrže manganat (VII) ion (MnO4−). Pošto mangan u tim spojevima ima oksidacijsko stanje +7, permanganatni(VII) ion je jako oksidacijsko sredstvo. Ion ima tetrahedralnu geometriju.[1] Rastvori permanganata su ljubičaste boje i stabilni su u neutralnim i blago bazičnim sredinama. Tačna hemijska reakcija zavisi od prisutnih organskih nečistoća i oksidanta koji se koristi. Naprimjer, trihloroetan (C2HCl3) se oksidira u prisustvu natrij-permanganata i daje ugljik-dioksid, mangan-dioksid, ione natrija (Na+), hidronij ione (H+) i ione hlora (Cl-).[2]
Permanganati su vrlo korisni reagensi sa organskim spojevima, ali nisu izrazito selektivni. Termalno, magnanati(VII) nisu stabilni. Naprimjer kalij-permanganat se raspada na temperaturi od 230 °C na kalij-manganat i mangan-dioksid, otpuštajući kisik:
- 2 KMnO4 → K2MnO4 + MnO2 + O2
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Sukalyan Dash, Sabita Patel and Bijay K. Mishra (2009). "Oxidation by permanganate: synthetic and mechanistic aspects". Tetrahedron 65 (4): 707–739. doi:10.1016/j.tet.2008.10.038
- ^ http://geocleanse.com/permanaganate.asp
