Natrij
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Natrij u periodnom sistemu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Hemijski element, Simbol, Atomski broj | Natrij, Na, 11 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serija | Alkalni metali | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa, Perioda, Blok | 1, 3, s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izgled | srebreno bijeli | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zastupljenost | 2,64[1] % | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomske osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomska masa | 22,98976928 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomski radijus (izračunat) | 180 (190) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentni radijus | 154 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsov radijus | 227 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronska konfiguracija | [Ne] 3s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Broj elektrona u energetskom nivou | 2, 8, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. energija ionizacije | 495,8 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikalne osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Agregatno stanje | čvrsto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohsova skala tvrdoće | 0,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristalna struktura | kubična prostorno centrirana | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gustoća | 968[2] kg/m3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetizam | paramagnetičan ( = 8,5 · 10−6)[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tačka topljenja | 370,87 K (97,72 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tačka ključanja | 1163 K (890[4] °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarni volumen | 23,78 · 10−6 m3/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplota isparavanja | 97,4[4] kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplota topljenja | 2,60 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pritisak pare | 1 Pa pri 554[3] K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brzina zvuka | 3200 m/s pri 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Specifična toplota | 1230 J/(kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Specifična električna provodljivost | 21 · 106 S/m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplotna provodljivost | 140 W/(m · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hemijske osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidacioni broj | 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksid | Na2O | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrodni potencijal | −2,713 V (Na++ e− → Na) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativnost | 0,93 (Pauling-skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sigurnosno obavještenje | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oznake upozorenja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Obavještenja o riziku i sigurnosti | R: 14/15-34 S: (1/2-)5-8-43-45 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ako je moguće i u upotrebi, koriste se osnovne SI jedinice. Ako nije drugačije označeno, svi podaci dobijeni su mjerenjima u normalnim uvjetima. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Natrij (latinski: natrium) jest hemijski element koji ima simbol Na i atomski broj 11. U periodnom sistemu nalazi se u trećoj periodi i kao alkalni metal u IA (glavnoj) grupi. Jedini stabilni izotop mu je 23Na.
Elementarni natrij prvi put je dobio Humphry Davy 1807. godine putem elektrolize istopljenog natrij hidroksida te mu dao ime sodium. Ovaj naziv se i danas koristi u mnogim jezicima, kao što su engleski i francuski, a njegovi nazivi u romanskim i nekim slavenskim jezicima se donekle razlikuju. U bosanskom jeziku, ime natrij je izvedeno iz arapskog ناترون natrun, natron, odnosno iz egipatskog netjerj. Pored bosanskog, ovaj naziv je raširen i u germanskim i slavenskim jezicima.
U normalnim uslovima, natrij je poput voska mehki metal, srebrenastog sjaja i izuzetno reaktivan. Zbog svoje velike reaktivnosti metalni (elementarni) natrij se skladišti u inertnim uslovima, najčešće u parafinskom ulju ili petroleumu, a za veće količine koriste se hermetički zatvorene čelične bačve. Natrij spada među deset najčešćih elemenata u Zemljinoj kori. Javlja se u brojnim mineralima u stijenama i na morskom dnu. U okeanima su također rastvorene značajne količine natrija u obliku iona.
Historija[uredi | uredi izvor]
Otkrio ga je engleski hemičar Sir Humphry Davy 1807. elektrolizom rastaljenog natrij-hidroksida (NaOH).
U starom Egiptu i u antičkim vremenima iz slanih jezera se dobijala soda, koju su Egipćani zvali netjerj (neter). Grci su preuzeli ovu riječ kao νίτρον nitron, Rimljani kao nitrium a Arapi kao ناترون natrun.[5] Spojevi natrija su, za razliku od elementarnog natrija, poznati mnogo duže, a neki od njih su se dobijali i prerađivali iz morske vode, jezera i izvora zemnog plina. Jedan od najvažnijih spojeva natrija je natrij-hlorid (kuhinjska so), koja se dobija u rudnicima ili isušivanjem morske vode odnosno slanih podzemnih voda. U historiji, kuhinjska so je bila jedan od najvažnijih trgovačkih artikala, na kojem su mnogi historijski gradovi izgradili svoju vojnu i ekonomsku moć. I danas nazivi brojnih gradova su izvedeni iz riječi so, kao što je Tuzla (tur. tuz) ili Salzburg (njem. Salz), te Halle (Saale), Bad Hall ili Hall in Tirol po germanskom nazivu Hall.[6] Osim soli, i brojni drugi prirodni natrijevi spojevi poput natrij-karbonata (soda ili natron) su se također koristili od davnih vremena.

Dobijanje elementarnog natrija prvi put je uspjelo engleskom naučniku Humphry Davyu 1807. godine putem elektrolize istopljenog natrij hidroksida (žive sode) korištenjem Voltinog elektrostatičkog stuba kao izvorom struje. Po izvještaju Kraljevskog društva iz Londona od 19. novembra 1807. godine, Davy je dobio dva različita metala: u sodi sadržani natrij koji je on nazvao sodium, naziv koji se i danas koristi za ovaj element u francuskom i engleskom jeziku, te drugi metal koji je on nazvao potassium (kalij). Berzelius je 1811. godine umjesto sodium predložio današnji naziv natrium.[5]
Osobine[uredi | uredi izvor]
Fizičke[uredi | uredi izvor]
Natrij je srebrenasto bijeli, mehki i lahki metal. U mnogim fizičkim osobinama, natrij stoji između litija i kalija. Tako naprimjer, tačka topljenja natrij iznosi 97,82 °C, što je između litijeve (180,54 °C) i kalijeve (63,6 °C).[8] Slično je i kod tačke ključanja i specifičnog toplotnog kapaciteta. Sa gustoćom od 0,968 g · cm−3[8] natrij spada u elemente sa najmanjom specifičnom težinom. Među elementima koji su u čvrstom stanju na sobnoj temperaturi, samo još litij i kalij imaju manju gustoću. Na Mohsovoj skali tvrdoće, natrij ima vrijednost od 0,5[9], odnosno tako mehak da se može rezati nožem.
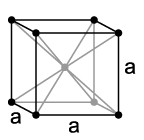
Natrij se, kao i drugi alkalni metali, kristalizira u kubičnom kristalnom sistemu u kubičnoj prostornoj centriranoj rešetki sa prostornom grupom i dvije formulske jedinice po jednoj elementarnoj ćeliji. Ispod temperature od 51 K on prelazi u heksagonalnu gustu kuglastu strukturu sa parametrom rešetke od a = 376 pm i c = 615 pm über.[7] Natrijeva para se sastoji iz pojedinih atoma metala, ali i dimera u obliku Na2. Na tački ključanja oko 16%[8] atoma se nalazi u obliku dimera. Para natrija je žute boje, a gledajući kroz nju nazire se i ljubičasta boja.
S kalijem gradi tečne smjese na sobnoj temperaturi u raznim opsezima koncentracija. Fazni dijagram pri 7 °C pokazuje peritektične otopljene spojeve Na2K i eutektičnu tačku na −12,6 °C sa sadržinom kalija od 77% po masenom udjelu.[10]

Hemijske[uredi | uredi izvor]
Kao i drugi alkalni metali, natrij je veoma neplemenit element (elektrodni potencijal: −2,71 V[8]) i vrlo lahko reagira sa brojnim drugim elementima, a jednim dijelom i sa spojevima. Reagira najlakše sa nemetalima, poput hlora i sumpora, vrlo burno, dajući ponekad i intenzivno žuti plamen. Kod posebno burne reakcije sa kisikom javlja se jedna posebnost. Natrij i kisik međusobno ne reagiraju bez prisustva vode na sobnoj temperaturi čak i pri zagrijavanju. U atmosferi bez prisustva vode ali uz prisustvo kisika, natrij se čak može i topiti, bez da reagira sa kisikom. Međutim, ako pri tome dođe u kontakt sa vlagom, vrlo lahko se zapali te nastaje natrij-peroksid.[8]
- reakcija natrija i kisika
Sa vodom natrij reagira tako što iz vode istiskuje vodik te gradi natrij-hidroksid. U alkoholima natrij gradi natrij alkoholate a iz njih također istiskuje vodik. Zbog velike reakcijske toplote, natrij u reakcijama se često topi. Ako se u reakciji pojavi natrij koji je u prahu, tako da se poveća reaktivna površina natrija, može doći i do eksplozije, a vodonik se može zapaliti. Ukoliko natrij dođe u kontakt sa spojevima koji u sebi sadrže hlor, kao što su dihlormetan, hloroform i tetrahlormetan, dolazi do stvaranja natrij-hlorida u brzoj i egzotermnoj reakciji.
- reakcija natrija i vode

Natrij se otapa u tečnom amonijaku daje plavu boju. Boja se javlja zbog oslobođenih elektrona, koje natrij otpušta u rastvoru. Na taj način, takav rastvor provodi električnu struju i blago je paramagnetičan.
Izotopi[uredi | uredi izvor]
Poznato je ukupno 15 izotopa i dva nuklearna izomera natrija počev od 18Na do 33Na.[11] Međutim, od njih samo jedan izotop 23Na se može naći u prirodi. Stoga je natrij jedan od 22 hemijska elementa koji imaju samo jedan stabilan izotop. Izotop sa najdužim vremenom poluraspada je 22Na čije vrijeme poluraspada iznosi 2,602 godina[11] a raspada se putem beta raspada i prelazi u 22Ne i 24Na koji se koristi u nuklearnoj medicini kao tracer. Svi drugi izotopi i nuklearni izomeri imaju vrlo kratka vremena poluraspada u intervalima od nekoliko sekundi ili milisekundi.
Rasprostranjenost[uredi | uredi izvor]

U poznatom svemiru, natrij je 14. po zastupljenosti hemijski element,[12] što se približno može uporediti sa rasprostranjenošću kalcija i nikla. U emitiranim svjetlosnim linijama mnogih svemirskih tijela, među njima i Sunca, moguće je detektirati i žute D-linije natrija. Na Zemlji, natrij je sadržan u Zemljinoj kori u približnom udjelu od 2,36%,[13] što ga stavlja na šesto mjesto najrasprostranjenijih elemenata na Zemlji. Međutim, zbog svoje velike reaktivnosti, ne pojavljuje se u elementarnom stanju. Među brojnim spojevima najviše su zastupljene soli natrija. Jedan od najvećih izvora natrijevih soli je morska voda. Jedan litar morske vode prosječno sadrži 11 grama iona natrija.[8]
Česti minerali natrija su albit, poznat i kao natronski feldspat sa formulom NaAlSi3O8 i oligoklas (Na,Ca)Al(Si,Al)3O8. Pored ovih minerala koji su sastavni dijelovi stijena iz grupe feldspata, natrij se također nalazi i u obliku velikih naslaga soli, naročito obične kuhinjske soli. Postoje ogromne zalihe natrij-hlorida (minerala halita, poznatog i kao kamena so). Pored nje, so se dobija i isušivanjem morske vode. One predstavljaju najvažniji izvor natrija i njegovih ostalih spojeva. Najpoznatiji rudnik kamene soli u Bosni i Hercegovini nalazi se u Tuzli, a duž obale Jadranskog mora nalaze se brojne solane. Kamene soli ima i u Njemačkoj, gdje su poznati rudnici u gradovima Salzgitter, Bad Reichenhall, Stade i Bad Friedrichshall. U obliku minerala nalazi se i u obliku alumosilikata NaAlSi3O8, čileanske šalitre (NaNO3), halita (NaCl) i kriolita Na3AlF6.
Pored natrij-hlorida, u prirodi se mogu naći i druge soli natrija. Tako naprimjer jedan od rijetkih prirodnih natrijevih minerala je i natrij-nitrat ili natronska salitra (Čileanska salitra) NaNO3. Zbog svoje dobre rastvorljivosti u vodi ona se može naći samo u posebno suhim područjima, kao što je pustinja Atacama u Čileu. Prije nego što je otkriven Haber-Boschov proces, čileanska salitra je bila osnovna sirovina za proizvodnju vještačkih đubriva i eksploziva. Natrij karbonat Na2CO3 se također može naći u velikim količinama u mnogim prirodnim materijalima. Najpoznatiji takav mineral je soda Na2CO3 · 10 H2O. Ona se kopa u industrijskim količinama a najvećim dijelom se koristi u proizvodnji stakla. Osim ovih, postoje brojni drugi minerali natrija. Jedan od poznatijih je kriolit (Na3[AlF6]), koji u istopljenom stanju služi, između ostalog, kao otapalo za aluminij oksid u procesu proizvodnje aluminija. Danas je poznato samo jedno mjesto gdje se u prirodi može naći kriolit na Grenlandu, tako da se kriolit uglavnom pravi vještački.
Dobijanje[uredi | uredi izvor]

Natrij se uglavnom dobija iz natrij hlorida, koji se dobija iz dva glavna izvora: rudnika kamene soli i isušivanjem rastvora koji sadrže so, kao što je morska voda. Samo jedan mali dio natrij hlorida se pretvara u elementarni natrij, dok se najveći dio koristi u ishrani kao kuhinjska so ili za proizvodnju drugih spojeva natrija. U tehničkom smislu, proizvodnja natrija se zasniva na procesu elektrolize suhog natrij hlorida u takozvanoj Downsovoj ćeliji (koju je 1924. godine patentirao James C. Downs). Za snižavanje tačke topljenja primjenjuje se eutektična smjesa soli sastavljena iz 60% kalcij hlorida i 40% natrij hlorida, koja se topi na 580 °C. U ovu smjesu ponekad se dodaje i barij hlorid. Pri elektrolizi primjenjuje se napon od oko 7 volti.[8] Za proizvodnju jednog kilograma natrija tokom elektrolize potroši se prosječno oko 10 kWh električne energije, a u ukupnom procesu proizvodnje oko 12 kWh.[14]
- Dobijanje natrija na katodi
- Dobijanje hlora na anodi
- ukupna reakcija
Cilindrična elektrolitična ćelija se sastoji iz jedne centralne anode sastavljene od grafita i okolnog katodnog prstena napravljenog od željeza. Iznad ćelije je zvono, u kojem se skuplja hlor i odvodi van. Natrij se sakuplja iznad katode i preko ohlađene cijevi izlazi izvan ćelije. U ovom procesu se dobija i kristalizirani kalcij i vraća se nazad u otopinu. Elektroliza natrij hlorida je zamijenila raniji Castnerov proces. U tom procesu se natrij dobijao putem elektrolize iz natrij-hidroksida. Iako je ovaj proces imao određene prednosti zbog niske tačke topljenja natrij hidroksida (318 °C), međutim trošilo se mnogo više električne energije. Od uvođenja hlor-alkalne elektrolize cijena natrija je drastično opala. Pri tom je natrij postao najskuplji lahki metal uopće. Njegova cijena uveliko zavisi od troškova električne energije i cijena hlora koji nastaje u tom procesu.
Upotreba[uredi | uredi izvor]

U svijetu se svakodnevno proizvedu ogromne količine natrij-hlorida i drugih spojeva natrija poput natrij-karbonata. Od toga se vrlo mali dio preradi u elementarni natrij. Najveći dio se direktno potroši ili se prerađuje u druge spojeve. Natrij je najviše upotrebljavani alkalni metal. On se koristi u različite tehničke i eksperimentalne svrhe. Iz jednog dijela natrija dobijaju se brojni drugi spojevi, između ostalih, sredstva za izbjeljivanje u koja se dodaje natrij-peroksid i jaka baza natrij-amid. Ovi spojevi se ne mogu naći u prirodi a također se ne mogu dobiti direktno iz natrij-hlorida. Iz natrija se dobijaju i natrij-cijanid i natrij-hidrid. Pošto natrij utiče na proces stvrdnjavanja, može se koristiti i kao dodatak aluminijsko-silicijskim legurama (proces oplemenjivanja po Aladar Paczu).
Katalizator[uredi | uredi izvor]
Natrij katalizira polimerizaciju 1,3-butadiena i izoprena. Zbog toga se on primjenjuje u proizvodnji vještačkog kaučuka.[15] Vještački materijal koji je dobijen sa natrijem kao katalizatorom, a koji se naziva buna, bio je prva vještačka guma na svijetu. Od 1937. godine takav materijal se proizvodio u takozvanim tvornicama bune (nazvanim tako po spoju 1,3-butadien i natriju) u gradiću Schkopau blizu Leipziga.[16]
Rashladno sredstvo[uredi | uredi izvor]
Pošto natrij ima toplotnu provodljivost od 140 W/m·K, što je daleko iznad čelika (15 do 58 W/m·K), te ima dobre osobine prenosa toplote kao i nisko talište a istovremeno i veliku temperaturni raspon u kojem je tečan, koristi se kao rashladno sredstvo za hlađenje ispusnih ventila u motorima sa sagorijevanjem gdje je su veliki termički zahtjevi. Pri tome se ventilski ispusti izvode šuplji da bi se napunili natrijem. Pri upotrebi, natrij se topi te se neprestano premješta između vruće i hladne strane. Time se odvodi toplota koja nastaje na crveno užarenim dijelovima ventila.
Također se i brzi oplodni reaktori hlade istopljenim natrijem. U takvim reaktorima se brzi neutroni nastali pri razbijanju jezgre atoma ne smiju usporavati između gorivih šipki kao što je to slučaj kod drugih tipova reaktora. Pri tome se ne smije koristiti voda za hlađenje, koja služi kao sredstvo za usporavanje (moderator). Zatim se toplota dalje prenosi preko sekundarnog kruga natrija dalje za stvaranje pare koja pokreće turbine.[17]
Svjetiljke[uredi | uredi izvor]
Svjetiljke sa natrijevim parama koriste karakterističnu žutu svjetlost, koju isijavaju pare natrija pri električnom pražnjenju. Često se koriste za javnu rasvjetu zbog dobre iskoristivosti električne energije.
Redukcijsko sredstvo[uredi | uredi izvor]
Neki metali, poput titanija, tantala i uranija se ne mogu dobiti putem reakcije redukcije sa ugljikom, pošto se tim reakcijama dobijaju veoma stabilni karbidi koje je teško odvojiti. Pored nekih elemenata koji se upotrebljavaju u tu svrhu, naročito aluminija i magnezija, vrlo često se kao redukcijsko sredstvo koristi i natrij. Osim navedenih, natrij se koristi i za proizvodnju kalija. Pošto je kalij vrlo neplemenit element, on se ne može dobiti putem redukcije sa ugljikom. Teoretska mogućnost je njegova proizvodnja putem elektrolize, ali u tehničkom smislu taj proces nije moguć zbog dobre rastvorljivosti kalija u otopljenom kalij-hloridu.
Natrij ima vrlo važnu ulogu kao redukcijsko sredstvo u organskim sintezama. Dugo vremena najznačajnija tehnička upotreba natrija bila je proizvodnja tetraetil olova iz hlor etana. On je bio vrlo važno sredstvo koje je služilo u benzinskim motorima za sprječavanje udara u motoru (kao antidetonator). Međutim iz ekoloških razloga, proizvodnja tetraetil olova je znatno smanjena a negdje i zabranjena. Time je i potrošnja natrija također smanjena. Natrij se koristi i u drugim sličnim reakcijama kao naprimjer u Birchevoj redukciji i pinakol kuplovanju.[18] Međutim, ove reakcije su značajne samo u laboratorijske svrhe.
Sredstvo za sušenje[uredi | uredi izvor]
Pošto natrij reagira sa vodom čak i u tragovima, svježe presovana žica od natrija se može koristiti kao sredstvo za sušenje organskih otapala poput dietil etera ili toluola. Ova metoda nije moguća za otapala koja sadrže halogene elemente kao što su hloroform i metilen hlorid, jer sa njima natrij reagira veoma burno. Legure natrija i kalija na sobnoj temperaturi su u tečnom stanju. One služe za prenos toplote kao i za dehalogeniziranje u organskim sintezama. Na-K je zgodna i za sušenje već dobro osušenih otapala, da bi se dobila posebno dehidrirana otapala.
Spojevi[uredi | uredi izvor]
Spojevi natrija je od ogromnog komercijalnog značaja, djelimično su osnova industrije stakla, papira, sapuna i tekstila.[19] Među najznačajnije spojeve natrija ubrajaju se natrij hlorid (obična, kuhinjska so) (NaCl), natrij-karbonat (Na2CO3), natrij bikarbonat (soda bikarbona, NaHCO3), natrij-hidroksid (kaustična soda, NaOH), natrij-nitrat (NaNO3), di- i trinatrij fosfati, natrij-tiosulfat (Na2S2O3·5H2O) i boraks (Na2B4O7·10H2O)[20] U svojim spojevima, natrij je obično u ionskoj vezi vezan sa vodom i anionima, i smatra se kao jaka Lewisova kiselina.[21]

Većina sapuna su soli natrija masnih kiselina. Natrijevi sapuni su tvrđi od kalijevih i imaju višu tačku topljenja.[20] Natrij hlorid se često koristi i za odleđivanje asfaltnih površina i kao dodatak za zaštitu prehrambenih namirnica od propadanja. Natrij bikarbonat se najčešće koristi za kuhanje. Zajedno sa kalijem, mnogim važnim lijekovima se dodaje natrij za poboljšanje njihove biološke dostupnosti (biodostupnost), mada je u tom pogledu mnogo bolji kalijev ion, natrij se često bira zbog svoje niže cijene koštanja i manje atomske težine.[22] Natrij hidrid se koristi kao baza za mnoge reakcije (kao što je aldol reakcija) u organskoj hemiji i kao redukcijsko sredstvo u neorganskoj hemiji.[23]
Do danas je ukupno poznato pet oksida natrija. To su natrij oksid Na2O, natrij-peroksid NaO2, dinatrij-trioksid Na2O3, natrij-hiperoksid NaO2 i natrij-trioksid NaO3. Natrij oksid je sastojak u mnogim vrstama stakla, a nastaje u izradi stakla iz natrij karbonata. Nastaje pri sagorijevanju natrija na samo određenim temperaturama (150–200 °C[8]) i stehiometrijski dodanim količinama natrija i kisika. U suprotnom, natrij sagorijeva do natrij peroksida. On je jako oksidacijsko sredstvo i u tehničkom smislu najznačajniji oksid natrija. Koristi se kao sredstvo za izbjeljivanje tekstila i papira kao i izvor kisika za ronjenje i u podmornicama. Ostali oksidi natrija su dosta nestabilni i vrlo brzo se raspadaju. Natrij-hidroksid (NaOH) je za industriju jedna od najvažnijih baza. Vodeni rastvor natrij hidroksida se naziva natronska lužina. Između ostalog, ona se koristi za pravljenje sapuna i boja kao i za preradu boksita u proizvodnji aluminija.
Druga jedinjenja natrija su:
Organonatrijski spojevi[uredi | uredi izvor]

Dobijeni su mnogi organonatrijski spojevi. Zbog velike polarnosti C-Na veza, oni se ponašaju kao izvor karbaniona (soli sa organskim anionima). Neki od poznatijih derivata uključuju natrij-ciklopentadienid (NaC5H5) i tritil-natrij ((C6H5)3CNa).[24]
Biološki značaj[uredi | uredi izvor]

Natrij je jedan od elemenata koji su neophodni (esencijalni) za sve životinjske organizme. U njima je natrij, zajedno sa hlorom devet najčešći element, i pored kalcija i kalija, predstavlja treći po zastupljenosti neorganski ion. Time se on fiziološki ubraja u makroelemente. U živim organizmima, natrij se javlja u obliku Na+ iona. U ljudskom tijelu, ako se uzme prosječna masa tijela od oko 70 kg, ima oko 100 g natrija u vidu Na+ iona.[25] Od toga dvije trećine otpada na NaCl a jedna trećina na NaHCO3. Pošto on u ljudskom tijelu čini oko 90% vanćelijskih elektrolita, koncentracija natrija određuje zapreminu međućelijskih i krvnih sudova te zapreminu međućelijskih tekućina.[26]

Preporučene minimalne količine natrija za čovjekov organizam, po preporukama njemačkog udruženja za ishranu, iznose oko 550 mg/dnevno za odraslu osobu.[27] Američki centar za kontrolu i prevenciju bolesti navodi da je čovjeku neophodno samo 350 mg natrija dnevno.[28] Druge slične organizacije daju i preporuke za najveću količinu natrija. Tako naprimjer Svjetska zdravstvena organizacija (WHO) daje preporuku da najviši dnevni unos natrija u ljudski organizam ne treba da premaši 2 grama,[29] dok Američko udruženje za srce (AHA) taj iznos ograničava na maksimalno 1,5 grama dnevno.[30] Međutim, stvarni dnevni unos natrija iznosi daleko iznad ovih preporučenih vrijednosti. Uzrok tome je relativno veliki dnevni unos kuhinjske soli (2,5 g soli u sebi sadrži oko 1 g natrija). Prema istraživanja instituta Max Rubner, muškarci prosječno dnevno unesu u organizam oko 3,2 grama natrija, dok je kod žena prosjek oko 2,4 grama dnevno.[31] Pretpostavlja se da unos natrija često prelazi ove vrijednosti, jer su ova istraživanja bazirana na intervjuima sa ispitivanim osobama. U drugim studijama WHO, prosječno izlučivanje natrija putem urina kod muškaraca u Njemačkoj iznosilo je 4,1 do 4,5 grama dnevno, a 2,7 do 3,5 grama kod žena.[32]
U organizmima ioni natrija Na+ nisu ravnomjerno raspoređeni. Kao i kod drugih iona, njihova koncentracija unutar i izvan ćelije su dosta različite. Ove koncentracije iona Na+ i iona hlora Cl− (uglavnom izvan ćelije), kalija K+ kao i organskih aniona (uglavnom unutar ćelije) značajno određuju uslove potencijala membrane živih ćelija. Ovaj potencijal membrane i ionski gradijenti su od životnog značaja za većinu ćelija. Pošto malehni anorganski ioni neprestano odlaze u okolna područja zbog razlika u koncentracijama, istovremeno se odvija drugi aktivni proces u obrnutom smjeru. Najvažniju ulogu pri tome igra takozvana natrij-kalij pumpa koja neprestano povratno djeluje trošeći energiju Na+- i K+ iona.[33]
Na+ ioni igraju važnu ulogu pri stvaranju i provođenju podražaja u nervnim ćelijama (i mišićnim vlaknima). Na postsinapsama nervnih ćelija (i na neuromuskularnim završecima mišića) nalaze se posebni receptori, koji se otvaraju nakon aktiviranja od strane prenosnih materija (neurotransmitera) a koje otpušta prethodna nervna ćelija koja je nadražena, te tako postaju propusni za ione natrija. Stvara se struja natrija koja lokalno mijenja osnovno stanje stabilnih potencijala membrane ćelije. Unutrašnost postaje manje negativna u odnosu na vanjski dio, što se naziva depolarizacija. Ako je ova depolarizacija na svom putu do aksona dovoljna jaka, dolazi do otvaranja druge vrste natrijevog kanala. Tada se radi o natrijevim kanalima aksona koji su zavisni od napona, a koji lokalnu depolarizaciju, zajedno sa drugim ionskim kanalima, provode dalje u određenom ritmu otvaranja i zatvaranja. Na aksonima nervnih ćelija nastaje trajni naponski talas, takozvani akcijski potencijal. Kod vraćanja na osnovno stanje, glavnu i osnovnu ulogu ponovno ima natrij-kalij pumpa.[33]
U biljkama[uredi | uredi izvor]
Za razliku od čovjeka, natrij u biljkama igra manje važnu ulogu. Dok je kalij esencijalan za sve biljke i većinu mikroorganizama, natrij je potreban za život i rast samo nekih C4- i CAM-biljaka, dok ga po pravilu C3 biljke ne trebaju. Prema određenom staništu, ipak su se razvile nezavisne biljke koje profitiraju od uzimanja natrija iz zemljišta. Takve biljke, nazvane halofiti, naročito dobro rastu u obalnim područjima i područjima gdje u zemljištu postoji visoka koncentracija natrija.
Halofiti kao što su kupus, šećerna repa i mnoge C4 trave dobro podnose so, tako da mogu transportirati natrij iz centralnog cilindra u vakuole ćelija lišća, gdje on kao ion osmotski djeluje za povećanje turgora (pritiska u ćeliji) te na taj način umjesto kalija pozitivno utječe na izduženje ćelija i rast površine lista. Na taj način natrij jednim dijelom zamjenjuje kalij, a drugim djeluje na dodatni rast.
Međutim, one biljke koje nisu u stanju transportirati natrij iz centralnog cilindra u ćelije lista, akumuliraju ga u ksilemski parenhim. Takve biljke nazivaju se natrofobi, gdje, između ostalih, spadaju kukuruz i niske sorte graha.
Reference[uredi | uredi izvor]
- ^ Harry H. Binder (1999). Lexikon der chemischen Elemente. Stuttgart: S. Hirzel Verlag. ISBN 3-7776-0736-3.
- ^ N. Greenwood; A. Earnshaw (1988). Chemie der Elemente (1 izd.). Weinheim: VCH. str. 97. ISBN 3-527-26169-9.CS1 održavanje: više imena: authors list (link)
- ^ a b David R. Lide, ured. (2003). CRC Handbook of Chemistry and Physics (84 izd.). Boca Raton, Florida: CRC Press. ISBN 978-1-4200-7483-3.
- ^ a b Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. u: Journal of Chemical & Engineering Data. 56, 2011, str. 328–337, doi:10.1021/je1011086
- ^ a b Mineralienatlas: Natrium
- ^ David Stifter: Hallstatt – In eisenzeitlicher Tradition? Arhivirano 21. 2. 2014. na Wayback Machine (PDF;). u: Interpretierte Eisenzeiten. Fallstudien, Methoden, Theorie. Tagungsbeiträge der 1. Linzer Gespräche zur interpretativen Eisenzeitarchäologie. Hrsg. Raimund Karl, Jutta Leskovar (= Studien zur Kulturgeschichte von Oberösterreich 18), Linz: Oberösterreichisches Landesmuseum 2005, str. 229–240.
- ^ a b K. Schubert: Ein Modell für die Kristallstrukturen der chemischen Elemente. u: Acta Crystallographica, 1974, B30, str. 193–204; doi:10.1107/S0567740874002469
- ^ a b c d e f g h Holleman-Wiberg (2007). Lehrbuch der Anorganischen Chemie (102 izd.). Berlin. ISBN 978-3-11-017770-1.
- ^ natrij na webelements.com, fizičke osobine
- ^ van Rossen, G.L.C.M.; van Bleiswijk, H.: Über das Zustandsdiagramm der Kalium-Natriumlegierungen. u: Z. Anorg. Chem., 1912, 74, str. 152–156; doi:10.1002/zaac.19120740115.
- ^ a b G. Audi, O. Bersillon, J. Blachot, A. H. Wapstra: The Nubase evaluation of nuclear and decay properties Arhivirano 23. 9. 2008. na Wayback Machine (PDF)
- ^ A. G. W. Cameron: Abundances of the elements in the solar system. u: Space Science Reviews, 1970, 15, str. 121–146; doi:10.1007/BF00172440
- ^ K. H. Wedepohl: The composition of the continental crust. u: Geochimica et Cosmochimica Acta, 1995, 59, 7, str. 1217–1232; doi:10.1016/0016-7037(95)00038-2
- ^ Zusammenfassung über Alkalimetalle von wiley-vch (PDF)
- ^ K. Ziegler, F. Bersch; H. Wollthan (1934). "Untersuchungen über alkaliorganische Verbindungen. XI. Der Mechanismus der Polymerisation ungesättigter Kohlenwasserstoffe durch Alkalimetalle und Alkalialkyle". Justus Liebigs Annalen der Chemie. 511 (1): 13–44. doi:10.1002/jlac.19345110103.CS1 održavanje: više imena: authors list (link)
- ^ Deutsches Chemie-Museum Merseburg, Geschichte der Busa-Werke Schkopau
- ^ M. Volkmer (1996). Basiswissen Kernenergie. Hamburgische Elektricitäts-Werke-AG. str. 52–53. ISBN 3-925986-09-X.
- ^ R. Brückner (2004). Reaktionsmechanismen (3 izd.). Spektrum Akad. Verlag. ISBN 3-8274-1579-9.
- ^ Alfred Klemm, Gabriele Hartmann, Ludwig Lange, "Sodium and Sodium Alloys" u Ullmann's Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a24_277
- ^ a b Holleman Arnold F.; et al. (1985). "Natrium". Lehrbuch der Anorganischen Chemie (jezik: njemački) (91–100 izd.). Walter de Gruyter. str. 931–943. ISBN 3-11-007511-3. Eksplicitna upotreba et al. u:
|author=(pomoć) - ^ Cowan James A. (1997). Inorganic Biochemistry: An Introduction. Wiley-VCH. str. 7. ISBN 978-0-471-18895-7. OCLC 34515430.
- ^ Remington Joseph P. (2006). Remington: The Science and Practice of Pharmacy (21 izd.). Lippincott Williams & Wilkins. str. 365–366. ISBN 978-0-7817-4673-1.
- ^ Wiberg Egon; et al. (2001). Inorganic Chemistry. Academic Press. str. 1103–1104. ISBN 978-0-12-352651-9. Eksplicitna upotreba et al. u:
|author=(pomoć) - ^ Renfrow, Jr., W. B.; Hauser, C. R. (1943): "Triphenylmethylsodium". Org. Synth.; Coll. vol. 2, str. 607 doi:10.15227/orgsyn.019.0083
- ^ W. Kaim, B. Schwederski (2005). Bioanorganische Chemie (4 izd.). Wiesbaden: Teubner. ISBN 3-519-33505-0.
- ^ Deetjen, P., Speckmann, E.-J., & Hescheler, J. (2005). Physiologie. München: Elvesier GmbH.
- ^ Deutsche Gesellschaft für Ernährung e.V. Referenzwerte für die Nährstoffzufuhr Arhivirano 11. 11. 2014. na Wayback Machine. 13.12.2013.
- ^ So ili natrijum hlorid najveći ubica današnjice! Arhivirano 12. 6. 2013. na Wayback Machine www.b92.net
- ^ World Health Organization Global Strategy on Diet, Physical Activity and Health. Population sodium reduction strategies. 13.12.2013.
- ^ American Heart Association The American Heart Association’s Diet and Lifestyle Recommendations. 13.12.2013.
- ^ Max Rubner-Institut, Bundesforschungsinstitut für Ernährung und Lebensmittel Nationale Verzehrsstudie II. Ergebnisbericht Teil 2. Die bundesweite Befragung zur Ernährung von Jugendlichen und Erwachsenen. Arhivirano 28. 12. 2013. na Wayback Machine. (PDF)
- ^ Elliott P, Brown I (2006) Sodium intakes around the world. Background document prepared for the Forum and Technical meeting on Reducing Salt Intake in Populations (Pariz 5-7.10.2006.). (PDF)
- ^ a b Müller-Esterl (2004). Biochemie. Eine Einführung für Mediziner und Naturwissenschaftler. Spektrum Akademischer Verlag. ISBN 3-8274-0534-3.
Vanjski linkovi[uredi | uredi izvor]
| Sodium na Wikimedia Commonsu. |
- EnvironmentalChemistry.com – Natrij[mrtav link]
- sodium
- sodium (natrium)
- Natrijum–naš svakodnevni saputnik
- Radiochemistry of elements Arhivirano 2. 6. 2013. na Wayback Machine
Literatura[uredi | uredi izvor]
- Mary Elvira Weeks (2003). Discovery of the Elements. Kessinger Publishing. str. 433–457. ISBN 9780766138728.
- Natrium u: Gmelins Handbuch der anorganische Chemie, 8. izd.; System-Nummer 21 (1928).










