Perioda periodnog sistema elemenata
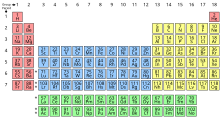
Pod pojmom periode periodnog sistema elemenata[1] podrazumijeva se u hemiji svaki red tabele periodnog sistema hemijskih elemenata.[2] Brojevi perioda od 1 do 7 odgovaraju glavnim kvantnim brojevima, a kojima se još dodaju i slovne oznake periode K do Q prema ljuskama atomskog modela ljusaka.
Izuzev prve periode, koja sadrži samo elemente vodik i helij, svaka perioda sadrži osam glavnih grupa elemenata. Od 4. periode (uključujući i nju) naviše, postoji još deset sporednih grupa elemenata. Šesta perioda sadrži još i dodatnih 14 elemenata koji se nazivaju lantanoidi, dok 7. perioda također sadrži 14 dodatnih elemenata koji se nazivaju aktinoidi.
| Perioda | Elektroni | Elementi | Napomene | |||||
|---|---|---|---|---|---|---|---|---|
| Glavni kvantni broj |
Ljuska | Orbitala/ Blokovi |
Glavne grupe |
Sporedne grupe |
Dodatne grupe | |||
| s-blok | p-blok | d-blok | f-blok | g-blok | ||||
| 1 | K | s | 2 | |||||
| 2 | L | s, p | 2 | 6 | ||||
| 3 | M | s, p | 2 | 6 | ||||
| 4 | N | s, p, d | 2 | 6 | 10 | |||
| 5 | O | s, p, d | 2 | 6 | 10 | |||
| 6 | P | s, p, d, f | 2 | 6 | 10 | 14 | ||
| 7 | Q | s, p, d, f | 2 | 6 | 10 | 14 | ||
| 8 | s, p, d, f, g | 2 | 6 | 10 | 14 | 18 | još nije otkriven niti jedan element | |
Pravila i zakonitosti[uredi | uredi izvor]
Unutar neke periode, po pravilu, atomski radijusi elemenata opadaju s lijeva na desno dok istovremeno raste elektronegativnost, dok broj pozitivno nabijenih protona u atomskom jezgru raste a s tim u neutralnim atomima također raste i broj negativno nabijenih elektrona u atomskoj ljusci. Korištenjem atomskog modela ljusaka, smatra se da se elektronske ljuske popunjavaju istim redoslijedom, dok noviji modeli atoma kao što je npr. model orbitala predviđa da se istim redoslijedom zauzimaju odgovarajuće atomske orbitale.
Promjene broja atomskih čestica u atomu unutar neke periode uzrokuje i različite osobine hemijskih elemenata unutar periode:
- promjene u broju osnovnih čestica u atomskom jezgru utječe uglavnom na različite fizičke osobine elemenata
- broj i mjesto elektrona u atomskom omotaču utječe najviše na razlike u hemijskim osobinama elemenata.
Reference[uredi | uredi izvor]
- ^ "Groups and Periods of the Periodic Table of the Elements Explained | Britannica". www.britannica.com (jezik: engleski). Pristupljeno 2023-08-24.
- ^ Maziek, Rylie (2021-03-23). "How to Read the Periodic Table | Groups & Periods". ChemTalk (jezik: engleski). Pristupljeno 2023-08-24.
