Karbonat
Ovaj članak ili neki od njegovih odlomaka nije dovoljno potkrijepljen izvorima (literatura, veb-sajtovi ili drugi izvori). |
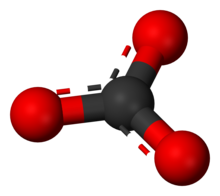
Karbonati su soli i estri ugljične (karbonske) kiseline (H2CO3). Od dvoprotoniziranih (dvobrojnih) soli izvode se dvije vrste soli i to: hidrogenkarbonati, koji se također nazivaju i primarni karbonati, sa općom formulom MIHCO3 te sekundarni karbonati sa općom formulom MI2CO3. Sekundarni karbonati zasnivaju se na dvostruko negativno nabijenom karbonatnom ionu CO32−.
Ester ugljične kiseline sa općom strukturnom formulom R1−O−C(=O)−O−R2, pri čemu su R1 i R2 alkil- i aril ostaci koji sadrže ugljik, također se nazivaju karbonati i svrstavaju se pod estre ugljične kiseline. Polimerni karbonati imaju opću strukturnu formulu (O−R−O−C(=O)−)n i ubrajaju se u polikarbonate. Od ortougljične kiseline (C(OH)4) koja ne postoji u slobodnom obliku izvode se estri ortougljične kiseline sa strukturnom formulom C(OR)4.
Karbonat ion je konjugirana baza od hidrogenkarbonatnog iona, odnosno karbonatne kiseline H2CO3. Karbonatni anioni vrše važnu funkciju u fiziologiji živih ćelija, npr. regulacija kiselinsko-bazne ravnoteže (hidrogenkarbonatni pufer), razmjena gasova, itd.
Najpoznatiji karbonat u prirodi je kalcijum karbonat, poznat i kao kreda, krečnjak i mermer.
Također pogledajte[uredi | uredi izvor]
Vanjski linkovi[uredi | uredi izvor]
| Commons ima datoteke na temu: Karbonat |
- BME 403: Respiratorni odjeljak na usc.edu.
- "Je li H2CO3 (ugljična kiselina) rastvorljiva ili nerastvorljiva u vodi?" na chemistry.stackexchange.com.

