Glavni kompleks histokompatibilnosti

Glavni kompleks histokompatibilnosti (MHC) je skup molekula na površini ćelija, kodiranih velikom porodicom gena koja kontrolira glavni dio imunog sistema svih kičmenjaka. MHC molekule posreduju u interakcijama leukocita pa se također nazivaju i leukocitnim. Te molekule su osnova imuniteta i skupa sa leukocitima i ostalim ćelijama čine imuni sistem organizma. MHC određuje i kompatibilnost donora za transplantaciju organa kao i podložnost na autoimmune bolesti preko unakrsne imunizacije. Kod ljudi, MHC se naziva ljudski leukocitni antigen (HLA, skr. od human leucocyte antigen)
Dakle, na površini svake ćelije nalaze se molekule koje su jedinstvene za svaku osobu. Putem molekula glavnog kompleksa histokompatibilnosti, tijelo može razlikovati sopstvene i strane supstance. Sve ćelije koje imaju iste molekule glavnog kompleksa histokompatibilnosti ne izazivaju imuni odgovor, a odbacuje se svaka ćelija koja nosi drugačije molekule glavnog kompleksa histokompatibilnosti.
Ćelije imunološkog sistema, između ostalih, imaju i memorijske sposobnosti pa mogu da “nauče” razlikovati vlastito od stranog. Još u fetusnoj fazi ontogeneze, kada počinje razvoj imunog sistema, matične ćelije odlaze u timus, gdje se dijele i razvijaju u T-limfocite. U daljoj fazi, unutar timusa, svaki T limfocit koji reagira na sopstvene molekule glavnog kompleksa histokompatibilnosti timusa, biva odstranjen. Svim T limfocitima koji podnose glavni kompleks histokompatibilnosti timusa i budu kompatibilne sa ćelijama koje izražavaju jedinstvene tjelesne MHC molekule, podobne su za sazrijevanje, tj. biva im "dozvoljeno" da sazriju i napuste timus.
Svaka MHC molekula na ćelijskoj površini ispoljava osobenu molekulsku frakciju proteina zvanu epitop.[1] Ispoljeni antigen može biti self ili nonself. U suštini, MHC kompleks je kao mjerilo koje odražava ravnotežu bjelančevina unutar ćelije.[2][3]
Proteini[uredi | uredi izvor]
MHC proteinI imaju [structure koje liče na imunoglobulin, a uključeni su u tri klase.
Klasa I[uredi | uredi izvor]
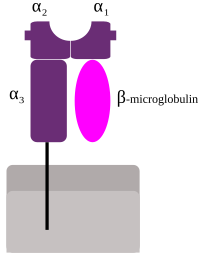
MHC I javlja se kao α lanac sastavljen od tri domena-α1, α2, i α3. α1 počiva na jedinici ne-MHC molekuli β2 mikroglobulina, koji je kodiran ljudskog hromosoma 15. Alfa-3 (α3) podjedinica je transmembrana za zadržavanje sidrenja molekula ‘’MHC klase I na ćelijskoj membrani. Peptid se prezentira držanjem pri dnu peptid-vezujućih žlijebova u centralnom području α1 / α2 heterodimera (molekula koja sastoji od dva neidentične podjedinice). Genetičko kodiranje i ekspresija [aminokiselina]], redoslijed ostataka peptid-vezujućih utora na dnu, određuje koji posebni peptidni ostatak ga veže.
Klasične MHC molekule imaju epitope za TCR u CD8+T limfocitima. Neklasične molekule (MHC klasa IB) ispoljava ograničeni polimorfizam svojih osobenosti I prezentiranih antigena. Ova grupa je podijeljena u grupu koja kodira produkte unutar MHC lokusa (tj. HLA-E, -F, -G), a može i nemati takvu ulogu, tj. samostalno inducirani antigeni (stres ligandi), kao što su ‘’ULBPs, Rae1, and H60); antigen/ligandi mnogih ovih molekula je nepoznati, ali svaki može međureagirati sa svakim od CD8+ T, NKT i NK ćelija.
Klasa II[uredi | uredi izvor]
MHC molekule klase II su formirane od dva lanca, α i β, od kojih svaki ima dvije domene-α1 i α2 i β1 i β2-svaki lanac ima zasebne transmembranske domene, α2 i β2, pridržavajući molekule MHC klase II za ćelijske membrane. Kod čovjeka, molekule MHC klase II imaju 5-6 isotipova. Klasične molekule predstavljaju i peptide za CD4 + limfociti. Neklasične molekule, dodatne, sa unutarćelijskim funkcijama, nisu ispoljene na ćelijskim membranama, već u unutrašnjim membranama u lizosomima, obično noseći antigene peptide na klasične molekule MHC klase II .
Klasa III[uredi | uredi izvor]
Molekule klasa III, za razliku od onih iz klasa I i II, imaju fiziološke uloge ali su kodirane sa hromosomskog segmenta između njih, u kratkom kraku hromosoma l6. Ove molekule uključuju nekoliko i izlučevinskih proteina sa imunim funkcijama: komponente dopune sistema (kao što C2 , C4 i B faktor), citokina (kao što su TNF-α, LTA i LTB) i proteini toplinog šoka.[4][5]
Antigeni histokompatibilnosti[uredi | uredi izvor]

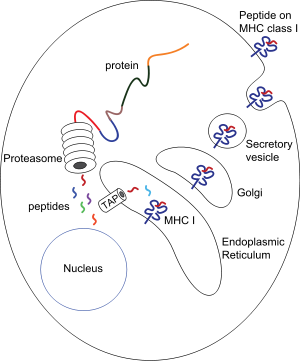
Proteini se degradiraju u citosolu pomoću proteasoma (velikog proteinskog kompleksa), oslobađajući peptide ugrađene pomoću TAP kanala u endoplazmatskom retikulumu.
Tu su asocirani sa svježe sintetiziranim MHC I molekulama.
MHC-I/peptid kompleks ulazi u Golgijev aparat, glikozilira, ulazi u sekretorne vezikule, fuzira sa plazma membranom.
Taj kompleks izlazi iz ćelije pri čemu na samoj membrane interreaguje sa T limfocitima.
Antigeni histokompatibilnosti (tkivne snošljivosti, tkivne podudarnosti) su glikoproteinske makromolekule ćelijskih membrana – koje kod organizma primatelja, ukoliko ih sam ne posjeduje, izazivaju imunološku reakciju kojom strani nosilac (ćelija, tkivo, organ) nedgovarajuće specifičnosti biva uništen (odbačen). Imunološki je relevantna samo prva kategorija jakih antigena, a determiniraju je geni glavnog kompleksa histokompatibilnosti (Major Hystocompatibility Complex – MHC; Major Hystocompatibility System – MHS). Njihova osnovna prirodna biološka funkcija nije, dakle, sprečavanje transplantacije, nego regulacija imunološke reakcije na invadirane proteinske molekule stranog porijekla (bakterije, gljivice, virusi, tumorski antigeni itd). MHC je genetički determiniran skupinom blisko vezanih lokusa, od kojih glavninu čini HLA sistem, imenovan po tome što su prvi antigeni ovog sistema (HLA–A, HLA–B i HLA–C) otkriveni na humanim (H – human) leukocitima (L – leucocyte) i prvoopisanom lokusu (A). U primarne analize MHC genske mape uključeni su genetički markeri već poznate unutarhromosomske lokacije, kao što su:
1. izoenzimski sistemi:
- eritrocitna fosfoglukomutaza 3 (PGM3),
- mokraćni pepsinogen 5 (PG5),
- glikoksalaza I (GLO I),
- indol–fenoloksidaza – B (IPO–B) ili superoksid dismutaza 2 (SOD 2),
- maleinska kiselina (ME1),
2. sistemi eritrocitnih antigena (krvnih grupa):
- P,
- Chido (Ch),
- Rodgers (Rg), i
3. faktori komplementarnog sistema:
- properdinski faktor B (Bf)
– proaktivator C3 komponente komplementa,
- C2 komponenta komplementa,
- C4 komponenta komplementa.
MHC sadrži genske lokuse koji kontroliraju produkciju:
- (1) tkivnih antigena (HLA–A, HLA–B, HLA–C);
- (2) determinatora specifične imunološke reaktivnosti (Ir);
- (3) faktora interakcije pomiješanih leukocita (HLA–D);
- (4) antigena vezanih za imunološki odgovor (HLA–DR);
- (5) nekih komponenti komplementarnog sustava (C2 i C4, te Bf–proaktivator C3);
- (6)nekih eritrocitnih antigena (P, Chido i Rodgers sistemi).
Drugim riječima, individualnu specifičnost MHC–a (glavnog histokompatibilnog kompleksa) determinira skupina gena, usko povezanih lokusa, odgovornih za sintezu proteinskih molekula, koje prepoznaju limfociti T u imunološkoj reakciji na strane antigene. Te molekule se mogu svrstati u četiri osnovne skupine (klase):
- (1) supstance koje citotoksični limfociti T mogu identificirati,
- (2) produkti koje pomoćni limfociti T (tvari heterogenih seroloških svojstava, tkivne distribucije i biohemijske strukture), prepoznaju te
- (3) neke komponente komplementa i
- (4) ostale supstance.[6][7]
| Klasa | Kodiranje | Ekspresija |
| MHC klasa I | (1) peptid-vezujući proteini koji biraju kratke sekvence aminokiselina za antigensko ispoljavanje, kao i (2) molekule koje pomažu procesuiranje antigena (kao što su transporter vezan sa procesuiranjem antigena: TAP i tapazin). |
Jedan lanac, zvani α, čiji je ligand CD8 receptor— posebno od T ćelija— i inhibicijski receptori NK ćelija |
| MHC klasa II | (1) peptid-vezujući proteini i (2) proteini koji pomažu unošenje antigena antigen na peptid-vezujuće proteine MHC klase II (kao što su MHC II DM, MHC II DQ, MHC II DR, i MHC II DP). |
Dva lanca, zvana α i β, čiji su ligandi CD4 receptori helper T ćelija. |
| MHC klasa III | Ostali imuni proteini, van procesuiranje i ispoljavanje kao š su komponente komplementne kaskade (tj., komplementne komponente C2 i C4, komplementni faktor B, citokini imune signalizacije (tj. TNF-α), i proteini toplotnog šoka i bufer ćelije stresova | Nekoliko |
| Karakter | MHC-I | MHC-II |
|---|---|---|
| Kompozicija ostabilnog peptidno-MHC kompleksa | Polimorfni lanac α i β2 mikroglobulina, peptidna veza sa α lancem | Polimorfni lanci α i β, obostrana peptidna veza |
| Tipovi antigen prezentirajućih ćelija (APC) | Sve ćelije sa jedrom | Dendritske ćelije, mononukleusni fagociti, B limfociti, neke endotelske ćelije, epitel timusa |
| T limfociti sa sposobnošću odgovora | Citotoksični T limfociti (CD8+) | Helper T limfociti(CD4+) |
| Porijeklo antigenskih proteina | Citosolnu proteini (pretežno sintetizirani u ćeliji; također mogu ući iz vanćelijske sredine preko fagosomama | Proteini koji su prisutni u endosomima ili lizosomima (pretežno potiču iz vanćelijske sredine) |
| Enzimi koji su odgovorni za generiranje peptida | Citosolski proteasomi | Proteaze iz endosoma i lizosoma (naprimjer, katepsin) |
| Lokacija nošenja peptida na MHC molekuli | Endoplazmatski retikulum | Specijalizirani mjehurasti odjeljak |
| Molekule koje učestvuju u transportu peptida i njihovog postavljanja na MHC molekule | Transporter koji je u vezi sa procesuiranjem antigena (TAP – transporter associated with antigen processing) | DM, nevarijantni lanac |
Porijeklo i evolucija diverziteta MHC alela[uredi | uredi izvor]
Porijeklo i evolucija diverziteta MHC alela privlače osobitu pozornost, kako u naučno–fundamentalnom, tako i u aplikativnom smislu. Nema pouzdanih egzatnih saznanja o primordijalnom MHC genu. Prema jednoj od više hipoteza, klasa II MHC–a je evoluirala prva, dok je – prema drugima – takvu poziciju imala klasa I, kao rezultat rekombinacije gena sličnim onim za C–domenu imunoglobulina i domenu HSP70 (heat–shock) proteina koja je odgovorna za interakciju peptida. Filogenetske analize ukazuju na određene relacije između klase II MHC –lanca i beta –2–mikroglobulina, kao i između klase II MHC –lanca i klase I –lanca.
Više takvih i sličnih dokaza potvrđuju hipotezu da su predačke MHC molekule imale strukturu sličnu recentnoj klasi II i da je ona bila osnova za evoluciju molekula klase I. Međutim, to još uvijek ne može objasniti molekularnu prirodu izvornog MHC gena. Evidencije prisustva gena iz klasa I, II i III kod nekih amfibija (Xenopus) ukazuju na stalno prisustvo fizičke povezanosti MHC–a vjerovatno tokom proteklih 370 miliona godina ili čak i duže.
Poznato je da su MHC lokusi visoko polimorfni kod ljudi, miša, a i dugih sisara. Heterozigotnost u navedenim kategorijama iznosti 80–90%. Postoje četiri hipoteze koje objašnjavaju takav visok stupanj polimorfizma:
- visoka mutaciona rata;
- genska konverzija ili interlokusna genetička razmjena;
- balansirana selekcija;
- frekvencijski–zavisna selekcija.
Distribucija polimorfizama sekvenci gena klase I kod čovjeka i miša je dokaz za četiri koordinirana faktora, koja mogu doprinijeti razumijevanju bogatstva alelnog diverziteta koji karakterizira MHC. To podrazumijeva:
- stupnjevita evolucijsku kumulaciju spontanih mutacionih supstitucija (nukleotidnih supstitucija ili tačkastih mutacija), ali bez izrazito visoke stope mutacije;
- negativnu selekciju mutacija nastalih u onim sekvencama molekula klase I koji se vežu za receptore na T–ćelijama ili određuju bitna svojstva antigena;
- selekciju koja favorizira polimorfizam i heterozigotnost mjesta prepoznavanja antigena;
- periodičnu intraalelnu, rjeđe intragensku rekombinaciju unutar gena klase I.
Treba naglasiti da interakcija mogućih mutacija i rekombinacija u evolucijskim tokovima varira u ovisnosti o zahvaćenim MHC lokusima, čak i na subgenskoj razini. Analiza nekodirajućeg regiona može poslužiti za razjašnjavanje obrazaca evolucije alela, obično dajući suprotne rezultate od onih koji se dobiju analizom kodirajućeg regiona. Glavni izvor varijabilnosti sekvenci HLA gena su tačkaste mutacije, ali njihova frekvencija nije ništa veća nego u ostatku genoma. Akumulacija tačkastih mutacija (tokom miliona godina evolucije) rezultirala je velikim polimorfizmom MHC gena. Nasuprot tome, genskom konverzijom je, od početka filogenetske separacije linije Homo, nastalo najmanje 80 novih alela klase I, što ukazuje na činjenicu da je stopa konverzije mnogo veća od frekvencije tačkastih mutacija.
Svaki MHC receptor je u stanju da T ćelijama prezentira antigenske peptide sa tačno određenom dužinom i aminokiselinskom sekvencom. Smanjen MHC polimorfizam u određenoj populaciji ograničava broj peptida koji potencijalno mogu biti prezentirant T–ćelijama u funkciji indukcije imunog odgovora. Ukoliko proteinske molekule određenog mikroorganizma ne sadrže peptidne sekvence kompatibilne sa ograničenim brojem MHC molekula, ne može doći do aktivacije T–celija, zbog čega izostaje i imuni odgovor. Tako bi, npr., u slučaju infekcije ovakvim mikroorganizmom, opstanak cijele populacije bio ozbiljno ugrožen. Iz svega navedenog, može se zaključiti da je u toku evolucije selektivni pritisak favorizovao populacije sa izraženim polimorfizmom glavnog kompleksa histokompatibilnosti (MHC).[8] [9][10] [11]
Polimorfizam i genetika HLA sistema[uredi | uredi izvor]
Prema mnogima, genski kompleks HLA regiona predstavlja najsloženiji do sada opisani genski kompleks čovjeka (iako njegova sekvenca čini svega 0,001 % genoma i obuhvata 0,02 rekombinacijske jedinice, tj. 2 centimorgama). Pozicija HLA genskih lokusa definirana je klasičnim (morganovskim) mapiranjem, tj. genetičkom analizom frekvencije međusobnih crossing–overa u sekvenci susjednih lokusa i putem hibridizacije ćelija. MHC, a time i HLA regioni, su locirani na kratkom kraku hromosoma 6 (6p21.31) i obuhvata sekvencu od 3,3 Mbp (megabaznih parova) u zavisnosti od haplotipa. Najduži je HLA–DR53 haplotip u zbog prisutnosti 110–160 kilobaza više DNK u DR/DQ regionu. Već je spomenuto da je HLA kompleks “podijeljen” na tri klase: I, II i III. Telomerni region klasičnog HLA kompleksa je nazvan klasa Ib region, a također, postoje teorije da je klasa IV locirana na telomernom dijelu na kraju regiona klase III. Klasični HLA antigeni su kodirani u svakom regionu HLA–A, HLA–B i HLA–C u (klasa I), zatim HLA–DR, HLA–DQ i HLA–DP (u regionu klase II). Svi geni klase I sadrže 3–6, a geni klase II, 4–11 kilobaza. Klasa III ima najveću zbijenost, ali neki od tih gena ne pripadaju imunom sistemu. Projekat sekvencioniranja humanog MHC–a omogućilo je mapiranje svih gena pripadajućeg regiona.
MHC molekule klase I i II imaju centralnu ulogu u detekciji prisustva stranih antigena u organizmu i konsekventnoj aktivaciji T–ćelija u funkciji uklanjanja tih antigena. Funkcija ovih grupa molekula je vrlo različita. Tako su molekule MHC klase I prisutne na svim ćelijama organizma i uglavnom omogućava detekciju prisustva intracelularnih mikroorganizama. Fragmenti proteina (peptidi), koji se normalno sintetiziraju u ćeliji, konstantno se prezentiraju na njenoj površini putem MHC molekula klase I. T–ćelije, koje su u stanju da reaguju na ove peptide, uklonjene su iz cirkulacije putem negativne selekcije i supresije njihove aktivnosti, tako da ne dolazi do indukcije imunog odgovora na vlastite proteine (izuzev u slučaju autoimunih oboljenja, npr.). U slučaju infekcije intracelularnim mikroorganizmima (npr. virusima), peptidi iz ovih organizama se prezentiraju na površini ćelija i time signaliziraju prisustvo inficiranih ćelija. Te ćelije se uklanjaju iz obrambenog sistema djalatnošću citotoksičnih T–ćelija. Supstanca MHC klasa II prisutna je samo na tzv. antigen–prezentirajućim ćelijama (dendritične ćelije, makrofagi, B–limfociti i određene vrste epitelijalnih ćelija) i uglavnom omogućava detekciju vanćelijskih organizama i antigena. Imaju naglašenu sposobnost fagocitoze a fagocitirani vanćelijski materijal razgrađuju i prezentiraju na površini ćelije putem MHC klase II. Ukoliko je prezentirani materijal stranog porijekla, dolazi do aktivacije T–ćelija–pomoćnica (helper T–cells) koje konsekvento aktiviraju B–ćelije i proizvodnju specifičnih antitijela.
HLA antigeni se javljaju u ogromnom broju mogućih kombinacija produkata pet blisko vezanih i izrazito polimorfnih (multiploalelnih) genskih lokusa (HLA-A, HLA-B, HLA-C, HLA–D i HLA–DR), čiji redosljed (A–C–B–DR–D) na odgovarajućem segmentu hromosoma 6 ne odgovara njihovom abecednom slijedu. Alelne varijante pojedinih gena označavaju se indeksnim brojem (HLA–A, HLA–A2 …), pri čemu nedovoljno definirane (radne) nose predznak w (od workshop: HLA–Aw19, npr.). Koncem osamdesetih godina prošlog stoljeća bila su šire poznata 23 alela (i antigena) HLA–A, 49 HLA–B, 8 HLA–C, 19 HLA–D i 16 HLA–DR, što znači da se na svakom, iz para homologih hromosoma 6, alternativno može javiti jedna od 2.740.864 njihove kombinacije. Kompleks odgovarajućih alela istog hromosoma (u "cis–položaju’’) označava se kao haplotip. Imajući u vidu činjenicu da su rekombinacije među njima prava rijetkost (A–B: oko 1%, B–C: 0,2%, B–D: 0,5% i A–C: 0,5%), haplotipske kombinacije se prenose u bloku, kao cjeloviti i jedinstveni nasljedni elementi (suglasno ponašanju alela za jednostavna monogenska svojstva). Međutim, ukupni broj genotipova unutar diploidne garniture iznosi čak oko 3,8 x 1012. Ni u jednoj od pet korespondirajućih serija setova multiplih alela nema odnosa dominantnosti, pa prisustvo svake njihove varijante ima svoj odgovarajući grupno–specifični (antigeni) fenotipski izraz. HLA–A, HLA–B, HLA–C i HLA–DR se označavaju kao SD antigeni (od serum defined – jer se detektiraju pomoću specifičnih seruma), a HLA–D kao LD (lymphocyte defined – jer se određuju miješanjem kultivisanih limfocita nesrodnih osoba). Geni lokusa HLA–A, HLA–B i HLA–C kontroliraju sintezu antigena koji se označavaju kao:
- tkivni (jer se nalaze u svim stanicama, a posebno u limfocitima, tjelesnim tečnostima i kolostrumu,
- leukocitni (jer su prvo otkriveni na bijelim krvnim zrncima) i
- transplantacijski (po tome što kod primaoca izazivaju imunološku reakciju od koje ovisi prihvatanje ili odbacivanje transplantata); integralno i parcijalno, svi su –
- antigeni histokompatibilnosti (zato što primarno određuju stepen podudarnosti, odnosno međusobne snošljivosti tkiva različitih individua).
- Geni HLA–D lokusa odgovorni su za produkciju antigenih glikoproteina koji uzrokuju stimulaciju rasta mješovite kulture leukocita (in vitro). U kulturi miješanih leukocita nesrodnih osoba oni međusobno stimuliraju intenzivnu blastičnu transformaciju i diobu, a intenzitet te reakcije ovisi o genetičkim razlikama na ovom lokusu. HLA–D antigeni su prisutni u stanicama limfoidnog i monocitno–makrofagnog reda te na Langerhansovim stanicama kože (a vjerovatno i u spermijima i endotelu).
- Aleli HLA–DR lokusa određuju proizvodnju antigena na B limfocitima, a susreću se na monocitima, makrofagima, spermatozoidima, epitelnim i endotelnim stanicama.
- Ir lokus se nalazi u I segmentu HLA regiona, a njegove alelne varijante kontroliraju specifični imunološki odgovor T–limfocite–Ir–imune response). Pretpostavlja se da imaju značajnu ulogu u prepoznavanju antigena i u interakciji limfocita tokom imunološke reakcije kao i u efektivnoj fazi imunološke reakcije protiv inkompatibilnih ćelija (antigena). Lokusi gena za komponente komplementa iz HLA regiona kontroliraju sintezu proaktivatora B (varijanta Bf), komponente C3 te komponenti C2 i C4, koje predstavljaju značajne elemente glavnog kompleksa histokompatibilnosti (MHC). Komplement obuhvata najmanje 10 različitih polipeptidnih faktora svježeg seruma (C1...C10). Prvi od njih aktivira specifičnu reakciju antigen – antitijelo, a zatim se uključuje odgovarajući slijed lančanih reakcija koje rezultiraju oštećenjem ćelije – nosioca nespecifičnog antigena. Alternativni početak aktivacije ovog procesa (umjesto C1) je C3 za što je neophodno prisustvo nekog proaktivatora Bf, čija je specifičnost determinirana sa najmanje šest alela (od kojih su najčešći BfS i BfF). Do sada su identifikovani i geni koji kontroliraju sintezu C2 komponente (sa tri alelne varijante: C2 1, C2 2 i C2 3), a specifičnost komponente C4 određuju četiri alelogena (C4F, C4S, C4F1 i C4M).
HLA genotipizacija[uredi | uredi izvor]
HLA genotipizacija je neizostavan postupak u svim suvremenim transplantacijskim zahvatima, jer HLA sistem ima ekstremno značajnu ulogu u imunom odgovoru organizma – putem T–ćelija. HLA sistemski proteini su visoko polimorfne membranske molekule, koje mogu vezati antigene i predati ih T–ćelijama. Te proteinske molekule su inkodirane genima MHC regiona, diferenciranim u tri klase:
- klasa I (HLA–A, HLA–B i HLA–C);
- klasa II (HLA–DR, HLA–DQ i HLA–DP);
- klasa III (uglavnom sadrže gene komplementarnih proteina i ciotkina).
U klasu I se također svrstavaju i lokusi HLA–E, HLA–F, HLA–G, HLA–H, HLA–J, HLA–K i HLA–L, ali većina njih nije značajna kao peptidni "prezenter".
Klinički značaj HLA se posebno ispoljava prilikom tipizacije tkiva za potencijalnu transplantaciju. Polazni preduvjet za uspješnu tranplantaciju organa ili tkiva je što veći stupanj podudarnosti kompletnih MHC lokusa donatora (donora) i primaoca (recipijenta), čime se preveniraju mogući rizici za odbacivanje transplantata. Pouzdano je dokazana asocijacija određenih HLA genotipova sa više od 30 bolesti. Prema tome, individualna pripadnost određenim genotipovima ovog sustava može indicirati (povećanu) predispoziciju za takve bolesti.
HLA genotipizacija počinje izolacijom genomske DNK iz uzoraka krvi potencijalnog donora i primatlja. Nakon toga se amplificiraju (SSP–PCR) grupno–specifični regioni (SSP –sequence–specific primers = sekvenciono–specifični prajmeri; PCR – Polymerase Chain Reaction) koje promatramo. PCR produkti se vizualiziraju na agaroznom gelu (gel elektroforeza) ili direktnom DNK analizom sekvenci. Komparativnom analizom dobijenih rezultata procjenjuje se stupanj "genetičke imunološke sličnosti" potencijalnog donatora i primaoca organa ili tkiva. Ta procjena je neposredni pokazatelj “genetičke podobnosti” davaoca da uspješno donira i primaoca da uspješno prihvati transplantat. Za tako usmjerenu HLA genozipizaciju najčešće se koriste HLA–A, HLA–B, HLA–C (iz klase I), te HLA–DRB1, HLA–DQB1 i HLA–DPB1 (iz klase II).
Relacije HLA sistema i nekih bolesti[uredi | uredi izvor]
Pozitivna iskustva u analizama povezanosti krvnih grupa ABO sistema i nekih bolesti (naročito nekih karcinoma želuca) snažno su stimulirala i istraživanja asociranosti određenih HLA genotipova i bolesti. Takva istraživanja pritom obuhvataju populacijske i porodične studije. U populacijskim studijama se istražuje značaj razlika između skupina nesrodnih bolesnika i zdravih individua u frekvenciji pojedinih HLA antigena. U porodičnim studijama se ispituje stupanj konkordantnosti po istoj bolesti između oboljelih ispitanika i njihovih srodnika i da li oni češće pripadaju istom HLA haplotipu nego što se to očekuje prema prirodi nasljeđivanja fenotipova HLA sistema.
Nakon utvđivanja povezanosti između individualne specifičnosti HLA antigena i neke bolesti, utvrđuje se stupanj i mehanizam nasljeđivanja takve "podložnosti". Antigeni iste serije (A, B, C, D ili DR) se ponašaju kao da ih nadzire jedan alelomorfni gen, po principu jedan gen – jedna osobina. Shodno tome, i svaka promjena frekvencije jednog antigena se odražava na promjenu frekvencija ostalih antigena iste serije.
Dosadašnja istraživanja su pokazala da pojedine bolesti mogu biti “vezane” za jedan ili više antigena HLA sistema i da ta povezanost, u osnovi, može imati dominantni i recesivni oblik nasljeđivanja. Povećana frekvencija homozigotnih HLA gena, koji obilježavaju povećan rizik na neku bolest, ukazuje na recesivno nasljeđivanje datog svojstva. Ako se povezanost neke bolesti očituje sa dva antigena različitih serija neophodna je procjena vjetovatnoće povezanosti pojedinih antigena sa datom bolesti.
Povezanost između određenih HLA gena i bolesti se, naravno, ne može shvatiti kao bezuvjetna. To znači da nosilac određenog antigena ne mora a prior biti oblikatni “kandidat” za bolest koja pokazuje jasnu vezu sa nekim od HLA gena. Kao dokaz ovoj tvrdnji uzima se činjenica da ista bolest u različitim populacijama pokazuje povezanost sa različitim genima HLA sistema. Pretpostavlja se da gen ili geni za prijemčivost za neku bolest nisu identični marker–genu određene bolesti (HLA genu). Takva posebnost, ipak, pokazuje da su takvi geni u poziciji LD–a (linkage disequilibriuma) sa HLA genima, tj. individualno prisustvo jednog alela može uticati na prisustvo određenog alela na drugom lokusu (lokusima).
Prema specifičnosti asocijacije određenih bolesti sa nekim HLA genima, moguće je diferencirati više skupina tih bolesti. Takva kategorizacija je zasnovana na tipu bolesti i specifičnoj asociranoj seriji HLA gena.
Asocijacija HLA genotipova i autoimunih bolesti[uredi | uredi izvor]
Ova veza se u novije vrijeme se posebno intezivno proučava. Općepoznata je osobina autoimunih oboljenja da ih prati stimulacija klonalne ekspanzije T–ćelija, koje nisu uništene u timusu nekim protektivnim mehanizmima imunog sistema.
HLA molekule određuju koji peptid u mikrobnom antigenu će ta individua najefikasnije prepoznati, što, konsekventno tome, ima primarni uticaj na ekspresiju (konzerviranih) autoimunih sekvenci. Sve to, na kraju, utiče na brzinu razvoja autoimunog oboljenja. Najveći broj autoimunih oboljenja je povezan sa HLA sistemom, pa se češće javljaju kod osoba koje nose određene HLA alele. Najveća povezanost nekog genotipa i autoimunog oboljenja nađena je kod dijabetičara (diabetes melitus – tip I; insulin–ovisni dijabetes) i reumatoidnog artritisa. U slučaju ovog tipa šećerne bolesti, cilj autoimune aktivnosti su ß–ćelije Langerhansovih ostrvaca. Općenito gledano, kod autoimunih oboljenja veliki je broj autoantigena koji predstavljaju ciljne molekule u imunim reakcijama antitijela i T–ćelija, kako kod ljudi, tako i kod eksperimentalnih životinja. Autoantitijela na ćelije Langerhansovih ostrvaca prisutna su u serumu više od 90% pacijenata s pomenutim tipom dijabetesa. Nakon perioda od oko jedne godine, ova autoantitijela polagano nestaju, a imunopatološke promjene, u osnovi, nastaju zbog ćelijskog imunog odgovora. IDDM je kod čovjeka u vezi sa ekspresijom alela HLA–DQß MHC klase II. Ovaj ß–lanac sadrži neutralnu aminokiselinu (Ser, Ala ili Val) na poziciji 57. Za razliku od ovog, aleli klase II koji na 57–oj poziciji imaju asparaginsku kiselinu u jasnoj su vezi sa otpornošću na IDDM (aspartat–57 formira so koja stabilizira peptidne veze). S druge strane, i najsitnije modifikacije na drugim mjestima DQß–lanca mogu dovesti do povećane autoreaktivnosti T–ćelija. Kod osoba koje nose alele za rezistenciju na IDDM formira se kompleks koji vodi ka uništavanju formiranih autoantigena – uzročnika autoimunih reakcija. Treba, međutim, imati u vidu i činjenicu da je dijabetes multigensko oboljenje u kojem učestvuju geni koji ne pripadaju MHC–kompleksu, a pozicionirani su na različitim mjestima u genomu. U familijarnim studijama, utvrđeno je da je najveći broj autoimunih oboljenja prije u vezi sa klasom II, nego klasom I histokompatibilnog kompleksa (MHC). Ankilozni spondilitis je poremećaj u čvrstoj vezi sa alelnom varijantom HLA–B27, ali je rizik obolijevanja izuzetno nizak (svega 2% svih HLA–B27 pozitivnih osoba). Ovo objašnjava pojavu da se kod poremećaja povezanih sa HLA supstancama histokompatibilnosti ne nasljeđuje bolest nego prijemčivost za neko oboljenje. Postojanje povezanosti sa HLA ukazuje (ali ne i dokazuje) na to da su imunološki mehanizmi u vezi sa patogenezom nekih oboljenja.
U nekim slučajevima vrlo je vjerovatno da intenzitet autoimune reakcije ne ovisi o samom imunom sistemu (tj. molekulama histokompatibilnog kompleksa) nego o mašineriji (genima) koja proizvodi peptide koji učestvuju u imunim reakcijama. Različiti setovi ovih peptida, također, mogu imati određeni uticaj na T–ćelijski imuni odgovor, tako da u utvrđivanju povezanosti nekog MHC genotipa i oboljenja treba voditi računa o polimorfizmu drugih molekula koje su uključeni u imunološki sistem organizma.
Reference[uredi | uredi izvor]
- ^ Kimball's Biology Arhivirano 7. 3. 2018. na Wayback Machine Histocompatibility Molecules
- ^ Hadžiselimović R., Pojskić N. (2005): Uvod u humanu imunogenetiku. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-3-4.
- ^ Karamehić J. (2002): Transplantacija organa. Printcom, Tuzla.
- ^ Hadžiselimović R., Pojskić N. (2005): Uvod u humanu imunogenetiku. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-3-4.
- ^ Karamehić J. (2002): Transplantacija organa. Printcom, Tuzla.
- ^ Hadžiselimović R., Pojskić N. (2005): Uvod u humanu imunogenetiku. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-3-4.
- ^ Karamehić J. (2002): Transplantacija organa. Printcom, Tuzla.
- ^ Hadžiselimović R., Pojskić N. (2005): Uvod u humanu imunogenetiku. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-3-4.
- ^ Karamehić J. (2002): Transplantacija organa. Printcom, Tuzla.
- ^ Hadžiselimović R. (2005): Bioantropologija – Biodiverzitet recentnog čovjeka. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-2-6.
- ^ Hadžiselimović R., Pojskić N. (2005): Uvod u humanu imunogenetiku. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-3-4.
Također pogledajte[uredi | uredi izvor]
Vanjski linkovi[uredi | uredi izvor]
- Major Histocompatibility Complex na US National Library of Medicine Medical Subject Headings (MeSH)
- Molecular individuality (German online-book 2012) Arhivirano 29. 1. 2013. na Wayback Machine
- Sexual attraction is linked to MHC compatibility
- NetMHC 3.0 server — predicts binding of peptides to a number of different MHC (HLA) alleles
- T-cell Group - Cardiff University
- The story of 2YF6: A Chicken MHC[mrtav link]
- RCSB Protein Data Bank: Molecule of the Month - Major Histocompatibility Complex Arhivirano 28. 5. 2010. na Wayback Machine
- dbMHC Home, NCBI's database of the Major Histocompatibility Complex
