Tetrahidrokanabinol
| Tetrahidrokanabinol | ||
|---|---|---|
| Naziv lijeka | Tetrahidrokanabinol | |
| Druga imena | dronabinol, THC | |
| Grupa | Kanabinoidi | |
| ||
| ATC kodovi | A04AD10 | |
| CAS registarski broj | 1972-08-3 | |
| ||
| Stručne informacije | ||
| ||
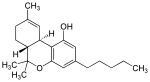 Ime po IUPAC (−)-(6aR,10aR)-6,6,9-trimetil-3-pentil-6a,7,8,10a-tetrahidro-6H-benzo[c]hromen-1-ol | ||
| Sumarna formula | C21H30O2 | |
| Tačka topljenja | 157 °C | |
| Molarna masa | 314,45 g/mol | |
| ||
| Biološka raspoloživost | 10-35% (inhalacija) 6-20% (oralno) | |
| Metabolizam | uglavnom hepatični | |
| Poluvrijeme eliminacije | 1,6h - 59h | |
| Izlučivanje | 65-80% fekalno, ostatak urinom | |
Tetrahidrokanabinol ili skraćeno THC, poznat i kao Δ9-THC, Δ9-tetrahidrokanabinol (delta-9-tetrahidrokanabinol), Δ1-tetrahidrokanabinol ili dronabinol, glavna je psihoaktivna supstanca koja se nalazi u biljci indijska konoplja (lat. Canabis sativa), poznatijoj kao marihuana. Nalazi se u indijskoj konoplji, pelinu i njegovom derivatu apsintu (švicarska rakija). THC je izoliran u Izraelu 1964. od strane Raphaela Mechoulama, Yechiela Gaonija i Habiba Ederyja na Weizmannovom institutu u Rehovotu. U mnogim zemljama danas se koristi u medicinske svrhe.
THC je veoma slabo rastvorljiv u vodi, ali se veoma dobro rastvara nekim drugim organskim otapalima, kao što su butan ili heksan. Osnovna funkcija THC-a u indijskoj konoplji, kao što je to slučaj s kofeinom i nikotinom, jeste da čuva biljku od štetočina ili biljoždera koji je mogu napasti. Također dobro apsorbira UV-B zračenje (280-315 nm), štiteći je od radijacije. U osnovnom stanju on je staklasta čvrsta tvar kad je hladno, dok pod utjecajem toplote prelazi u viskozno stanje i postaje ljepljiv.
Farmakologija[uredi | uredi izvor]
Svoje farmakološko djelovanje THC ostvaruje kao egzogeni agonist koji se vezuje za tzv. kanabinoidne receptore CB 1 u mozgu. Ovi receptori spadaju u porodicu G–protein receptora i identifikovana su dva podtipa kanabinoidnih receptora – CB 1 i CB 2, a od kojih je CB 1 pronađen u mozgu. Ćelijski odgovor pri vezivanju liganda sa kanabinoidnim receptorom je višestruk. Prvi korak je aktivacija G-proteina, što dalje dovodi do promjene kod više intracelularnih komponenti, npr, cAMP, kao i ioni kalcija i kalija, koji dovode do promjene u ćelijskoj funkciji. Definitivni ćelijski odgovor zavisi od tipa ćelije, liganda i drugih molekula koji se takmiče za mjesto vezivanja na receptoru. Različiti agonisti imaju različitu snagu vezivanja za receptor, što zavisi od efektivne doze aktivne supstance i efikasnosti koja predstavlja maksimalnu snagu signala koji se prenosi do ćelije. Kod THC-a su ove vrijednosti niže nego kod sintetičkih kanabinoida, koji su znatno efikasniji.
Prisutnost ovih specijaliziranih receptora u mozgu navela je istraživače na ideju unutrašnjih kanabinoida koje proizvodi tijelo. Krenula je potraga za tvarima koje normalno proizvodi mozak i vežu se za kanabinoidne receptore, takozvani prirodni agonist i ligand, što je dovelo do otkrića anandamida, 2-arachidonil glicerida (2-AG) i ostalih sličnih spojeva. Priča je slična kao i kod otkrića unutrašnjih opiata (endorfin, enkefalin, dinorfin) nakon što se shvatilo za koje receptore se vežu morfin i drugi opiati. Naknadno se pokazalo da kanabinoidi, preko trenutno nepoznatog mehanizma, aktiviraju unutrašnje staze opiata preko μ1 opoidnog receptora, naglo oslobađajući dopamin u nucleus accumbens. Ovaj efekt može biti potisnut sa antagonistom rimonabant (SR141716A) CB1 kanabinoidnog receptora ili kod opioidnim receptorom sa antagonistom nalokson ili naloksazin.[1].
THC ima analgetička svojstva i pri malim dozama, što je dovelo do mogućnosti liječenja boli medicinskim kanabisom. Mehanizam koji to omogućava još nije u potpunosti poznat. Drugi efekti su opuštanje, euforija, promijenjena percepcija vremena i prostora, osjetljivost vizualnih, slušnih i njušnih živaca, dezorijentacija, eventualni umor i povećani apetit, sve povezano sa stimulacijom CB1 receptora u centralnom nervnom sistemu (CNS-u). Povećani apetit donekle je objašnjen preko gastro-hipotalamičkog sistema. Aktivnost CB1 receptora u centru za glad u hipotalamusu čini hranu ukusnijom i prihvatljivijom, hormon za glad grelin povećava signale za glad kako hrana dospijeva u želudac. Tu su još neka svojstva koja spuštaju razinu agresije.
THC ima i aktivni metabolit, 11-hidroksi-THC, koji također ima ulogu u analgetičkim i rekreacijskim efektima biljke.
CB-1 receptori[uredi | uredi izvor]
CB 1 receptori se nalaze u mozgu u velikom broju, čak više nego većina drugih receptora iz njihove grupe, a u 10 puta su većem broju u odnosu na opioidne receptore preko kojih se ispoljava efekt morfina.
Ovi receptori su po svom sastavu proteini i kao većina receptora su dijelom uronjeni u ćelijsku membranu. Vezuju se za ekstracelularni dio receptora aktivirajući signalni mehanizam unutar ćelije. Molekula CB 1 receptora veća je nego molekula CB 2 receptora. Njihova homolognost je 44% za cijelokupni protein.
Kanabinoidni receptori su učvršćeni u ćelijskoj membrani i spojeni sa G proteinom i enzimom adenil ciklaza (AC). Receptori se aktiviraju pri kontaktu s THC–om ili njegovim derivatom, što izaziva niz reakcija, uključujući inhibiciju adenilciklaze, što smanjuje produkciju cAMP-a, otvaranje K+ kanala, a zatvaranje Ca kanala.
Toksičnost[uredi | uredi izvor]
Prema Merck indeksu, 12. izdanje, THC ima LD50 vrijednost od 1270 mg/kg (muški štakor) i 730 mg/kg (ženski štakor) uzeto oralnim putem rastopljeno u sezamovom ulju.[2]
Kad bi se te vrijednosti računale prema odraslom čovijeku, iznosile bi otprilike 50 i 86 g za 68 kg ženske ili muške osobe. To je ekvivalent za 1 do 1,8 kg kanabisa sa 5% THC-a uzeto oralnim putem. LD50 vrijednost za štakore uzeto putem inhalacije iznosi 42 mg/kg po težini tjelesne mase. Potrebno je napomenuti da studije toksičnosti kod životinjskih modela ne moraju nužno odgovarati toksičnosti u ljudskom organizmu. Receptor raspodjele THC-a u centralnom nervnom sistemu štakora drugačiji je nego kod ljudi, što znači da postoji bitna mogućnost da toksičnost kod ljudi varira od objavljenih životinjskih studija prema LD50. Ne postoji dokumentirana smrt povezana s predoziranjem marihuanom ili THC-om. Apsorpcija je ograničena serumskim lipidima, koji mogu postati zasićeni THC-om, tako da prisutna topljivost može ublažiti toksičnost.
Studije na temu distribucije kanabinoidnih receptora objašnjavaju zašto je toksičnost THC-a tako mala. Dijelovi mozga koji upravljaju vitalnim funkcijama, poput respiratornog sistema, nemaju mnogo receptora, stoga su relativno nezahvaćeni i dozama daleko većim od prosječnih ili onih koje bi dospjele u organizam u normalnim uvjetima.
Sintetički THC[uredi | uredi izvor]
Sintetički THC još je poznat pod imenom dronabinol, dostupan je kao lijek na recept (pod trgovačkim imenom Marinol) u nekoliko država uključujući SAD, Holandiju i Njemačku. U SAD-u, Marinol je tretiran kao nenarkotička droga sa vrlo slabim rizikom za fizičku i mentalnu ovisnost, propisan na recept, na tzv. popisu III kontroliranih supstanci. Iako je DEA 2002. prihvatila peticiju, cannabis još uvijek nije tretiran jednako kao Marinol. Marinol je odobren od FDA u terapijama anoreksije kod pacijenata sa AIDS-om, kao i kod nekih glavobolja ili povraćanja za pacijente hemoterapije.
Analog dronabinolu, nabilon, dostupan je slobodno u Kanadi pod trgovačkim imenom Cesament kojeg proizvodi firma Valeant. Cesament ja također dobio odobrenje FDA-a za buduću dostupnost u SAD-u u nivou II kontroliranih supstanci.
U aprilu 2005. godine, Kanada je odobrila Sativex, raspršivač za usta za oboljele od multiple skleroze za olakšanje boli. Sativex sadrži tetrahidrokanabinol zajedno sa kanabidiolom. Proizvodi ga firma GW Pharmaceuticals i to je prvi lijek u svijetu baziran na kanabisu.
Istraživanja[uredi | uredi izvor]
Mnoge studije uključuju medicinske mogućnosti THC-a u liječenju raka i side, i to, npr, povećavajući apetit i smanjujući mučnine. Pokazalo se i od koristi kod oboljelih od glaukoma, gdje snižava očni pritisak.[nedostaje referenca] THC je korišten i u obliku kanabisa kod mnogobrojnih pacijenata oboljelih od multiple skleroze. Nedavno je kanabis preko medicinskog recepta korišten kod odraslih i maloljetnih pacijenata s ADD i ADHD poremećajima zbog svog opuštajućeg i umirujućeg efekta.
Neke studije također su pokazale i negativnu stranu THC-a povezanu s neprestanom i dugotrajnom upotrebom, koje uključuju gubitak kratkotrajnog pamćenja. Međutim, postoje studije koje opovrgavaju ove tvrdnje, tvrdeći da magnentna rezonanca (MR) kod dugotrajnih korisnika pokazuje vrlo male ili nikakve razlike spram MR-a osoba koje nisu uzimale THC. Studije na temu učinaka kod dugotrajnog korištenja su manjkave zbog ilegalnog statusa droge, što sâmō istraživanje čini otežanim.
Pripremna istraživanja sa sintetičkim THC-om kod pacijenata oboljih od Touretteovog sindrom pokazuju da bi THC mogao u velikoj mjeri pomoći u smanjenju živčanih tikova.
Studije na životinjama s "Marinolom" i nikotinom pokazuju da bi mogli biti korisna dopuna neuroleptičnim lijekovima. Također, istraživanje na 12 pacijenata pokazuje da "Marinol" snižava tikove bez značajnih štetnih učinaka. Slično istraživanje pokazalo je iste rezultate kod 24 pacijenta u periodu od 6 sedmica.
Nedavna istraživanja sa sintetičkim kanabinoidom pokazuju da aktivacija CB1 receptora može uzrokovati neuroobnavljanje i neurozaštitu, a može zaustaviti i prirodnu degeneraciju kod neurodegenerativnih bolesti kao što su Parkinsonova ili Alzheimerova bolest.
U in-vitro eksperimentima sa THC-om s izuzetno visokim koncentracijama (koje nisu dostupne u uobičajenoj konzumaciji) pokazalo se da uzrokuje inhibiciju određenih formacija koje uzrokuju Alzheimerovu bolest, i to bolje nego trenutno odobreni lijekovi.[3]
Studija iz 1975. pokazuje redukciju tumora kod miševa, što je dokaz potencijalnom tretmanu protiv raka.
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Carl R Lupica; et al. "Marijuana and cannabinoid regulation of brain reward circuits". Pristupljeno 1. 7. 2007. Eksplicitna upotreba et al. u:
|author=(pomoć) - ^ Erowid. "Hemija kanabisa". Pristupljeno 20. 3. 2006.
- ^ Eubanks LM, Rogers CJ, Beuscher AE; et al. (2006). "Molekularna veza između marihuane i patologije Alchajmerove bolesti". Mol. Pharm. 3 (6): 773–7. doi:10.1021/mp060066m. PMID 17140265. Eksplicitna upotreba et al. u:
|author=(pomoć)CS1 održavanje: više imena: authors list (link)
| Commons ima datoteke na temu: Tetrahidrokanabinol |

