Defosforilacija
Defosforilacija je skidanje fosfata (PO43−) organskih sastojaka putem hidrolize . To je reverzibilna posttranslacijska modifikacija. Defosforilaciju i njegovih suprotni pravac fosforilaciju, aktiviraju i deaktiviraju enzimi za odvezivanje ili privezivanje fosfornih estera i anhidrida. Značajna pojava defosforilacije je konverzija adenozin trifosfata (ATP) u ADP i anorganski fosfat.[1][2][3][4]
Defosforilaciju pokreće hidrolitički enzim hidrolaza, koji raskida esterske veze. Prominentna potklasa hidrolaza u defosforilaciji je fosfataza. Fosfataza uklanja fosfatne grupe hidrolizom monoestera fosforne kiseline u fosfatni ion i molekulu sa slobodnom hidroksilnom (-OH) grupom.
Reverzibilna reakcija fosforilacije-defosforilacija se javlja u svakom fiziološkom procesu, što pravilno usmjeravafunkciju protein fosfataza koje su neophodne za održivost organizma. zato što je defosforilacija protein ključni proces u ćelijskoj signalizacijI, protein fosfataze su upletene u stanja kao što su srčane bolesti, dijabetes i Alzheimerova bolest.
Funkcija
[uredi | uredi izvor]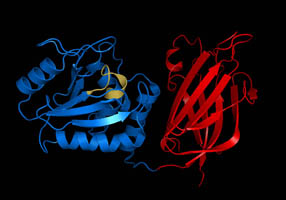
Aktivno mjesto plavog N-terminala fosfatazne domene je žuto, a C-terminala C2 domene – crveno.
Fosforilacija i defosforilacija hidroksilnih skupina koje pripadaju neutralnim ali polarnim aminokiselinams, kao što su serin, treonin, tirozin, unutar specifičnih ciljnih protein, temeljni su dio regulacije svakog fizioloških procesa. Fosforilacija uključuje kovalentnu modifikaciju hidroksilne sa fosfatnom grupom putem nukleofilnog napada alfa fosfata u ATP, kisikom u hidroksilu. Defosforilacija uključuje uklanjanje fosfatne grupe, hidratacijskim dodavanjem molekula vode i oslobađanjem originalne fosfatne grupe, regenerirajući hidroksilne. Oba procese su reverzibilna, a svaki mehanizam može se koristiti za aktiviranje ili deaktiviranje proteina. Fosforilacija proteina stvara mnoge biohemijske efekte, kao što su izmjene konformacije u vezivanju za određeni ligand , povećanjem ili smanjivanjem aktivnosti. Fosforilacija i defosforilacija se mogu koristiti na svim vrstama podloga, kao što su strukturni proteini, enzimi, membranski kanali, signalnie molecule I druge kinaze i fosfataze. Zbir tih procesa se naziva ‘’’fosforegulacija’’’.[5] Deregulacija fosforegulacije može dovesti do pojave bolesti
Defosforilacija u drugim reakcijama
[uredi | uredi izvor]Ostale molekule, osim ATP podliježu defosforilaciji kao dio ostalih bioloških sistema. Kao rezultat defosforilacije, razni sastojci produciraju različite promjene slobodne energijemolecule.[6]
| Molekula | Promjena u slobodnoj energiji |
|---|---|
| Acetil fosfat | 47.3 kJ/mol |
| Glukoza-6-fosfat | 13.8 kJ/mol |
| Fosfoenolpiruvat (PEP) | -61.9 kJ/mol |
| Fosfokreatin | 43.1 kJ/mol |
Također pogledajte
[uredi | uredi izvor]Reference
[uredi | uredi izvor]- ^ Kornberg A. (1989): For the love of enzymes – The Odyssay of a biochemist. Harvard University Press, Cambridge (Mass.), London,ISBN 0-674-30775-5, ISBN 0-674-30776-3.
- ^ Hunter G. K. (2000): Vital Forces. The discovery of the molecular basis of life. Academic Press, London 2000, ISBN 0-12-361811-8.
- ^ Nelson D. L., Cox M. M. (2013): Lehninger Principles of Biochemistry. W. H. Freeman and Co., ISBN 978-1-4641-0962-1.
- ^ Bajrović K, Jevrić-Čaušević A., Hadžiselimović R., Ed. (2005): Uvod u genetičko inženjerstvo i biotehnologiju. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-1-8.
- ^ Beltrao P., Trinidad J. C., Fiedler D. (2009): Evolution of phosphoregulation: comparison of phosphorylation patterns across yeast species. PLoS Biol., 7 (6): 1000134.
- ^ http://www.chemistry.wustl.edu/~edudev/LabTutorials/Cytochromes/cytochromes.html, Energy for the Body: Oxidative Phosphorylation, Department of Chemistry, Washington University.
