Dužina hemijske veze
Dužina hemijske veze ili distanca veze – u molekulskoj geometriji – je prosječno (fizičko) rastojanje između jezgara dva vezana atom u molekuli. Ona je prenosivi dio veze između povezanih atoma, relativno nezavisna od ostatka molekule.
Opis[uredi | uredi izvor]
Dužina veze se odnosi na red veze: kada u njenom formiranju sudjeluje više elektrona, ona je kraća. Dužina veze je također obrnuto proporcionalna snazi veze i energiji disocijacije veza: sve ostalo je jednako, a jače veze su kraće. U vezi između dva identična atoma, polovina njene dužine jednaka je kovalentnom radijusu.
Dužine veze se mjere u čvrstoj fazi pomoću difrakcije X-zrakama ili , u plinovitoj fazi, približno se procjennjuje mikrotalasnom spektroskopijom. Veza između određenog para atoma može se razlikovati između različitih molekula. Naprimjer, ugljik u vodikovoj vezi metana je drugačiji od onog u metil hloridu. Međutim, kada je struktura ista, moguće je napraviti i određena uopćavanja.
Dužina veze ugljika s drugim elementima[uredi | uredi izvor]
Slijedi tabela sa eksperimentalnim jednostrukim vezama ugljika i drugih elemenata. Dužine veza su date u pikometrima (pm). Pri aproksimaciji dužine veza između dva različita atoma uzet je zbir pojedinačnih kovalentnih radijusa (navedeni su članci za svaki hemijski element). Kao opći trend, dužina veze pada preko reda u periodnom sistemu i povećava se ispod grupa u sistemu. Ovaj trend je identičan onom kod atomskog radijusa.
| Vezani elementi | Dužina veze (pm) |
Grupa |
| H | 106 - 112 | Grupa 1 |
| Be | 193 | Grupa 2 |
| Mg | 207 | Grupa 2 |
| B | 156 | Grupa13 |
| Al | 224 | Grupa 13 |
| In | 216 | Grupa 13 |
| C | 120 - 154 | Grupa 14 |
| Si | 186 | Grupa 14 |
| Sn | 214 | Grupa 14 |
| Pb | 229 | Grupa 14 |
| N | 147 - 210 | Grupa 15 |
| P | 187 | Grupa 15 |
| As | 198 | Grupa 15 |
| Sb | 220 | Grupa 15 |
| Bi | 230 | Grupa 15 |
| O | 143 - 215 | Grupa 16 |
| S | 181 - 255 | Grupa 16 |
| Cr | 192 | Grupa 16 |
| Se | 198 - 271 | Grupa 16 |
| Te | 205 | Grupa 16 |
| Mo | 208 | Grupa 16 |
| W | 206 | Grupa 16 |
| F | 134 | Grupa 17 |
| Cl | 176 | Grupa 17 |
| Br | 193 | Grupa 17 |
| I | 213 | Grupa 17 |
Dužine veze organskih jedinjenja[uredi | uredi izvor]
Dužina vezu između dva atoma u molekuli ne zavisi samo od atoma, već i faktora kao što su orbitalna hibridizacija i elektronski i prostorni prirod supstituenta. U vezi ugljik–ugljik (C-C) dužina u dijamantu je 154 pm, što je ujedno i najveća dužina veze koja postoji za obične ugljikove kovalentne veze.
Postoje i neuobičajeno duge veze. U spoju triciklobutabenzenu, dužina veze 160 pm. Sadašnji rekorder je još jedan ciklobutabenzen, dužine 174 pm, na osnovu kristalografije X-zrakama. U ovoj vrsti spojeva sa ciklobutanskim prstenom, veličina uglova od 90° na atomu ugljika, povezana je sa benzenskim prstenom, gdje obično imaju uglove od 120°.[2] In this type of compound the cyclobutane ring would force 90° angles on the carbon atoms connected to the benzene ring where they ordinarily have angles of 120°.
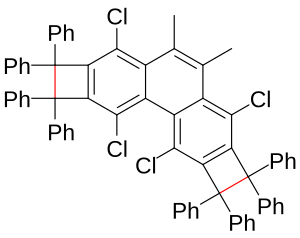
Smatra se da se veće dužine veze C-C veza, do 290 pm, javljaju u dimeru dva tetracijanoetilenska dianiona, što se odnosi i na veze 2-elektron-4-centra.[3][4] Ovaj način vezanja je također uočena u dimeru neutralnog fenalena. Dužina tih takozvanih "palačinka veza"[5] je do oko 305 pm.
Moguće su i potprosječne dužine C-C veze: alkeni i alkini imaju dužine veza od 133 pm i 120 pm, zbog povećanog s-karaktera sigma veza. U benzenu, sve veze imaju iste dužine: 139 pm. U centralnoj jednostrukoj ugljik–ugljik vezi, također je značajan porast s-karaktera diacetilena (137 pm), kao i kod određenih tetrahedranskih dimera (144 pm). U propionitrilu, cijano grupa povlači elektrone, što rezultira smanjenjem dužine veza (144 pm). Najmanja teorijska dužina jednostruke C-C veze za tetrahedranske derivate u ovom istraživanju je bola 131 pm. Postoji neobičan organski spoj pod nazivom ln-metilciklofan, sa metil grupom koja je stisnuta između tripticena i fenil grupe, a vrlo malom dužinom veza, od 147 pm.[6] U eksperimentiratima in silico, nađene dužine hemijskih veza su 136 pm, procijenjene za neopentan koji je zatvoren u fulerenu[7] U istim istraživanjima, procijenjeno je da istezanje ili stiskanje C-C veze u molekuli etana za 5 pm odgovara 2,8 ili 3, 5 kJ/mola, a procjena za 15 pm iznosi 21,9 ili 37,7 kJ/mol.
| C–H | Dužina (pm) |
C–C | Dužina (pm) |
Višestruke veze | Dužina (pm) |
| sp3–H | 110 | sp3–sp3 | 154 | Benzen | 140 |
| sp2–H | 109 | sp3–sp2 | 150 | Alken | 134 |
| sp–H | 108 | sp2–sp2 | 147 | Alkin | 120 |
| sp3–sp | 146 | Alen | 130 | ||
| sp2–sp | 143 | ||||
| sp–sp | 137 |
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Handbook of Chemistry & Physics (65th izd.). CRC Press. 1984. ISBN 0-8493-0465-2.
- ^ Fumio Toda (april 2000). "Naphthocyclobutenes and Benzodicyclobutadienes: Synthesis in the Solid State and Anomalies in the Bond Lengths". European Journal of Organic Chemistry. 2000 (8): 1377–1386. doi:10.1002/(SICI)1099-0690(200004)2000:8<1377::AID-EJOC1377>3.0.CO;2-I. Arhivirano s originala, 29. 6. 2012. Pristupljeno 9. 5. 2016.
- ^ Novoa JJ, Lafuente P, Del Sesto RE, Miller JS (2. 7. 2001). "Exceptionally Long (2.9 Å) C-C Bonds between [TCNE]- Ions: Two-Electron, Four-Center *-* C-C Bonding in -[TCNE]22-". Angewandte Chemie International Edition. 40 (13): 2540–2545. doi:10.1002/1521-3773(20010702)40:13<2540::AID-ANIE2540>3.0.CO;2-O. Arhivirano s originala, 29. 6. 2012. Pristupljeno 9. 5. 2016.CS1 održavanje: više imena: authors list (link)
- ^ Lü J-M, Rosokha SV, Kochi JK (2003). "Stable (Long-Bonded) Dimers via the Quantitative Self-Association of Different Cationic, Anionic, and Uncharged -Radicals: Structures, Energetics, and Optical Transitions". J. Am. Chem. Soc. 125 (40): 12161–12171. doi:10.1021/ja0364928.CS1 održavanje: više imena: authors list (link)
- ^ Suzuki S, Morita Y, Fukui K, Sato K, Shiomi D, Takui T, Nakasuji K (2006). "Aromaticity on the Pancake-Bonded Dimer of Neutral Phenalenyl Radical as Studied by MS and NMR Spectroscopies and NICS Analysis". J. Am. Chem. Soc. 128 (8): 2530–2531. doi:10.1021/ja058387z.CS1 održavanje: više imena: authors list (link)
- ^ Huntley DR, Markopoulos G, Donovan PM, Scott LT, Hoffmann R (2005). "Squeezing CC Bonds". Angewandte Chemie International Edition. 44 (46): 7549–7553. doi:10.1002/anie.200502721. PMID 16259033.CS1 održavanje: više imena: authors list (link)
- ^ Martinez-Guajardo G, Donald KJ, Wittmaack BK, Vazquez MA, Merino G (2010). "Shorter Still: Compresing C-C Single Bonds". Organic Letters, ASAP. 12 (18): 4058. doi:10.1021/ol101671m.CS1 održavanje: više imena: authors list (link)
- ^ Fox, Marye Anne; Whitesell, James K. (1995). Organische Chemie: Grundlagen, Mechanismen, Bioorganische Anwendungen. Springer. ISBN 978-3-86025-249-9.CS1 održavanje: više imena: authors list (link)
- ^ Prof Chao-Jun Li, Ph.D. in lecture, March 2009}}
