Zeleni fluorescentni protein
| Zeleni fluorescentni protein | |
|---|---|
 Struktura zelenog fluorescentnog proteina Aequorea victoria.[1] | |
| Identifikatori | |
| Simbol | GFP |
Zeleni fluorescentni protein (GFP) je protein koji pokazuje jarko zelenu fluorescenciju kada je izložen svjetlu u plavom do ultraljubičastom opsegu.[2][3] Oznaka GFP tradicionalno se odnosi na protein koji je prvi izolovan iz meduza Aequorea victoria i ponekad se naziva avGFP. Međutim, GFP-ovi su pronađeni u drugim organizmima uključujući korale, morske anemone, zoanitide, copepoda i lancelete.[4]
GFP iz A. victoria ima glavni pik ekscitacije na talasnoj dužini od 395 nm i manji na 475 nm. Vrh njegove emisije je na 509 nm, što je u donjem zelenom dijelu vidljivog spektra. Kvantni prinos (QY) florescencije GFP-a je 0,79. GFP iz morske maćuhice (Renilla reniformis) ima jedan glavni ekscitacioni vrh na 498 nm. GFP je odličan alat u mnogim oblicima biologije zbog svoje sposobnosti da formira unutrašnji hromofor, bez potrebe za bilo kakvim dodatkom kofaktora, genskih proizvoda ili enzima / supstrata osim molekulskog kisika.[5]
U citologiji i molekulskoj biologiji, GFP gen se često koristi kao izvještač ekspresije.[6] Korišten je u modifikovanim oblicima za pravljenje biosenzora, a stvorene su mnoge životinje koje eksprimiraju GFP, što pokazuje dokaz koncepta da se gen može eksprimirati u datom organizmu, u odabranim organima , ili u ćelijama od interesa. GFP se može uvesti u životinje ili druge vrste putem transgenih tehnika, i održavati u njihovom genomu i genomu njihovog potomstva. Do danas, GFP je bio izražen u mnogim taksonima, uključujući bakterije, kvasce, gljive, ribe i sisare, uključujući i ljudske ćelije. Naučnici Roger Y. Tsien, Osamu Shimomura i Martin Chalfie su 10. oktobra 2008. dobili Nobelovu nagradu za hemiju 2008. za njihovo otkriće i razvoj zelenog fluorescentnog proteina .
Većina komercijalno dostupnih gena za GFP i slične fluorescentne proteine dugi su oko 730 parova baza. Prirodni protein ima 238 aminokiselina. Njegova molekulska masa je 27 kD.[7] Stoga, spajanje GFP gena sa genom proteina od interesa može značajno povećati veličinu i molekulsku masu proteina i može narušiti prirodnu funkciju proteina ili promijeniti njegovu lokaciju ili putanju transporta unutar ćelija.[8]
Pozadina[uredi | uredi izvor]


GFP divljeg tipa (wtGFP)[uredi | uredi izvor]
Prva prijavljena kristalna struktura GFP-a bila je ona mutanta S65T od strane Remingtonove grupe u Science 1996.[9] Mjesec dana kasnije, Phillipsova grupa je nezavisno prijavila GFP divljeg tipa struktura u Nature Biotechnology.[10] Ove kristalne strukture pružile su vitalnu pozadinu za formiranje hromofora i interakcije susjednih ostataka. Istraživači su modificirali ove ostatke usmjerenom i nasumičnom mutagenezom, kako bi proizveli širok spektar GFP derivata koji se danas koriste. Dalja istraživanja GFP-a su pokazala da je otporan je na deterdžente, proteaze, tretmane gvanidinij-hloridom (GdmCl) i drastične promene temperature.[11]
Nomenklatura[uredi | uredi izvor]
Nomenklatura modificiranih GFP-ova često je zbunjujuća zbog preklapanja mapiranja nekoliko GFP verzija na jedno ime. Naprimjer, mGFP se često odnosi na GFP sa N-terminalom palmitoilacijom koji uzrokuje da se GFP veže za ćelijske membrane. Međutim, isti termin se također koristi za označavanje monomernih GFP-a, koji se često postiže tako što interfejs dimera razbija mutaciju A206K.[12] GFP divljeg tipa ima slabu tendenciju dimeraizacije pri koncentracijama iznad 5 mg/mL. mGFP je također skraćenica za "modificirani GFP", koji je optimiziran kroz razmjenu aminokiselina za stabilnu ekspresiju u biljnim ćelijama.
U prirodi[uredi | uredi izvor]


Svrha i (primarnih) bioluminiscencija (od djelovanja ekvorins na luciferin) i (sekundarne) fluorescencije GFP-a u meduzama je nepoznata. GFP se ko-eksprimira sa ekvorinom u malim granulama oko oboda zvona meduze. Sekundarni ekscitacijski vrh (480 nm) GFP-a apsorbuje nešto od plave emisije ekvorina, dajući bioluminiscenciji zeleniju nijansu. Ostatak serina 65 GFP-a hromofora je odgovoran za spektre ekscitacije sa dvostrukim vrhom GFP-a divljeg tipa. Sačuvan je u sve tri GFP izoforme koje je prvobitno klonirao Prasher. Gotovo sve mutacije ovog ostatka konsolidiraju ekscitacijske spektre u jedan vrh na 395 nm ili 480 nm. Precizan mehanizam ove osjetljivosti je složen, ali, čini se, uključuje doniranje vodika iz serina 65 u glutamat 222, koji utiče na ionizaciju hromofora.[3] Budući da jedna mutacija može dramatično povećati 480 nm ekscitacioni vrh, što GFP čini mnogo efikasnijim partnerom ekvorina, Čini se da A. victoria evolucijski preferira manje efikasan spektar ekscitacije sa dvostrukim vrhom. Roger Tsien je spekulisao da promjenjivi hidrostatski pritisak sa dubinom može uticati na sposobnost serina 65 da donira vodik hromoforu i pomjeri omjer dva ekscitirajuća pika. Dakle, meduza može promijeniti boju svoje bioluminiscencije s dubinom. Međutim, kolaps u populaciji meduza u Friday Harbor, Washington, gdje je GFP prvobitno otkriven, omeo je dalje proučavanje uloge GFP-a u prirodnom okruženju meduze.
Poznato je da većina vrsta lancelet proizvodi GFP u različitim dijelovima svog tijela.[13] Za razliku od A. victoria, lancete ne proizvode sopstvenu plavu svjetlost, a porijeklo njihovog endogenog GFP-a je još uvijek nepoznato. Neki nagađaju da privlači plankton prema ušću lancete, služeći kao pasivni mehanizam za lov. Takođe može poslužiti kao fotoprotektivni agens u larvama, sprečavajući oštećenja uzrokovana plavim svjetlom visokog intenziteta pretvarajući ga u zeleno svjetlo nižeg intenziteta. Međutim, ove teorije nisu testirane.
Proteini slični GFP-u pronađeni su u više vrsta morskih Copepoda, posebno iz porodica Pontellidae i Aetideidae.[14] GFP izolovan iz Pontella mimocerami pokazao je visok nivo sjaja sa kvantnim prinosom od 0,92, što ih čini skoro dvostruko svetlijim od obično korišćenog EGFP izolovanog iz A. victoria.[15]
Struktura[uredi | uredi izvor]
GFP ima beta-barelnu strukturu koja se sastoji od jedanaest β-lanaca sa nabranim rasporedom beta-listova, sa alfa-heliksom koji sadrži kovalentno vezan hromofor 4-(p-hidroksibenziliden)imidazolidin-5- jedan (HBI) koji prolazi kroz centar.[3][9][10] Pet kraćih alfa-heliksa formiraju kape na krajevima strukture. Beta-barelna struktura je skoro savršen cilindar, 42Å dug i 24Å u prečniku (neke studije su prijavile prečnik od 30Å[11]),[9] stvarajući ono što se naziva "β-kan" formacija, koja je jedinstvena za porodicu sličnih GFP-u.[10] HBI, spontano modifikovani oblik tripeptida Ser65–Tyr66–Gly67, nije fluorescentan u odsustvo pravilno presavijene GFP skele i postoji uglavnom u neionizovanom obliku fenola u wtGFP.[16] Bočni lanci cijevi okrenuti prema unutra indukuju specifične reakcije ciklizacije u Ser65–Tyr66–Gly67 koje indukuju ionizaciju HBI u fenolatnu formu i formiranje hromofora. Ovaj proces posttranslacijske modifikacije naziva se sazrevanjem.[17] Mreža vodikove veze i interakcije slaganja elektrona sa ovim bočnim lancima utiču na boju, intenzitet i fotostabilnost GFP-a i njegovih brojnih derivata.[18] Čvrsto zbijena priroda barela isključuje molekule rastvarača, štiteći hromoforsku fluorescenciju od gašenja vodom. Pored autociklizacije Ser65-Tyr66-Gly67, reakcija 1,2-dehidrogenacije se dešava na ostatku Tyr66.[11] Pored tri ostatka koja formiraju hromofor, ostaci kao što je Gln94 , Arg96, His148, Thr203 i Glu222 djeluju kao stabilizatori. Ostaci Gln94, Arg96 i His148 su u stanju da se stabilizuju delokalizacijom naboja hromofora. Arg96 je najvažniji stabilizirajući ostatak zbog činjenice da potiče potrebna strukturna preusmjeravanja koja su neophodna iz HBI prstena. Svaka mutacija na ostatku Arg96 bi rezultirala smanjenjem brzine razvoja hromofora jer bi se izgubile pravilne elektrostatske i sterne interakcije. Tyr66 je primatelj vodikova veza|vodikovih veza]] i ne ionizira kako bi proizveo povoljnu elektrostatiku.[19]

| [[slika:Gfp and fluorophore.png|thumb|300px|Molekule GFP u stilu crtanog filma, jedan u lpotpunosti, a jedan sa odsječenom stranom beta-barela, kako bi se otkrio hromofor (istaknut kao [[model lopte i štapa]) ]). Prma 1GFL.]] | 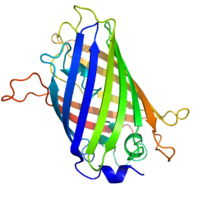 |
Autocatalitsko formiranje hromofora u wtGFP[uredi | uredi izvor]
 Mehanički, proces uključuje ciklizaciju posredovanu bazom praćenu dehidratacijom i oksidacijom. U reakciji od 7a do 8 dolazi do stvaranja enamina iz imina, dok se u reakciji od 7b do 9 apstrahuje proton.[20] Formirani HBI fluorofor je označen zelenom bojom.
Mehanički, proces uključuje ciklizaciju posredovanu bazom praćenu dehidratacijom i oksidacijom. U reakciji od 7a do 8 dolazi do stvaranja enamina iz imina, dok se u reakciji od 7b do 9 apstrahuje proton.[20] Formirani HBI fluorofor je označen zelenom bojom.
Reakcije su katalizirane ostacima Glu222 i Arg96.[20][21] Analogni mehanizam je također moguć sa treoninom umjesto Ser65.
Transgeni kućni ljubimci[uredi | uredi izvor]

Alba, zeleno-fluorescentni zec, stvoren je u francuskoj laboratoriji koju je naručio Eduardo Kac koristeći GFP za potrebe umjetnosti i društvenog komentara.[22] Američka kompanija Yorktown Technologies prodaje akvarijske zelene fluorescentne zebrice (GloFish) koje su prvobitno razvijene za otkrivanje zagađenja u vodenim putevima. NeonPets, kompanija sa sjedištem u SAD-u, reklamirala je zelene fluorescentne miševe industriji kućnih ljubimaca kao NeonMice.[23] Zelene fluorescentne svinje, poznate kao Noels, uzgajala je grupa istraživača pod vodstvom Wu Shinn-Chiha na Odsjeku za nauku o životinjama i tehnologiju na Nacionalnom univerzitetu Tajvana.[24] Japansko-američki tim stvorio je zeleno-fluorescentne mačke kao dokaz koncepta kako bi ih potencijalno koristio kao uzorne organizme za bolesti, posebno HIV.[25] U 2009. južnokorejski tim sa Nacionalnog univerziteta u Seulu uzgojio je prve transgene biglove sa ćelijama fibroblasta iz morskih anemona. Psi emituju crveno fluorescentno svjetlo, a trebali bi omogućiti naučnicima da proučavaju gene koji uzrokuju ljudske bolesti poput narkolepsija i sljepila.[26]
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Ormö M, Cubitt AB, Kallio K, Gross LA, Tsien RY, Remington SJ (septembar 1996). "Crystal structure of the Aequorea victoria green fluorescent protein". Science. 273 (5280): 1392–5. Bibcode:1996Sci...273.1392O. doi:10.1126/science.273.5280.1392. PMID 8703075. S2CID 43030290.
- ^ Prendergast FG, Mann KG (Aug 1978). "Chemical and physical properties of aequorin and the green fluorescent protein isolated from Aequorea forskålea". Biochemistry. 17 (17): 3448–53. doi:10.1021/bi00610a004. PMID 28749.
- ^ a b c Tsien RY (1998). "The green fluorescent protein" (PDF). Annual Review of Biochemistry. 67: 509–44. doi:10.1146/annurev.biochem.67.1.509. PMID 9759496.
- ^ Salih A (2019). "Fluorescent Proteins". u Cox G (ured.). Fundamentals of Fluorescence Imaging. Boca Raton: Jenny Stanford Publishing. str. 122. doi:10.1201/9781351129404. ISBN 9781351129404. S2CID 213688192.
- ^ Stepanenko OV, Verkhusha VV, Kuznetsova IM, Uversky VN, Turoverov KK (Aug 2008). "Fluorescent proteins as biomarkers and biosensors: throwing color lights on molecular and cellular processes". Current Protein & Peptide Science. 9 (4): 338–69. doi:10.2174/138920308785132668. PMC 2904242. PMID 18691124.
- ^ Phillips GJ (Oct 2001). "Green fluorescent protein--a bright idea for the study of bacterial protein localization". FEMS Microbiology Letters. 204 (1): 9–18. doi:10.1016/S0378-1097(01)00358-5. PMID 11682170.
- ^ Uckert W, Pedersen L, Günzburg W (2000). "Green fluorescent protein retroviral vector: generation of high-titer producer cells and virus supernatant". Methods in Molecular Medicine. 35: 275–85. doi:10.1385/1-59259-086-1:275. ISBN 1-59259-086-1. PMID 21390811.
- ^ Goodman SR, ured. (2008). "Chapter 1 - Tools of the Cell Biologist: Green Fluorescent Protein". Medical Cell Biology (3rd izd.). Amsterdam: Elsevier/Academic Press. str. 14–25. doi:10.1016/B978-0-12-370458-0.50006-2. ISBN 978-0-12-370458-0. S2CID 90224559.
- ^ a b c Ormö M, Cubitt AB, Kallio K, Gross LA, Tsien RY, Remington SJ (Sep 1996). "Crystal structure of the Aequorea victoria green fluorescent protein". Science. 273 (5280): 1392–5. Bibcode:1996Sci...273.1392O. doi:10.1126/science.273.5280.1392. PMID 8703075. S2CID 43030290.
- ^ a b c Yang F, Moss LG, Phillips GN (Oct 1996). "The molecular structure of green fluorescent protein" (PDF). Nature Biotechnology. 14 (10): 1246–51. doi:10.1038/nbt1096-1246. hdl:1911/19233. PMID 9631087. S2CID 34713931.
- ^ a b c Brejc K, Sixma TK, Kitts PA, Kain SR, Tsien RY, Ormö M, Remington SJ (mart 1997). "Structural basis for dual excitation and photoisomerization of the Aequorea victoria green fluorescent protein". Proceedings of the National Academy of Sciences of the United States of America. 94 (6): 2306–2311. Bibcode:1997PNAS...94.2306B. doi:10.1073/pnas.94.6.2306. PMC 20083. PMID 9122190.
- ^ Zacharias DA, Violin JD, Newton AC, Tsien RY (maj 2002). "Partitioning of lipid-modified monomeric GFPs into membrane microdomains of live cells". Science. 296 (5569): 913–16. Bibcode:2002Sci...296..913Z. doi:10.1126/science.1068539. PMID 11988576. S2CID 14957077.
- ^ Yue JX, Holland ND, Holland LZ, Deheyn DD (juni 2016). "The evolution of genes encoding for green fluorescent proteins: insights from cephalochordates (amphioxus)". Scientific Reports. 6 (1): 28350. Bibcode:2016NatSR...628350Y. doi:10.1038/srep28350. PMC 4911609. PMID 27311567.
- ^ Hunt ME, Scherrer MP, Ferrari FD, Matz MV (juli 2010). "Very bright green fluorescent proteins from the Pontellid copepod Pontella mimocerami". PLOS ONE. 5 (7): e11517. Bibcode:2010PLoSO...511517H. doi:10.1371/journal.pone.0011517. PMC 2904364. PMID 20644720.
- ^ "eGFP". FPbase.
- ^ Bokman SH, Ward WW (1982). "Reversible denaturation of Aequorea green-fluorescent protein: physical separation and characterization of the renatured protein". Biochemistry. 21 (19): 4535–4540. doi:10.1021/bi00262a003. PMID 6128025.
- ^ Pouwels LJ, Zhang L, Chan NH, Dorrestein PC, Wachter RM (Sep 2008). "Kinetic isotope effect studies on the de novo rate of chromophore formation in fast- and slow-maturing GFP variants". Biochemistry. 47 (38): 10111–22. doi:10.1021/bi8007164. PMC 2643082. PMID 18759496.
- ^ Chudakov DM, Matz MV, Lukyanov S, Lukyanov KA (Jul 2010). "Fluorescent proteins and their applications in imaging living cells and tissues". Physiological Reviews. 90 (3): 1103–63. doi:10.1152/physrev.00038.2009. PMID 20664080. S2CID 10767597.
- ^ Stepanenko OV, Verkhusha VV, Shavlovsky MM, Kuznetsova IM, Uversky VN, Turoverov KK (novembar 2008). "Understanding the role of Arg96 in structure and stability of green fluorescent protein". Proteins. 73 (3): 539–551. doi:10.1002/prot.22089. PMC 2908022. PMID 18470931.
- ^ a b Rosenow MA, Huffman HA, Phail ME, Wachter RM (april 2004). "The crystal structure of the Y66L variant of green fluorescent protein supports a cyclization-oxidation-dehydration mechanism for chromophore maturation". Biochemistry. 43 (15): 4464–4472. doi:10.1021/bi0361315. PMID 15078092.
- ^ Ma Y, Yu JG, Sun Q, Li Z, Smith SC (1. 7. 2015). "The mechanism of dehydration in chromophore maturation of wild-type green fluorescent protein: A theoretical study". Chemical Physics Letters (jezik: engleski). 631–632: 42–46. Bibcode:2015CPL...631...42M. doi:10.1016/j.cplett.2015.04.061. ISSN 0009-2614.
- ^ Kac E. "GFP Bunny".
- ^ "Glow-In-The Dark NeonMice". Arhivirano s originala, 14. 2. 2009. Pristupljeno 30. 8. 2016.
- ^ Scientists in Taiwan breed fluorescent green pigs
- ^ Wongsrikeao P, Saenz D, Rinkoski T, Otoi T, Poeschla E (2011). "Antiviral restriction factor transgenesis in the domestic cat". Nature Methods. 8 (10): 853–9. doi:10.1038/nmeth.1703. PMC 4006694. PMID 21909101.
- ^ "Fluorescent puppy is world's first transgenic dog".
Dopunska literatura[uredi | uredi izvor]
- Pieribone V, Gruber D (2006). Aglow in the Dark: The Revolutionary Science of Biofluorescence. Cambridge: Belknap Press. ISBN 978-0-674-01921-8. OCLC 60321612. Popular science book describing history and discovery of GFP
- Zimmer M (2005). Glowing Genes: A Revolution In Biotechnology. Buffalo, NY: Prometheus Books. ISBN 978-1-59102-253-4. OCLC 56614624.
Vanjski linkovi[uredi | uredi izvor]
| Library resources about Zeleni fluorescentni protein |
| Commons ima datoteke na temu: Zeleni fluorescentni protein |
- A comprehensive article on fluorescent proteins at Scholarpedia
- Brief summary of landmark GFP papers
- Interactive Java applet demonstrating the chemistry behind the formation of the GFP chromophore
- Video of 2008 Nobel Prize lecture of Roger Tsien on fluorescent proteins
- Excitation and emission spectra for various fluorescent proteins
- Green Fluorescent Protein Chem Soc Rev themed issue dedicated to the 2008 Nobel Prize winners in Chemistry, Professors Osamu Shimomura, Martin Chalfie and Roger Y. Tsien
- Molecule of the Month, June 2003: an illustrated overview of GFP by David Goodsell.
- Molecule of the Month, June 2014: an illustrated overview of GFP-like variants by David Goodsell.
- Green Fluorescent Protein on FPbase, a fluorescent protein database
- P42212

