Fosfor-trijodid
| Fosfor-trijodid | |
|---|---|
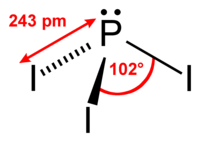  | |
| Općenito | |
| Hemijski spoj | Fosfor-trijodid |
| Druga imena | Triiodofosfin IUPAC ime: Fosfor trijodid Fosfor(III) jodid |
| Molekularna formula | PI3 |
| CAS registarski broj | 13455-01-1 |
| SMILES | IP(I)I |
| InChI | 1/I3P/c1-4(2)3 |
| Kratki opis | Tamno crvena čvrsta supstanca |
| Osobine1 | |
| Molarna masa | 411,68717 g/mol |
| Agregatno stanje | Čvrsto |
| Gustoća | 4,18 g/cm3 |
| Tačka topljenja | 61,2 |
| Tačka ključanja | 200 |
| Rastvorljivost | Razlaže se |
| Rizičnost | |
| NFPA 704 | |
| 1 Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
Fosfor-trijodid (PI3) je tamno crveni čvrsti hemijski spoj koji se široko primjenjuje u hemijskoj industriji.
Navodi da je to nestabilna crvena čvrsta supstanca koja burno reagira s vodom i da ga je suviše nestabilan za skladištenje – uobičajena su zabluda.[1] PI3 je, u stvari, komercijalno dostupan i naširoko se koristi u organskoj hemiji za prevođenje alkohola do alkil-jodida. To je također snažno redukcijsko sredstvo. Treba također znati da fosfor formira i niže jodide, P2I4, ali postojanost PI5 je upitna na sobnoj temperaturi.
Osobenosti[uredi | uredi izvor]
PI3 u biti ima nulti dipolni moment u otopini ugljik-disulfida, jer P-I veza gotovo da i nema dipol. P-I veza je slaba; PI3 mnogo je manje stabilan od PBr3 i PCl3 , s standardnom entalpijom nastajanja za PI3 od samo –46 kJ / mol (čvrsti). Atom fosfora ima hemijski pomak NMR od 178 ppm (niz polje od H3PO4).
Reakcije[uredi | uredi izvor]
Fosfor-trijodid snažno reagira s vodom, proizvodeći fosfornu (H3PO3) hidrojodnu kiselinu (HI), sa manjom količinom fosfina i P-P spojeva. Sa alkoholima isto tako formira alkil-jodide, što omogućava glavnu upotrebu PI3.
PI3 ije također moćan reducirajući i dezoksigenirajući agens. Reducira sulfokside do tioetera, čak i na −78 °C.[2] U međuvremenu, zagrijavanje otopine 1-jodobutana PI3 sa crvenim fosforom izaziva redukciju do P2I4.
Dobijanje[uredi | uredi izvor]
Uobičajeni metod dobijanja fosfor-jodida je spajanje dva elementa, često putem dodavanja jodina na otopinu bijelog fosfora u ugljik-disulfidu:
- P4 + 6 I2 → 4 PI3.
Alternativno, PCl3 može biti pretvoren u PI3 djelovanjem vodik-jodida ili nekih metalnih jodida.
Upotreba[uredi | uredi izvor]
Fosfor-jodid se obično koristi u laboratorijama za konverziju primarnih ili sekundarnih alkohola do alkil-jodida.[3] Alkohol se često upotrebljava kao otapalo i vrhunski reaktant. Ćesto se PI3 pravi in situ, reakcijom crvenog fosfora sa jodinom, u prisustvu alkohola; primjerice, pretvaranje metanola u jodometan:[4]
- PI3 + 3 CH3OH → 3 CH3I + H3PO3
Ovi alkil-jodidi su upotrebljivi spojevi za reakcije nukleofilne supstitucije i za pripremanje Grignardovih reagenasa.
Rakođer pogledajte[uredi | uredi izvor]
- Dušik-trijodid
- Difosfor-tetrajodid
- Fosfor- trifluorid
- Fosfor-trihlorid
- Fosfor-tribromid
- Fosfor-pentajodid
Reference[uredi | uredi izvor]
- ^ L. G. Wade, Jr., Organic Chemistry, 6th ed., p. 477, Pearson/Prentice Hall, Upper Saddle River, New Jersey, USA, 2005.
- ^ J. N. Denis; A. Krief (1980). "Phosphorus tri-iodide (PI3), a powerful deoxygenating agent". J. Chem. Soc., Chem. Commun. (12): 544–5. doi:10.1039/C39800000544.
- ^ B. S. Furnell et al., Vogel's Textbook of Practical Organic Chemistry, 5th edition, Longman/Wiley, New York, 1989.
- ^ King, C. S., Hartman, W. W. (1943): Methyl Iodide. orgSint, 2: 399 - CV2P0399.
Vanjski linkovi[uredi | uredi izvor]
| Phosphorus triiodide na Wikimedia Commonsu. |


