Hemoglobin A

Hemoglobin A (HbA), znan i kao hemoglobin odraskih, hemoglobin A1 ili α2β2, je najčešći ljudski hemoglobinski tetramer, čineći preko 97% ukupnog hemoglobina crvenih krvnih zrnaca.[1] Hemoglobin je protein koji veže kisik i nalazi se u eritrocitima, koji transportuju kiseik iz pluća u tkiva.[2] Hemoglobin A je najčešći oblik hemoglobina kod odraslih i postoji kao tetramer koji sadrži po dvije alfa i beta podjedinice (α2β2).[3] Hemoglobin A2 (HbA2) je rjeđi oblik hemoglobina odraslih i sastoji se od po dvije alfa i delta-globinske podjedinice. Ovaj hemoglobin čini 1-3% hemoglobina kod odraslih.[4]
Struktura i funkcija
[uredi | uredi izvor]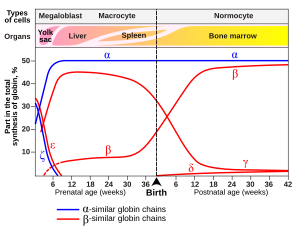
Hemoglobin A (HbA) najčešći je oblik hemoglobina odraslih i postoji kao tetramer koji sadrži po dvije alfa i beta podjedinice (α2β2).[3] Svaka podjedinica sadrži grupu hema na koju se mogu vezati dvoatomske molekule kisika (O2).[5] Osim kisika, poznato je da sklop podjedinice i kvaternarna struktura imaju važnu ulogu u afinitetu Hb. Kada se hemoglobin veže za O2 (oksihemoglobin), vezat će se za gvožđe II (Fe2+) hema i upravo taj ion može vezati i osloboditi kisik za transport kroz tijelo. Da bi hemoglobin u normalnim uvjetima mogao pokupiti i osloboditi kisik, moraju biti prisutne sve podjedinice.[6]
Sinteza
[uredi | uredi izvor]
Sinteza hema
[uredi | uredi izvor]Sinteza hema uključuje niz enzimskih koraka koji se odvijaju u mitohondrijama i citosolu ćelije. Prvo, u mitohondrijama, dolazi do kondenzacije sukcinil CoA i glicina, pomoću ALA sintaza, da bi se proizvela 5-aminolevulinska kiselina (ALA). ALA se zatim prebacuje u citosol i, nakon niza reakcija, stvara koproporfirinogen III. Ova molekula vraća se u mitohondriju, gde reaguje sa protoporfirin-III oksidazama dajući protoporfirin IX. Zatim se gvožđe enzimski ubacuje u protoporfirin putem, ferohaletaze, da bi se dobio hem.[7]
Sinteza globina
[uredi | uredi izvor]Sinteza globina odvija se u ribosomima, koji se nalaze unutar citosola. Dva lanca globina koji imaju hen-grupe kombiniraju se u hemoglobin. Jedan od lanaca je alfa, a drugi nealfa lanac. Priroda ne-alfa lanca u molekulama hemoglobina varira zbog različitih varijabli. Fetusi imaju ne-alfa lanac koji se naziva gama, a nakon rođenja tada se naziva beta. Beta-lanac će se upariti s alfa lancem. Kombinacija dva alfa i nealfa lanca stvara molekulu hemoglobina. Dva alfa i dva gama lanca formiraju fetusni hemoglobin ili hemoglobin F (HbF). Nakon prvih pet do šest mjeseci nakon rođenja, kombinacija po dva alfa i beta lanca formira hemoglobin odraslih (HbA). Geni koji kodiraju alfa lance nalaze se na hromosomu 16, dok se geni koji kodiraju alfa lance nalaze na hromosomu 11.[7]
Također pogledajte
[uredi | uredi izvor]Reference
[uredi | uredi izvor]- ^ "Hemoglobinopathies". Pristupljeno 6. 2. 2009.
- ^ Farid, Yostina; Lecat, Paul (2019), "Biochemistry, Hemoglobin Synthesis", StatPearls, StatPearls Publishing, PMID 30725597, pristupljeno 10. 4. 2019
- ^ a b Immigrant medicine. Walker, Patricia Frye., Barnett, Elizabeth D. (Elizabeth Day). St. Louis, Mo.: Elsevier Mosby. 2007. ISBN 9780323034548. OCLC 489070888.CS1 održavanje: others (link)
- ^ Kato, Gregory J.; Piel, Frédéric B.; Reid, Clarice D.; Gaston, Marilyn H.; Ohene-Frempong, Kwaku; Krishnamurti, Lakshmanan; Smith, Wally R.; Panepinto, Julie A.; Weatherall, David J. (15. 3. 2018). "Sickle cell disease" (PDF). Nature Reviews Disease Primers. 4: 18010. doi:10.1038/nrdp.2018.10. hdl:10044/1/57817. ISSN 2056-676X. PMID 29542687. S2CID 3870507.
- ^ Barrick, Doug; Lukin, Jonathan A; Simplaceanu, Virgil; Ho, Chien (2004), "Nuclear Magnetic Resonance Spectroscopy in the Study of Hemoglobin Cooperativity", Methods in Enzymology, Elsevier, 379: 28–54, doi:10.1016/s0076-6879(04)79002-3, ISBN 9780121827830, PMID 15051350
- ^ "Hemoglobin Overview". sickle.bwh.harvard.edu. Pristupljeno 10. 4. 2019.
- ^ a b "Hemoglobin Synthesis". sickle.bwh.harvard.edu. Pristupljeno 11. 4. 2019.
Vanjski linkovi
[uredi | uredi izvor]- Hemoglobin A na US National Library of Medicine Medical Subject Headings (MeSH)
