Plazmin
Plazmin, sa svojim prekursorom zvamim plazminogen, jest značajan enzim (EC: 3.4.21.7) u krvi, koji razlaže mnoge plazmatske proteine, uključujući i fibrin krvnih pločica. Razgradnja fibrina naziva se fibrinoliza. Kod ljudi kodiran je genom PLG.[5]
Aminokiselinska sekvenca[uredi | uredi izvor]
Dužina polipeptidnog lanca je 810 aminokiselina, а molekulska težina 90.569 Da.[6]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MEHKEVVLLL | LLFLKSGQGE | PLDDYVNTQG | ASLFSVTKKQ | LGAGSIEECA | ||||
| AKCEEDEEFT | CRAFQYHSKE | QQCVIMAENR | KSSIIIRMRD | VVLFEKKVYL | ||||
| SECKTGNGKN | YRGTMSKTKN | GITCQKWSST | SPHRPRFSPA | THPSEGLEEN | ||||
| YCRNPDNDPQ | GPWCYTTDPE | KRYDYCDILE | CEEECMHCSG | ENYDGKISKT | ||||
| MSGLECQAWD | SQSPHAHGYI | PSKFPNKNLK | KNYCRNPDRE | LRPWCFTTDP | ||||
| NKRWELCDIP | RCTTPPPSSG | PTYQCLKGTG | ENYRGNVAVT | VSGHTCQHWS | ||||
| AQTPHTHNRT | PENFPCKNLD | ENYCRNPDGK | RAPWCHTTNS | QVRWEYCKIP | ||||
| SCDSSPVSTE | QLAPTAPPEL | TPVVQDCYHG | DGQSYRGTSS | TTTTGKKCQS | ||||
| WSSMTPHRHQ | KTPENYPNAG | LTMNYCRNPD | ADKGPWCFTT | DPSVRWEYCN | ||||
| LKKCSGTEAS | VVAPPPVVLL | PDVETPSEED | CMFGNGKGYR | GKRATTVTGT | ||||
| PCQDWAAQEP | HRHSIFTPET | NPRAGLEKNY | CRNPDGDVGG | PWCYTTNPRK | ||||
| LYDYCDVPQC | AAPSFDCGKP | QVEPKKCPGR | VVGGCVAHPH | SWPWQVSLRT | ||||
| RFGMHFCGGT | LISPEWVLTA | AHCLEKSPRP | SSYKVILGAH | QEVNLEPHVQ | ||||
| EIEVSRLFLE | PTRKDIALLK | LSSPAVITDK | VIPACLPSPN | YVVADRTECF | ||||
| ITGWGETQGT | FGAGLLKEAQ | LPVIENKVCN | RYEFLNGRVQ | STELCAGHLA | ||||
| GGTDSCQGDS | GGPLVCFEKD | KYILQGVTSW | GLGCARPNKP | GVYVRVSRFV | ||||
| TWIEGVMRNN |
Funkcija[uredi | uredi izvor]

Plazmin je serin-proteaza koja djeluje tako darazlaže fibrinske krvne ugruške. Osim fibrinolize, plazminski proteini obavljaju proteolizu u raznim drugim sistemima: aktiviraju kolagenaze, neke posrednike komplementarnog sistema i slabi zid Graafovog folikula , što dovodi do ovulacija. Plazmin je također integralno uključen u upale.[7] On cijepa fibrin, fibronektin, trombospondin, laminin i von Willebrandov faktor. Plazmin, poput tripsina, pripada porodici serin-proteaza.
Plazmin se oslobađa kao zimogen zvan plazminogen (PLG) iz jetre u sistemsku cirkulaciju. Kod ljudi, postoje dvije glavne glikoforme plazminogena – plazminogen tipa I sadrži dva glikozilacijska dijela (N-vezan za N289 i O-vezan za T346), dok plazminogen tipa II sadrži samo jedan O-vezani šećer (O-vezan za T346) . Plazminogen tipa II se prvenstveno regrutuje na ćelijsku površinu u odnosu na glikoformu tipa I. Nasuprot tome, plazminogen tipa I lakše se regrutira u krvne ugruške.
U cirkulaciji, plazminogen ima zatvorenu konformaciju otpornu na aktivaciju. Nakon vezanja za ugruške ili na ćelijsku površinu, plazminogen dobija otvoreni oblik konformacije koji se može pretvoriti u aktivni plazmin. raznim enzimma, uključujući tkivni aktivator plazminogena (tPA), urokinazni aktivator plazminogena (uPA), kalikrein i faktor XII (Hagemanov faktor). Fibrin je kofaktor za aktivaciju plazminogena tkivnim aktivatorom plazminogena. Urokinazni receptor aktivatora plazminogena (uPAR) je kofaktor za aktivaciju plazminogena aktivatorom urokinaze plazminogena. Pretvaranje plazminogena u plazmin uključuje cijepanje peptidne veze između Arg-561 i Val-562.[5][8][9][10]
Cijepanjem plazmina nastaje angiostatin.
Mehanizam aktivacije plazminogena[uredi | uredi izvor]
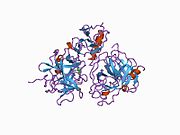
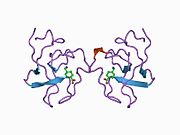
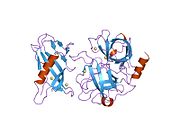
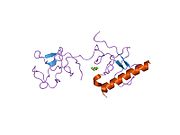
Plazminogen pune dužine sadrži sedam domena. Osim C-terminalnog domena serin-proteaze sličnog himotripsinu, plazminogen sadrži N-terminalni Pan Appleov domen (PAp), zajedno s pet Kringleovih domena (KR1-5) . Pan-Appleov domen sadrži važne odrednice za održavanje plazminogena u zatvorenom obliku, a Kringleovi domeni odgovorni su za vezivanje za ostatke lizina u receptorima i supstratima.
Rentgenska kristalna struktura zatvorenog plazminogena otkriva da domeni PAp i SP održavaju zatvorenu konformaciju kroz interakcije ostvarene u cijelom nizu Kringleovih domena.[11] Hloridni ioni dalje premošćuju sučelja PAp/KR4 i SP/KR2 , objašnjavajući fiziološku ulogu serumskog hlorida u stabilizaciji zatvorene konformacije. Strukturne studije također otkrivaju da razlike u glikozilaciji mijenjaju položaj KR3. Ovi podaci pomažu u objašnjenju funkcionalnih razlika između glikoformi plazminogena tipa I i tipa II.
U zatvorenoj konformaciji plazminogena, pristup aktivacijskoj vezi (R561/V562) ciljanoj cijepanjem pomoću tPA i uPA blokiran je kroz položaj sekvence linkera KR3/KR4 i O-vezanog šećera na T346. Položaj KR3 može također ometati pristup aktivacijskoj petlji. Interakcije između domena također blokiraju sva mjesta vezanja Kringleovog liganda osim onog KR-1, što sugerira da potonji domen upravlja regrutovanjem proenzima za ciljeve. Analiza srednje strukture plazminogena sugerira da se konformacijska promjena plazminogena u otvoreni oblik inicira kroz KR-5 prolazno se skidajući od domena PAp. Ovi pokreti izlažu mjesto vezanja lizina KR5 potencijalnim partnerima vezanja i predlažu zahtjev za prostorno različitim ostacima lizina u izazivanju regrutiranja plazminogena i konformacijske promjene.[11]
Mehanizam inaktivacije plazmina[uredi | uredi izvor]
Plazmin se inaktivira proteinima kao što su α2-makroglobulin i α2-antiplazmin.[12] Mehanizam inaktivacije plazmina uključuje cijepanje α2-makroglobulina u regiji mamca (segment aM-a koji je posebno osjetljiv na proteolitsko cijepanje) putem plazmina. Ovo inicira konformacijsku promjenu, tako da se α2-makroglobulin ppostavlja oko plazmina. U rezultirajućem kompleksu α2-makroglobulin-plazmin, aktivno mjesto plazmina je sterno zaštićeno, čime se značajno smanjuje pristup plazmina proteinskim supstratima. Dva dodatna događaja dešavaju se kao posljedica cijepanja regije mamaca, i to (1) h-cisteinil-g-glutamil tiol ester α2-makroglobulin postaje visoko reaktivan i (2) velika konformacijska promjena izlaže konzervirano COOH-terminalno vezanje receptorskog domena. Izloženost ovog domena koji veže receptore omogućava kompleksu α2-makroglobulinske proteaze da se veže za receptore klirensa i ukloni iz cirkulacije.
Klinički značaj[uredi | uredi izvor]
Nedostatak plazmina može dovesti do tromboza, jer ugrušci nisu adekvatno razgrađeni. Nedostatak plazminogena kod miševa dovodi do oštećenja jetre,[13] neispravnog zarastanja rana, reproduktivne abnormalnosti.
Kod ljudi je rijedak poremećaj koji se naziva nedostatak plazminogena tip I (OMIM: 217090) uzrokovan mutacijama PLG gena i često se manifestira lignusni konjunktivitis.
Interakcije[uredi | uredi izvor]
Pokazalo se da plazmin ima interakcije sa:
- Trombospondinom 1,[14][15]
- Alfa 2-antiplazminom[16][17] i
- IGFBP3.[18]
Plazmin inducira generiranje bradikinina kod miševa i ljudi putem cijepanja - Kininogena velike molekulske težine.[19]
Reference[uredi | uredi izvor]
- ^ a b c GRCh38: Ensembl release 89: ENSG00000122194 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000059481 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b "Entrez Gene: plasminogen".
- ^ "UniProt, P00747" (jezik: engleski). Pristupljeno 9. 10. 2021.
- ^ Atsev S, Tomov N (decembar 2020). "Using antifibrinolytics to tackle neuroinflammation". Neural Regeneration Research. 15 (12): 2203–2206. doi:10.4103/1673-5374.284979. PMC 7749481. PMID 32594031.
- ^ Miyata T, Iwanaga S, Sakata Y, Aoki N (oktobar 1982). "Plasminogen Tochigi: inactive plasmin resulting from replacement of alanine-600 by threonine in the active site". Proc. Natl. Acad. Sci. U.S.A. 79 (20): 6132–6. Bibcode:1982PNAS...79.6132M. doi:10.1073/pnas.79.20.6132. PMC 347073. PMID 6216475.
- ^ Forsgren M, Råden B, Israelsson M, Larsson K, Hedén LO (mart 1987). "Molecular cloning and characterization of a full-length cDNA clone for human plasminogen". FEBS Lett. 213 (2): 254–60. doi:10.1016/0014-5793(87)81501-6. PMID 3030813. S2CID 9075872.
- ^ Law RH, Caradoc-Davies T, Cowieson N, Horvath AJ, Quek AJ, Encarnacao JA, Steer D, Cowan A, Zhang Q, Lu BG, Pike RN, Smith AI, Coughlin PB, Whisstock JC (2012). "The X-ray crystal structure of full-length human plasminogen". Cell Rep. 1 (3): 185–90. doi:10.1016/j.celrep.2012.02.012. PMID 22832192.
- ^ a b Law RH, Caradoc-Davies T, Cowieson N, Horvath AJ, Quek AJ, Encarnacao JA, Steer D, Cowan A, Zhang Q, Lu BG, Pike RN, Smith AI, Coughlin PB, Whisstock JC (2012). "The X-ray crystal structure of full-length human plasminogen". Cell Rep. 1 (3): 185–90. doi:10.1016/j.celrep.2012.02.012. PMID 22832192.
- ^ Wu, Guojie; Quek, Adam J.; Caradoc-Davies, Tom T.; Ekkel, Sue M.; Mazzitelli, Blake; Whisstock, James C.; Law, Ruby H.P. (5. 3. 2019). "Structural studies of plasmin inhibition". Biochemical Society Transactions. 47 (2): 541–557. doi:10.1042/bst20180211. ISSN 0300-5127. PMID 30837322.
- ^ Bezerra JA, Bugge TH, Melin-Aldana H, Sabla G, Kombrinck KW, Witte DP, Degen JL (21. 12. 1999). "Plasminogen deficiency leads to impaired remodeling after a toxic injury to the liver". Proc. Natl. Acad. Sci. U.S.A. Proceedings of the National Academy of Sciences of the United States of America. 96 (26): 15143–8. Bibcode:1999PNAS...9615143B. doi:10.1073/pnas.96.26.15143. PMC 24787. PMID 10611352.
- ^ Silverstein RL, Leung LL, Harpel PC, Nachman RL (novembar 1984). "Complex formation of platelet thrombospondin with plasminogen. Modulation of activation by tissue activator". J. Clin. Invest. 74 (5): 1625–33. doi:10.1172/JCI111578. PMC 425339. PMID 6438154.
- ^ DePoli P, Bacon-Baguley T, Kendra-Franczak S, Cederholm MT, Walz DA (mart 1989). "Thrombospondin interaction with plasminogen. Evidence for binding to a specific region of the kringle structure of plasminogen". Blood. 73 (4): 976–82. doi:10.1182/blood.V73.4.976.976. PMID 2522013.
- ^ Wiman B, Collen D (septembar 1979). "On the mechanism of the reaction between human alpha 2-antiplasmin and plasmin". J. Biol. Chem. 254 (18): 9291–7. doi:10.1016/S0021-9258(19)86843-6. PMID 158022.
- ^ Shieh BH, Travis J (maj 1987). "The reactive site of human alpha 2-antiplasmin". J. Biol. Chem. 262 (13): 6055–9. doi:10.1016/S0021-9258(18)45536-6. PMID 2437112.
- ^ Campbell PG, Durham SK, Suwanichkul A, Hayes JD, Powell DR (august 1998). "Plasminogen binds the heparin-binding domain of insulin-like growth factor-binding protein-3". Am. J. Physiol. 275 (2 Pt 1): E321-31. doi:10.1152/ajpendo.1998.275.2.E321. PMID 9688635.
- ^ Marcos-Contreras OA, Martinez de Lizarrondo S, Bardou I, Orset C, Pruvost M, Anfray A, Frigout Y, Hommet Y, Lebouvier L, Montaner J, Vivien D, Gauberti M (august 2016). "Hyperfibrinolysis increases blood brain barrier permeability by a plasmin and bradykinin-dependent mechanism". Blood. 128 (20): 2423–2434. doi:10.1182/blood-2016-03-705384. PMID 27531677.
Dopunska literatura[uredi | uredi izvor]
- Shanmukhappa K, Mourya R, Sabla GE, Degen JL, Bezerra JA (juli 2005). "Hepatic to pancreatic switch defines a role for hemostatic factors in cellular plasticity in mice". Proc. Natl. Acad. Sci. U.S.A. 102 (29): 10182–7. Bibcode:2005PNAS..10210182S. doi:10.1073/pnas.0501691102. PMC 1177369. PMID 16006527.
- Anglés-Cano E, Rojas G (2002). "Apolipoprotein(a): structure-function relationship at the lysine-binding site and plasminogen activator cleavage site". Biol. Chem. 383 (1): 93–9. doi:10.1515/BC.2002.009. PMID 11928826. S2CID 29248198.
- Ranson M, Andronicos NM (2003). "Plasminogen binding and cancer: promises and pitfalls". Front. Biosci. 8 (6): s294-304. doi:10.2741/1044. PMID 12700073.
Vanjski linkovi[uredi | uredi izvor]
- The MEROPS online database for peptidases and their inhibitors: S01.233 Arhivirano 13. 9. 2019. na Wayback Machine
- Plasmin na US National Library of Medicine Medical Subject Headings (MeSH)
Ovaj članak uključuje tekst iz Nacionalne medicinske biblioteke Sjedinjenih Država, koji je u javnom vlasništvu.