Konjugirani sistem



U hemiji, konjugirani sistem je sistem povezanih p-orbitala sa delokaliziranim elektronima u molekuli, koji općenito smanjuje ukupnu energiju molekule i povećava stabilnost. Ona konvencijski predstavljena ima naizmenične jednostruke i višestruke veze. Usamljeni parovi, radikali ili karbenij ioni mogu biti dio sistema, koji može biti ciklični, aciklički, linearni ili mješoviti. Termin "konjugirani" skovao je njemački hemičar Johannes Thiele. 1899.[1]
Konjugacija je preklapanje jedne p-orbitale s drugom, preko susjedne σ-veze (u prelaznim metalima mogu biti uključene i d-orbitale). Konjugirani sistem ima područje preklapanja p-orbitala, premošćujući međusobne lokacije, za koje jednostavni dijagrami pokazuju da nemaju π-vezu. Omogućuju delokalizaciju π-elektrona kroz sve susjedne poravnate p-orbitale.[2] Elektroni π ne pripadaju jednoj vezi ili atomu, već grupi atoma.
Najveći konjugirani sistemi nalaze se u grafenu, grafitu, provodljivom polimeru i ugljičnim nanocijevima .
Hemijsko vezanje u konjugiranim sistemima[uredi | uredi izvor]

Gornji red: piridin, furan, kation tropilija.
Drugi red: alil radikal, acetatni ion, akrolein.
Uključeni atomi su podebljano crvene boje, dok su elektroni uključeni u delokaliziranu vezu plavom bojom.
(Posebnu pažnju treba obratiti na uključenost ili neuključenost "nevezujućih" elektrona.)
Konjugacija je moguća pomoću naizmjeničnih jednostrukih i dvostrukih veza, u kojima svaki atom isporučuje p-orbitalu okomito na ravan molekule. Međutim, to nije jedini način da se dogodi konjugacija. Sve dok svaki susjedni atom u lancu ima dostupnu p-orbitalu, sistem se može smatrati konjugiranim. Naprimjer, furan je peteročlani prsten s dvije naizmjenične dvostruke veze koje okružuju kisik u peteročlanom prstenu. Kisik ima dva usamljena para, od kojih jedan zauzima p-orbitalu okomito na prsten u tom položaju, održavajući tako konjugaciju tog petočlanog prstena, preklapanjem sa okomitom p-orbitalom na svakom od susjednih atoma ugljika. Drugi usamljeni par ostaje u ravni i ne sudjeluje u konjugaciji.
Općenito, svaki sp2 ili sp-hibridizirani ugljik ili heteroatom, uključujući one koji nose praznu orbitalu ili usamljeni par orbitala, mogu sudjelovati u konjugiranim sistemima, iako usamljeni parovi ne sudjeluju uvijek. Naprimjer, piridinski atom dušika već sudjeluje u konjugiranom sistemu formalnom dvostrukom vezom sa susjednim ugljikm, pa usamljeni par ostaje u ravni prstena u sp 2 hibridnoj orbitali i ne učestvuje u konjugaciji. Zahtjev za konjugaciju je preklapanje orbite; prema tome, konjugirani sistem mora biti ravan (ili gotovo takav). Kao posljedica toga, usamljeni parovi koji sudjeluju u konjugiranim sistemima zauzet će orbitale čistog p-karaktera umjesto spn hibridnih orbitala tipskih za nekonjugirane usamljene parove.

Jedan od usamljenih parova kisika učestvuje u konjugaciji u ap-orbitali, dok je drugi usamljeni par u sp2 hibridiziranoj orbitali u ravni molekule a ne dijelu π sistema.
Učešće šest elektrona u π-sistemu čini furan aromatskim (vidi dolje).
Uobičajeni model za liječenje konjugiranih molekula je tretman kompozitne valentne veze / Hückel-ove molekularne orbitalne teorije (VB / HMOT), u kojem je σ-okvir molekule odvojen od π-sistema (ili sistema) molekule.
Iako se σ-veza može tretirati i delokaliziranim pristupom, obično se uzima u obzir π-veza kada se delokalizirana veza poziva u kontekstu jednostavnih organskih molekula.
Sigma (σ) okvir: σ okvir opisan je strogo lokaliziranom shemom povezivanja, a sastoji se od σ-veza nastalih u interakciji između sp3–, sp2–, i sp – hibridizirane atomske orbitale na glavnim elementima grupe (i 1s atomske orbitale na vodiku), zajedno s lokaliziranim usamljenim parovima izvedenim iz ispunjenih, nevezanih hibridnih orbitala. Interakcija koja rezultira σ-vezom poprima oblik međusobnog preklapanja većeg režnja svake hibridne orbitale (ili pojedinačnog sfernog režnja vodikove 1s orbitale). Svaka atomska orbitala doprinosi jednim elektronom, kada se orbitale u paru preklapaju da bi se stvorile dvoelektronske σ-veze ili dva elektrona kada orbitala čini usamljeni par. Sve ove lokalizirane orbitale (vezujuće i nevezujuće) nalaze se u ravnini molekule, a σ-veze uglavnom su lokalizirane između jegara duž međujezgarne osi.
Pi (π) sistem ili sistemi: Ortogonski gore opisanom σ-okviru, π-veza nastaje iznad i ispod ravni molekule u kojoj se odvija σ-veza. Sistemi π-molekule nastaju interakcijom nehibridiziranih p-atomskih orbitala na atomima koji imaju sp2– i sp-hibridizaciju. Interakcija koja rezultira π-vezom odvija se između p-orbitala koje su susjedne zahvaljujući σ-vezi koja spaja atome i poprima oblik bočnog preklapanja dvaju jednako velikih režnjeva, koji čine svaku p-orbitalu. Atomi koji su sp3 hibridizirani nemaju nehibridiziranu p-orbitalu, koja je dostupna za sudjelovanje u π-vezanju a njihovo prisustvo nužno završava π-sistem ili razdvaja dva π-sistema. Osnova p-orbitale koja učestvuje u π-sistemu može doprinijeti jednim elektronom (što odgovara polovini formalne "dvostruke veze"), dva elektrona (što odgovara delokalizoiranom "usamljenom paru") ili nula elektrona (što odgovara formalnom stanju "prazna" orbitala). Vezanjem za π-sisteme nastale iz preklapanja više od dvije p-orbitale rukuje se pomoću Hückelovog pristupa da bi se dobila nulta (kvalitativna) aproksimacija molekulskih orbitala π-simetrije koje nastaju delokaliziranim π-vezanjem.

Lewisove rezonantne strukture molekule poput diazometana mogu se prevesti u vezujuću sliku koja se sastoji od π-sistema i lokaliziranih usamljenih parova postavljenih na lokalizirani okvir σ-veza.
Ovaj jednostavan model hemijskog vezanja uspješan je za opis većine molekula normalne valencije koje se sastoje samo od elemenata s– i p-bloka, iako sistemi koji uključuju vezujuće nedostatke elektrona, uključujući neklasične karbokacije, klastere litija i bora i hipervalentne centre, zahtijevaju značajne modifikacije, u kojima se također dozvoljava delokalizacija σ-veza i možda ih je bolje tretirati kanonskim molekulskim orbitalama koje se delokaliziraju na čitavoj molekuli. Isto tako, ovaj jednostavni model neadekvatno opisuje i d– i f-blok-organe. Veze u napetim malim prstenovima (poput ciklopropana ili epoksida) nisu dobro opisane strogim razdvajanjem σ / π, jer se veza između atoma u prstenu sastoji od "savijenih veza" ili "banana veza", koje su savijene prema spolja i u prirodi su posredne između σ- i π-veza. Ipak, organska hemija često koristi jezik ovog modela da racionalizu strukturu i reaktivnost tipskih organskih spojeva.
Elektrone u konjugiranom π-sistemu dijele svi susjedni sp2 – i sp-hibridizirani atomi koji doprinose preklapanju paralelnih p-atomskih orbitala. Kao takvi, uključeni atomi i π-elektroni ponašaju se kao jedan veliki vezani sistem. Ovi sistemi se često nazivaju n- centar k- elektronske π-veze, kompaktno označeni simbolom Π k
n, da senaglasi ovo ponašanje. Naprimjer, smatra se da su delokalizirani π-elektroni u acetatnom anionu i benzenu uključeni u Π 4
3 i Π 6
6 sistem.
Svaki od njih zauzima jedan ili dva elektrona u skladu s principom aufbau i Hundovim pravilom. Prikazi preklapajućih p-orbitala, poput one za benzen u nastavku, pokazuju osnovnu p-atomsku orbitalu, prije nego što su kombinirani u molekulske orbitale. U skladu s [[[Paulijev sistem isključenja|Paulijevim principom isključenja]], preklapanje p-orbitala ne rezultira stvaranjem jedne velike MO koja sadrži više od dva elektrona.
Hückelova MO teorija je uobičajeni pristup za dobijanje slike nultog reda delokaliziranih π-molekulskih orbitala, uključujući matematički znak talasne funkcije na različitim dijelovima molekule i lokacijama čvornih ravni. Naročito se lahko primijenjuje na konjugirane ugljikovodike i pruža razumnu aproksimaciju, sve dok se pretpostavlja da je molekula poravnata s dobrim preklapanjem p-orbitala.
Stabilizacija energije[uredi | uredi izvor]
Kvantitativna procjena stabilizacije iz konjugacije notorno je sporna i ovisi o implicitnim pretpostavkama, koje se daju prilikom usporedbe referentnih sistema ili reakcija. Energija stabilizacije poznata je kao rezonancijska energija, kada se formalno definira kao razlika u energiji između stvarnih i hipotetskih hemijskih vrsta, koje lokalizirano sadrže π-vezu koja odgovara najstabilnijom obrascu rezonancije. Ova energija ne može se izmjeriti i vjerovatno će precizna definicija koju prihvati većina hemičara ostati neuhvatljiva. Ipak, mogu se dati neke široke mogućnosti. Općenito, stabilizacija je značajnija za kationske sisteme od neutralnih. Za buta-1,3-dien, gruba mjera stabilizacije je energija aktivacije za rotaciju veze C2-C3. Ovo postavlja rezonancijsku stabilizaciju na oko 6 kcal/mol.[3] Usporedba vrelina hidrogeniranja 1,4-pentadiena i 1,3-pentadiena procjenjuje nešto skromniju vrijednost od 3,5 kcal/mol.[4] Za usporedbu, alilni kation ima barijeru rotacije plinske faze od oko 38 kcal/mol,[5] što je mnogo veća kazna za gubitak konjugacije. Usporedba afiniteta hidridnih iona propil-kationa i alil-kationa, korigirana za induktivne efekte, rezultira znatno nižom procjenom rezonantne energije, na 20-22 kcal/mol.[6]Ipak, jasno je da konjugacija stabilizira alilni kation u mnogo većoj mjeri od buta-1,3-diena. Za razliku od obično manjeg učinka neutralne konjugacije, aromatska stabilizacija može biti značajna. Procjene za rezonantnu energiju benzena kreću se u rasponu od oko 36–73 kcal/mol.[7]
Uopćavanja i srodni koncepti[uredi | uredi izvor]

Postoje i drugi tipovi interakcija koje uopćavaju ideju interakcije p-orbitala u konjugiranom sistemu. Koncept hiperkonjugacije drži da se određene σ-veze također mogu delokalizirati u nisko ležeću neusku orbitalu π-sistema ili neuskuu p-orbitalu. Termin kiperkonjugacija se obično koristi da bi se objasnila stabilnost alkil supstituiranih radikala i karbokationa. Manje je važna za vrste kod kojih svi atomi zadovoljavaju pravilo okteta, ali nedavna računarska studija podržava hiperkonjugaciju kao ishodište povećane stabilnosti alkena sa višim stepenom supstitucije (Pravilo Zajceva).[8]
Homokonjugacija je preklapanje dva π-sistema odvojena nekonjugirajućom grupom, kao što je CH2. Nedvosmisleni primjeri su relativno rijetki u neutralnim sistemima, zbog relativno male energetske koristi koju lahko nadjačaju razni drugi faktori; međutim, česte su u kationskim sistemima u kojima se jakim delovanjem može postići delokalizacija pozitivnog naboja. Neutralni sistemi uglavnom zahtijevaju ograničene geometrije, koje favoriziraju interakciju da bi se postigli značajni stupnjevi homokonjugacije.[9] U donjem primjeru, frekvencije karbonilnog istezanja IR spektra odgovarajućih spojeva pokazuju homokonjugaciju ili nedostatak iste u molekulama neutralnog osnovnog stanja.
Zbog djelimičnog π-karaktera, za formalne σ-veze u ciklopropanskom prstenu, također su prikupljeni dokazi za prijenos „konjugacije“ kroz ciklopropane.[10]
Dva odgovarajuće poravnata π-sistema, čiji se krajevi spajaju pod pravim uglom, mogu se uključiti u spirokonjujgaciju.[11]
Konjugirani ciklični spojevi[uredi | uredi izvor]


Molekulske orbitale se često opisuju kao linearne kombinacije atomskih orbitala, čiji su koeficijenti ovdje naznačeni veličinom i sjenčenjem orbitalnih režnjeva.
Ciklični spojevi mogu biti djelimično ili u potpunosti konjugirani. Anuleni, potpuno konjugirani monociklični ugljikovodici, mogu biti aromatski, nearomatski ili antiaromatski.
Aromatski spojevi[uredi | uredi izvor]
Spojevi koji imaju monociklični, ravni konjugirani sistem koji sadrži (4n + 2) π-elektrona za cijele brojeve n su aromatski i pokazuju neobičnu stabilnost. Klasični primjer benzena ima sistem od šest π-elektrona, koji zajedno s ravninskim prstenom C–C σ-veza koje sadrže 12 elektrona i radijalnim C–H σ-vezama koje sadrže šest elektrona, čini termodinamički i kinetički stabilan benzenski prsten, zajedničko jezgro benzenoidnih aromatskih spojeva. Za sam benzen postoje dvije ekvivalentne konjugirane Lewisove strukture (tzv. Kekuléove strukture) koje prevladavaju.[12] Iako dva Kekuleova rezonantna oblika doprinose većini (> 90%) energije π-veze, postoji i niz drugih manjih doprinosa talasnoj funkciji u obradi valentne veze, uključujući tri Dewarova rezonantna oblika, pa čak i manji doprinos raznih ionskih i jednostrukih diradijalnih oblicka. Prava elektronska struktura je stoga kvantno-mehanička kombinacija (rezonantni hibrid) ovih doprinositelja, što rezultira eksperimentalno uočenim C–C vezama, koje su posredne između jednostruke i dvostruke veze i jednake čvrstoće i dužine. Na molekulskoj orbitalnoj slici, šest p-atomskih orbitala benzena kombiniraju se, dajući šest molekulskih orbitala. Tri od ovih orbitala, koje leže na nižim energijama od izolirane p orbitale i zbog toga su po karakteru neto povezane (jedna molekulska orbitala je snažno vezana, dok su druge dvije jednake po energiji, ali se vežu u manjoj mjeri), zauzima šest elektrona , dok su tri destabilizirane orbitale ukupnog protivveznog karaktera i dalje nezauzete. Rezultat je jaka termodinamička i kinetička aromatična stabilizacija. Oba modela opisuju prstenove π-elektronske gustoće iznad i ispod okvira C–C σ-veza.
Nearomatski i antiaromatski spojevi[uredi | uredi izvor]
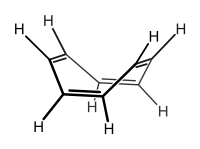
Dvostruke veze stoga nisu konjugoirane.
Nisu svi spojevi sa naizmeničnim dvostrukim i jednostrukim vezama aromatski. Ciklooktatetraen, naprimjer, ima izmjenične jednostruke i dvostruke veze. Molekula obično ima konformaciju "kada". Budući da se p-orbitale molekule ne poravnaju dobro u ovoj neplanarnoj molekuli, π-veze su u osnovi izolirane i nisu konjugirane. Nedostatak konjugacije omogućava molekuli 8 π-elektrona da izbjegne antiaromatičnost, destabilizirajući efekt povezan sa cikličnim, konjugiranim sistemima koji sadrže 4 n π (n = 0, 1, 2, .. .) elektrona. Ovaj je učinak posljedica smještaja dva elektrona u dvije degenerirane nevezujuće (ili gotovo nevezujuće) orbitale molekule, što bi, osim drastičnog smanjenja termodinamičke delokalizirane stabilizacije, ili prisililo molekulu da poprimi trojni diradikalni karakter, ili uzrokovalo da se podvrgne Jahn-Tellerovom izobličenju, kako bi se ublažila degeneracija. To ima za posljedicu znatno povećanje kinetičke reaktivnosti molekule. Budući da je učinak tako nepovoljan, ciklooktatetraen poprima neplanarnu konformaciju i nearomatičnog je karaktera, ponašajući se kao tipski alken. Suprotno tome, pronađeno je da su derivati ciklooktatetraenskog dikationa i dianiona eksperimentalno ravni, u skladu s predviđanjem da su stabilizirani aromatski sistemi sa 6 i 10 π-elektrona. Budući da je antiaromatičnost svojstvo koje molekuli pokušavaju izbjeći kad god je to moguće, vjeruje se da je samo nekoliko eksperimentalno uočenih vrsta antiaromatično. Ciklobutadienski i ciklopentadienilski kationi se obično navode kao primjeri antiaromatskih sistema.
U pigmentima[uredi | uredi izvor]
U konjugovanom pi-sistemu, elektroni su u stanju da uhvate određene fotone dok elektroni rezoniraju na određenoj udaljenosti p-orbitala – slično onome kako radio antena detektira fotone po svojoj dužini. Tipski, što je pi-sistem konjugiraniji (duži), talasna dužina fotona može biti duža. Drugim riječima, sa svakom dodanom susjednom dvostrukom vezom na prikazanom dijagramu molekula, može se predvidjeti da će sistem imati manje šanse da apsorbira žutu svjetlost (čini se crvenijom u očima) i vjerovatnije da apsorbira crvenu svjetlost (izgleda više žuto).[13]
Mnoge boje koriste konjugirane elektronske sisteme za apsorpciju vidljive svetlosti, stvarajući jake nijanse. Naprimjer, dugo konjugirani ugljikovodikov lanac u beta-karotenu dovodi do njegove jake narandžaste boje. Kada elektron u sistemu apsorbuje foton, svetlosti desne talasne dužine, može se povisiti na viši nivo energije. Jednostavan model nivoa energije pruža kvantnomehanički problem jednodimenzijskih čestica u kutiji dužine L, koje predstavlja kretanje π-elektrona duž dugo konjugiranog lanca atoma ugljika. U ovom modelu, najmanja moguća energija apsorpcije odgovara energetskoj razlici između najviše zauzete molekulske orbitale ( HOMO) i najmanje zauzete orbitale (LUMO). Za lanac n veza C=C ili 2n atoma ugljika u molekuli osnovnog stanja, postoje 2n π-elektrona koji zauzimaju n molekulske orbitale , tako da je energetska praznina:[14]
Budući da se dužina kutije L približno linearno povećava s brojem veza C=C n, to znači da je energija fotona ΔE apsorbiranog u HOMO-LUMO tranziciji približno proporcionalna do 1/n. Foton talasne dužine λ = hc / ΔE tada je približno proporcionalan n-u. Iako je ovaj model vrlo približan, λ se općenito povećava sa n (ili L) za slične molekule. Naprimjer, talasne dužine apsorpcije HOMO–LUMO za konjugirani butadien, heksatrien i oktatetraen su 217 nm, 25 nm i 304 nm.[15] Međutim, za dobro numeričko slaganje čestice u modelu eksperimenta sa kutijom, moraju se uzeti u obzir izmjene dužina jednostruke / dvovezne veze poliena[16] Alternativno, može se koristiti Hückelov metod koji je također dizajniran za modeliranje elektroničke strukture konjugiranih sistema.
Mnogi elektronski prijelazi u konjugovanim π-sistemima su iz pretežno vezane molekularne orbitale (MO) u pretežno antivezive MO (π do π*), ali elektroni iz nevezujućih usamljenih parova mogu također biti promovirani u π-sistem MO (n do π*), kao što se često događa u kompleksima koji prenose naboj. Prijelaz HOMO u LUMO vrši elektron, ako to dozvoljavaju pravila izbora za elektromagnetni prijelaz. Konjugoirani sistemi s manje od osam konjugovanih dvostrukih veza apsorbiraju samo u ultraljubičastom području i bezbojni su za ljudsko oko. Sa svakom dodatom dvostrukom vezom, sistem apsorbira fotone s duže talasne dužine (i niže energije), a spoj se kreće od žute do crvene boje. Plavi ili zeleni spojevi obično se ne oslanjaju samo na konjugirane dvostruke veze.
Ova apsorpcija svetlosti u ultraljubičastom u vidljivom spektru može se kvantifikovati upotrebom metoda zvanog ultraljubičasta – vidljiva spektroskopija i čini osnovu za celokupnu oblast fotohemije.
Konjugirani sistemi koji se široko koriste za sintetske pigmenta i bojila su diazo i azo-spojevi i ftalocijaninski spojevi.
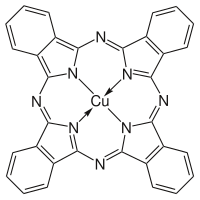
Ftalocijaninski spojevi[uredi | uredi izvor]
Konjugirani sistemi ne samo da imaju pobude sa niskom energijom u vidljivom spektarskom području, već i lahko prihvataju ili doniraju elektrone. Ftalocijanin, koji poput plavog i zelenog ftalociajnina, često sadrže prijelazni metalni ion, razmjenjuju elektron sa ionima prijelaznog metala koji lahko mijenjaju svoje stanje oksidacije. Ovakvi pigmenti i boje su kompleksi za prijenos naboja.
Porfirini i slični spojevi[uredi | uredi izvor]
Porfirini imaju konjugoirane molekulske prstenaste sisteme (makrociklus koji se pojavljuju u mnogim enzimskim biološkim sistemima. Kao ligand, porfirin formira brojne komplekse sa metalnim ionima poput gvožđa u hemoglobinu koji boji krv u crveno. Hemoglobin transportuje kiseik do tjelesnih ćelija. Kompleksi porfirin-metal često imaju jake boje. Slična molekulska strukturna prstenasta jedinica nazvana hlorin slično je složena sa magnezijem, umjesto gvožđa, kada čini dio najčešćih oblika molekula hlorofila, dajući im zelenu boju. Još jedna slična makrociklična jedinica je korin, koja se kompleksira sa kobaltom, kada čini dio molekula kobalamina (vitamin B12), koji je intenzivno crven. Korinska jedinica ima šest konjugiranih dvostrukih veza, ali nije konjugirana sve do svog makrocikličnog prstena
 |
 |

|
| Hem grupa hemoglobina | Hlorinska sekcija molekule hlorofila a. Zeleni okvir prikazuje grupu koja varira među tipovima hlorofila. | Kobalaminska struktura uključuje korin. |
Hromofore[uredi | uredi izvor]
Konjugirani sistemi čine osnovu hromofora, koje su dijelovi molekula koji upijaju svjetlost i koji mogu dovesti do obojenja spoja. Takve hromofore su često prisutne u raznim organskim spojevima, a ponekad i u polimer]ima koji su obojeni ili svijetle u mraku. Hromofore se često sastoje od niza konjugiranih veza i/ili prstenastih sistema, obično aromatskih, koji mogu uključivati veze C–C, C=C, C=O ili N=N.

Konjugirane hromofore nalaze se u mnogim organskim spojevima, uključujući azo boje (također veštački aditivi za hranu), spojeve u voću i povrću (likopene i antocijanidine), fotoreceptore oka i neke farmaceutske spojeve, kao što su:

Također pogledajte[uredi | uredi izvor]
- Rezonancija
- Hiperkonjugacija
- Unakrsna konjugacija
- Polien
- Konjugirani mikroporozni polimer
- Lista konjugiranih polimera
- Metalna veza
Reference[uredi | uredi izvor]
- ^ Thiele, Johannes (1899). "Zur Kenntnis der ungesättigten Verbindungen" [[Contribution] to our knowledge of unsaturated compounds]. Justus Liebig's Annalen der Chemie (jezik: njemački). 306: 87–142. doi:10.1002/jlac.18993060107. On p. 90, Thiele coined the term "conjugated": "Ein solches System benachbarter Doppelbindungen mit ausgeglichenen inneren Partialvalenzen sei als conjugirt bezeichnet." (Such a system of adjacent double bonds with equalized inner partial valences shall be termed "conjugated".)
- ^ March, Jerry (1985). Advanced Organic Chemistry reactions, mechanisms and structure (3rd izd.). New York: John Wiley & Sons, Inc. ISBN 0-471-85472-7.
- ^ Feller, David; Craig, Norman C. (2009-02-05). "High Level ab Initio Energies and Structures for the Rotamers of 1,3-Butadiene". The Journal of Physical Chemistry A (jezik: engleski). 113 (8): 1601–1607. doi:10.1021/jp8095709. PMID 19199679.
- ^ Carey, Francis A.; Guiliano, Robert M. (2013-01-07). Organic chemistry (Ninth izd.). New York, NY. ISBN 9780073402741. OCLC 822971422.
- ^ Gobbi, Alberto; Frenking, Gernot (1994-10-01). "Resonance Stabilization in Allyl Cation, Radical, and Anion". Journal of the American Chemical Society. 116 (20): 9275–9286. doi:10.1021/ja00099a052. ISSN 0002-7863.
- ^ Barbour, Josiah B.; Karty, Joel M. (2004-01-14). "Resonance Energies of the Allyl Cation and Allyl Anion: Contribution by Resonance and Inductive Effects toward the Acidity and Hydride Abstraction Enthalpy of Propene". The Journal of Organic Chemistry (jezik: engleski). 69 (3): 648–654. doi:10.1021/jo035189m. PMID 14750787.
- ^ Cotton, Frank Albert (1990). Chemical applications of group theory (3rd izd.). New York: Wiley. ISBN 978-0471510949. OCLC 19975337.
- ^ Braida, Benoit; Prana, Vinca; Hiberty, Philippe C. (2009-07-20). "The Physical Origin of Saytzeff's Rule". Angewandte Chemie International Edition (jezik: engleski). 48 (31): 5724–5728. doi:10.1002/anie.200901923. ISSN 1433-7851. PMID 19562814.
- ^ Scott, L. T. (1986-01-01). "Cyclic homoconjugation in neutral organic molecules". Pure and Applied Chemistry (jezik: engleski). 58 (1): 105–110. doi:10.1351/pac198658010105. ISSN 1365-3075.
- ^ Stewart, John Mathews; Pagenkopf, Gordon K. (January 1969). "Transmission of conjugation by the cyclopropane ring". The Journal of Organic Chemistry (jezik: engleski). 34 (1): 7–11. doi:10.1021/jo00838a003. ISSN 0022-3263.
- ^ Maslak, Przemyslaw (1994). "Spiroconjugation: An added dimensi in the design of organic molecular materials". Advanced Materials. 6 (5): 405–407. doi:10.1002/adma.19940060515. ISSN 0935-9648.
- ^ Rashid, Zahid; van Lenthe, Joop H. (March 2011). "Generation of Kekulé valence structures and the corresponding valence bond wave function". Journal of Computational Chemistry. 32 (4): 696–708. doi:10.1002/jcc.21655. ISSN 1096-987X. PMID 20941739.
- ^ Lipton, Mark (Jan 31, 2017). "Chapter 1. Electronic Structure and Chemical Bonding". Purdue: Chem 26505: Organic Chemistry I (Lipton) (LibreTexts izd.). Purdue University.
- ^ P. Atkins and J. de Paula Physical Chemistry (8th ed., W.H.Freeman 2006), p.281 ISBN 0-7167-8759-8
- ^ Atkins and de Paula p.398
- ^ Autschbach, Jochen (November 2007). "Why the Particle-in-a-Box Model Works Well for Cyanine Dyes but Not for Conjugated Polyenes". Journal of Chemical Education (jezik: engleski). 84 (11): 1840. doi:10.1021/ed084p1840. ISSN 0021-9584.

