Krvno-moždana barijera
| Krvno-moždana barijera | |
|---|---|
 Permesbilnost za rastvor BBB vs. horoidni pleksus | |
| Detalji | |
| Sistem | Neuroimmunski sistem |
| Akronim(i) | BBB |
| Anatomska terminologija | |
Krvno–moždana barijera (BBB) ili krvno-moždana prepreka ili krvno-moždana zapreka je visoko selektivna polupropusna granica endotelskih ćelija koja sprečava rastvore iz cirkulirajuće krvi da pređu u vanćelijsku tečnost centralnog nervnog sistema sa neuronima.[1] Krvno-moždana barijera formirana je od endotelnih ćelija kapilarnog zida, astrocitnih krajnjih stopala koja štite kapilar, a periciti su ugrađeni u kapilarnu baznu membranu.[2] Ovaj sistem omogućava prolazak nekih molekula pasivnom difuzijom, kao i selektivni transport različitih hranjivih sastojaka, iona, organskih aniona i makromolekula, kao što su glukoza, voda i aminokiseline, neophodne su za uravnoteženu nervnu funkciju.[3]
Ova posebna razgraničenja krvi (intravaskularno) iz ekstravaskularnog prostora u mozgu i leđnoj moždini razvijena su kod svih kopnenih kičmenjaka (Tetrapoda) i omogućava živčanom tkivu da održi stabilne okolinske uslove (homeostaza). U suštini, ova prepreka se formira od endotelnih ćelija, koje su ovdje usko povezane u kapilarne krvne žile preko čvrstih spojeva.
Krvno-moždana barijera štiti mozak od patogena, toksina i glasničkih tvari koje cirkuliraju u krvi. To je visokoselektivan filter kroz koji se isporučuju hranjive tvari potrebne mozgu, a uklanjaju se nastali metabolički proizvodi. Snabdijevanje i odlaganje zagarantovani su nizom posebnih transportnih procesa.
S druge strane, ova zaštitna funkcija mozga otežava liječenje lijekovima za veliki broj neuroloških bolesti, jer mnoge aktivne tvari ne mogu da prelaze krvno-moždanu barijeru. Prelaz kroz krvno-moždanu barijeru je aktuelna tema istraživanja u svijetu nauke. Vrlo mali broj izuzetno rijetkih bolesti je izravno povezanih s krvno-moždanom barijerom, dok sama može uticati na znatno veći broj rasprostranjenih bolesti.
Prve eksperimente koji su ukazivali na postojanje ove barijere izveo je Paul Ehrlich 1885. Međutim, pogrešno je protumačio rezultate testa. Konačni dokaz krvno-moždane barijere uradio je 1967. elektronsko-mikroskopskim pregledima.

telencefalon]] 11-dnevnog mišjeg embrija ood elektronskim mikroskopom. U gornjoj polovini slike je bijeli lumen kapilarne žile. Endotelne ćelije međusobno su povezane uskim spojnicama (tamniji "kanali"). Ispod su Adhereni čvorovi. Širina slike odgovara oko 4,2 µm.]]


Funkcije[uredi | uredi izvor]
U ljudi, mozak čini oko 2% tjelesne mase. Međutim, udio potreba za hranjivim tvarima je oko 20%. Za razliku od drugih tjelesnih organa, mozak ima izuzetno ograničene rezerve hranjivih sastojaka ili kisika . Živčane ćelije također nisu u stanju da anaerobno ispune svoje energetske potrebe , tj. bez elementarnog kisika. Prekid u opskrbi mozga krvlju dovodi do nesvijesti nakon deset sekundi, a nervne ćelije umiru samo nekoliko minuta kasnije. Ovisno o aktivnosti određenog područja mozga, njegove energetske potrebe i rezerve mogu biti vrlo različite. Kako bi se mogla prilagoditi ponuda ovisno o potrebama, ova područja automatski reguliraju opskrbu krvlju.
Složene funkcije mozga vezane su za visoko osjetljive elektrohemijske i biohemijske procese koji se mogu odvijati u velikoj mjeri samo bez smetnji u konstantnom unutrašnjem okruženju, homeostazi. Naprimjer, fluktuacije vrijednosti pH krvi ne smiju se prenijeti na mozak. Fluktuacije koncentracije kalija izmijenit će membranski potencijal nervnih ćelija. Neurotransmiteri koji kruže krvnim sudovima ne smiju ući u centralni nervni sistem jer bi značajno poremetili protok informacija u tamošnjim sinapsama . Osim toga, neuroni nisu sposobni za regeneraciju u slučaju oštećenja uzrokovanih fluktuacijom okoline. Konačno, mozak kao centralno upravljajući organ mora biti zaštićen i od djelovanja egzogenih supstanci, poput ksenobiotika i patogena . Opsežna nepropusnost krvno-moždane barijere za patogene, antitijela i krvne leukocite, čini je i imunskom barijerom.[4][5][6] S druge strane, velike potrebe mozga za energijom – u usporedbi s drugim organima – proizvode natprosječne količine produkata metaboličke razgradnje. koje je potrebno ukloniti, ponovo preko krvno-moždane barijere. Da bi se osigurale sve ove funkcije (napajanje, odlaganje i homeostaza), cerebralni sistem krvnih sudova kod kičmenjaka pokazuje niz strukturnih i funkcionalnih razlika u odnosu na sistem perifernih krvnih sudova. Ova diferencijacija uzrokuje da se mozak u velikoj mjeri odvoji od okolnog vanćelijskog prostora i od suštinske je važnosti za zaštitu osjetljivog neuronskog tkiva i za održavanje konstantnog unutarnjeg okruženja.
Promjene u funkciji krvno-moždane barijere uzrokuju promjene u stanju centralnog nervnog sistema, što zauzvrat može dovesti do disfunkcije ili bolesti u CNS-u. Prema tome, niz neuroloških bolesti direktno je ili indirektno povezano s krvno-moždanom barijerom.
Anatomija[uredi | uredi izvor]


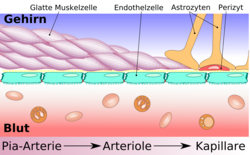
Esencijalni element krvno-moždane barijere su endotelne ćelije sa svojim uskim spojevima. Ipak, dvije druge vrste ćelija, periciti i astrociti , od velikog su značaja za funkciju, strukturu i razvoj krvno-moždane barijere . Interakcije ćelija-ćelija između endotelnih ćelija, pericita i astrocita su bliže nego u bilo kojoj drugoj ćeliji. Ove tri vrste ćelija zajedno formiraju krvno-moždanu barijeru kod većine kičmenjaka, endotelnu krvno-moždanu barijeru . Sljedeće anatomske informacije odnose se na endotelnu krvno-moždanu barijeru kičmenjaka. Glijina krvno-moždana barijera razvijena kod nekih kičmenjaka i mnogih beskičmenjaka navedena je odvojeno na kraju ovog poglavlja.
Endotel[uredi | uredi izvor]
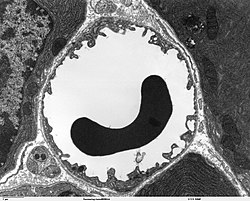
Kao i u perifernim krvnim sudovima, kapilare stvaraju endotelne ćelije. Endotel perifernih kapilara ima otvore (fenestracije) promjera oko 50 nm i međućelijske praznine širine 0,1 do 1 µm, za razmjenu vode i tvari koje su u njemu otopljene ili suspendirane između krvi i vanćelijske tekućine okolnog tkiva. Suprotno tome, u mozgu nema fenestracija i unutarćelijskih praznina između endotelnih ćelija[7] Membrana suda okrenuta ka unutrašnjosti kapila znatno se razlikuje od apikalne strane koja je okrenuta prema intersticiju s obzirom na vrstu membranskih proteina.[8] Broj pinocitotskih vezikula koji omogućavaju endocitozu otopljenih supstanci vrlo je mali u endotelu mozga.
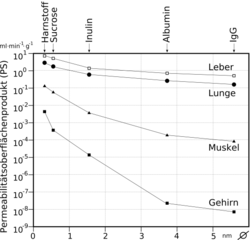
Suprotno tome, broj mitohondrija je oko 5 do 10 puta veći nego u perifernim kapilarama. To je pokazatelj velike energetske potrebe endotela – između ostalog i za aktivne transportne procese – i velike metaboličke aktivnosti . Barijera između krvi i mozga nije samo fizička, već i metabolička ili enzimska barijera.[9][10][11][12][13] U ćelijskoj membrani endotela nalazi se veći broj enzima u znatno većem broju nego, naprimjer, u ćelijama parenhima . Tu spadaju γ-glutamiltransferaza, alkalna fosfataza i glukoza-6-fosfataza. U metabolizmu enzima kao što su katehol-O-metiltransferaza , monoamin-oksidaza ili citohrom P450 također su aktivni u endoteu u relativno visokim koncentracijama.[14][15][16][17] Na ovaj se način mnoge tvari metaboliziraju prije ili za vrijeme njihova unutarćelijskog transporta. Endotelne ćelije su ekstremno tanke, svega 0,3 do 0,5 um. U odnosu, enterocite, u epitelnim ćelijama crijeva, znatno je deblja i iznosi 17-30 μm. Kao i u drugim endotelnim ćelijama, omjer holesterola u fosfolipidima iznosi 0,7. Čisti difuzijski procesi kroz sćelijsku membranu su stoga jednako brzi kroz krvno-moždanu barijeru kao i kod ostalih endotelnih ćelija. Endotelne ćelije imaju veliki broj akvaporina na ćelijskoj membrani, za reguliranje vodene ravnoteže mozga . Ovi kanali omogućavaju molekulama vode da difundiraju slobodno i prema mozgu i prema krvi.[18] Nedostatak fenestracija i pinocitotskih vezikula predstavljaju pasivnu barijeru krvno-moždane barijere. Ovaj barijerski efekat može se fizički kvantificirati njenim električnim otporom . Otpor kod zdravih odraslih pigmentiranih pacova iznosi oko 1500 do 2000 Ω cm². Suprotno tome, vrijednost za kapilare u mišićnom tkivu je oko 30 Ω cm².[19] Aktivni transportni sistemi endotela, koji će biti detaljnije opisani kasnije, formiraju aktivnu barijeru krvno-moždane barijere.
Čvrste međućelijske veze[uredi | uredi izvor]
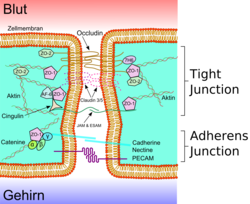

B – apikalna strana
C – bazalna strana
a – sluzi
b – apikalna strana
c – bazolateralna površina d – čvrsta veza
f – paraćelijski prostor
g – ćelijska membrana
e – proteinski kompleks
1 – okludin
2 – klaudin -1
3 – E-kaderin
4 – ZO-1
5 – JAM-1
6 – katenini
7 – cingulin
8 – aktin

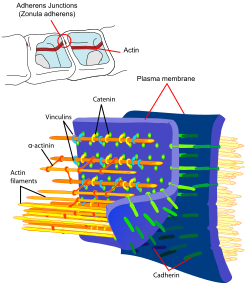
Endotelne ćelije međusobno su povezane čvrstim vezama ćelija, takozvanim tijesnim spojevima. Ovi uski spojevi predstavljaju čvrste veze između susjednih ćelija i daju značajan doprinos zaprečnoj funkciji krvno-moždane barijere.[20][21] Budući da oni zabravljavaju prostor između ćelija i na taj način praktički isključuju paracelularni transport, omogućuju prolazak tvari duž međućelijskog prostora između susjednih endotelnih ćelija.[22][23][24]
Nekoliko transmembranskih proteina , kao što su okludin , različiti klavidi i molekule spojne adhezije (JAM), povezuju endotel u apikalnom području bočnih ćelijskih zidova obodnim proteinskim vrpcama u uskim spojnicama, na taj način u velikoj mjeri sprječavajući paraćelijski prolaz kroz međućelijski razmak između dviju endotelnih ćelija za veće molekule.[25] Pojedinačne veze protein-protein djeluju poput paralelnog osigurača.[26] Od 24 poznata klaudina, endotelne ćelije krvno-moždane barijere imaju samo klaudin-5 i klaudin-12. Klaudin-5 koristi se kao najvažniji protein adhezije ćelija i smatra se krvno-moždanom barijerom. Isključivanje (nokautom gena) gena CLDN5, koji kodira klaudin-5 , dovodi do krvno-stvaranje moždanih barijera kod miševa koje su propusne za molekule molarne mase do 800 g · mol –1 stanice. Genetički modificirane životinje uginule su za nekoliko sati od rođenja.[27] Fiksacija endotela osigurava njihovo poravnanje na dvije vrlo različite strane: lumenska strana okrenuta prema krvi i obilna strana okrenuta prema mozgu.
Bazna lamina[uredi | uredi izvor]

Endotelne ćelije su u potpunosti okružene slojem proteina bazne lamine. [8] Ovaj dvostruki sloj je debljine oko 40 do 50 nm i vidljiv je samo pod elektronskim mikroskopom. U osnovi se sastoji od kolagena tipa IV, heparin-sulfata – proteoglikana, laminine, fibronektina i drugih proteina vanćelijskog matriksa. Bazna lamina graniči s plazma membranom terminalnih krajeva astrocita.
Periciti[uredi | uredi izvor]

Periciti, koji se nazivaju Rougetovim ćelijama posebno u starijoj literaturi nakon otkrića Charlesa Marieja Benjamina Rougeta (1824-1904) [32] , važan su dio krvno-moždane barijere. Tri su osnovna svojstva u prvom planu: njihova sposobnost ugovaranja, regulacija endotela i aktivnost makrofaga.
Oko 20% vanjske endotelne površine moždanihnih kapilara prekriveno je relativno malim pericitima ovalnog oblika i svaka druga do četvrta endotelna ćelija povezana je s pericitom. Periciti su poželjno smješteni na mjestu kontakta između dvije endotelne ćelijee.[28] bezeichnet, sind ein wichtiger Bestandteil der Blut-Hirn-Schranke.[29][30] Periciti se nalaze na gotovo svim arteriolama, venulama i kapilarima – i to ne samo u moždanom endotelu. Stupanj pokrivenosti endotela pericitima direktno je u korelaciji sa nepropusnošću uskih spojnica . U fenestriranim kapilarima, naprimjer u skeletnim mišićima, odnos endotela i pericita iznosi 100: 1.[31][32] Poput endotelskih čelija,i periciti su također okruženi kontinuiranom baznom laminom.[33][34]
Kontakt pericit-endotel[uredi | uredi izvor]

Ovi proteinski kompleksi koji formiraju kanal predstavljaju jednu vrstu veze pericita u endotelne ćelije.
Periciti su čvrsto usidreni u endotelnim ćelijama. Vezu između ove dvije vrste ćelija, tvore najmanje tri vrste pericite-endotelnog kontakta. To su jazni spojevi (proteinski kompleksi koji formiraju kanal), žarišna adhezija (adhezijski plakovi) i intuscepcijska spona . Spojevi između praznina vežu dvije citoplazme i omogućavaju razmjenu iona i manjih molekula između dva tipaćelija, putem kanala. [39] Periciti su mehanički pričvršćeni na endotel, putem žarišne adhezije. Invazije u vidu klipova i utičnica sastoje se od međusobno isprepletenih izbočina dvije međusobno povezane ćelije.[35]
Obje vrste ćelija međusobno utiču jedna na drugu, s obzirom na njihovu mitozu i vjerojatno se odnose i na fenotipsku ekspresiju.[36] Ovaj tip međućelijskog kontakta također očito doprinosi mehaničkom sidrenju pericita u endotelu[30][37][38]
Kontrakcija[uredi | uredi izvor]
Periciti imaju visok udio kontraktilnog strukturnog proteina aktina . To im omogućuje promjenu promjera kapilara preko njihovih ekstenzija i na taj način lokalno reguliraju krvni pritisak.[39][40]
Makrocitna svojstva[uredi | uredi izvor]
Očigledno je da samo periciti na cerebralnim kapilarama imaju posebno svojstvo. Tamo djeluju kao makrofagi . Postoji mnogo lizozomi u citoplazmi u periciti i in vivo su pokazali sposobnost da se rastvorljivih trasera koji su intravenski ili intraventrikularni i na drugi način uzeti samo putem makrofaga. U kulturama tkiva pokazalo se da su periciti sposobni za fagocitozu[41][42] i prezentaciju antigena.[43][44]
Ta makrocitna svojstva su "druga linija obrane " protiv neurotoksičnih molekula koji su već prešli kroz endotelni sloj prema mozgu.[45] Periciti, stoga, značajno doprinose imunskom sistemu centralnog nervnog sistema. S druge strane, posredstvom ovih svojstava oni sudjeluju i u razvoju različitih, posebno autoimunih bolesti . Raspravlja se i o indirektnom uključivanju u Alzheimerovu bolest.[46][47]
Astrociti[uredi | uredi izvor]
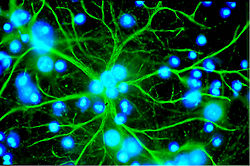

Astrociti su zvjezdaste, razgranate ćelije iz porodice makroglija koje su znatno veće od pericita . Dodijeljeni su centralnom nervnom sistemu i još su se sposobni dijeliti se i nakon rođenja. Kod viših kičmenjaka, oni nemaju direktnu barijersku funkciju, čak i ako terminalnim stopalima pokrivaju oko 99% kapilara u mozgu. [53] Međutim, oni su u direktnoj interakciji s endotelom.[48][49] Astrociti induciraju funkciju krvno-moždane barijere u endotelu moždanih krvnih sudova. Bilo je do dokazanih pokušaja transplantacije. Moždani krvni sudovi koji su presađeni u periferne organe ponašale su se poput "normalnih" kapilara tamo i, naprimjer, formirale fenestracije. U obrnutom eksperimentu, periferni kapilari koji su presađeni u centralni nervni sistem, iformirali su tamošnji fenotip s uskim vezama. Uticaj astrocita na fenotipsku ekspresiju endotela može se vidjeti i u testovima in vitro. U kokulturama astrocita i endotelnih ćelija endotel je gušći nego u čistim endotelnim kulturama .[50]
Astrociti oslobađaju brojne glasničke supstance koje mogu modulirati propusnost endotela u rasponu od sekunde do minute. S druge strane, objavljeno je da endotelne ćelije leukemija-inhibitornog faktora (LIF) i citokina klase interleukin-6 koja izazivaju diferencijaciju astrociti.[51] Udaljenost između podnožja astrocita i endotelnih ćelija i pericita je samo 20 nm. Glavna funkcija astrocita je, međutim, selektivna opskrba neurona hranjivim tvarima i regulacija koncentracije vanćelijskih iona. Većinu holesterola koji postoji u mozgu proizvode astrociti. Holesterol ne može prijeći krvno-moždanu barijeru, zbog čega ga se mora sintetizirati lokalno u mozgu. Oko 25% telesnog holesterola nalazi se u mozgu; u osnovi u mijelinu koji pokriva aksone neurona.

Terminalna stopala astrocita sa endotelnim ćelijama formiraju osjetljiv kontakt poput rozete. Ovaj raspored je važan za međusobno uticaj i komunikaciju dva tipa ćelija. Moguća je i slobodna difuzija endotela i parenhima mozga.
Bolesti koje direktno ili indirektno utječu na astrocite, poput Alzheimerove ili astrocitoma , mogu značajno narušiti funkcioniranje krvno-moždane barijere, uslijed bliske interakcije astrocita i endotela.
Područja mozga bez krvno-moždane barijere[uredi | uredi izvor]


Nisu svi kapilari u mozgu izgrađene kao u krvno-moždanoj barijeri. Naprimjer, područja mozga koja oslobađaju neuroendokrine spojeve (hormone) u krv ili koja imaju senzornu funkciju – naprimjer za određene peptidne hormone – nužno su bez krvno-moždane barijere. To je slučaj sa šest cirkventrikularnih organa. Epifiza, eminentia mediana, neurohipofiza, na području postrema je organum vasculosum lamine terminalis i organum subfornicale, imaju fenestrirane kapilare. Naprimjer, neuroni područja postrema otkrivaju za tijelo otrovne tvari i centar za povraćanje koji stimulira mučninu. U potkomisurnom organu, krvno-moždana barijera jedini je cirkumentikularni organ. Da bi zaštitili okolno moždano tkivo, cirkventrikularni organi su okruženi tanicitima. To su posebne ependimaske ćelije s vrlo gustim čvrstim međućelijskim vezama.[52][53]
Značajniji transporteri kroz krvno-moždanu barijeru i njihovi genetički determinatori[uredi | uredi izvor]
| Transporter | Naziv | Gen | Hromosom, genski lokus | Porodica | Izvor |
| Olakšana difuzija | |||||
| GLUT1 | Glukozni transporter 1 | SLC2A1 | 1 p35-p31.3 | Nosač rastvora | [54] |
| LAT1 | Veliki neutralni transportrr aminokiselina 1 | SLC7A5 | 16 q24.3 | Nosač rastvora | [54] |
| CAT1 | Kationski transporter aminokiselina 1 | SLC7A1 | 13 q12.3 | Nosač rastvora | [54] |
| MCT1 | Transporter 1 monocarboksilnih kiselina | SLC16A1 | 1 p13.2-p12 | Nosač rastvora | [54] |
| CNT2 | Transporter 2 koncentrativvnih nukleozida | SLC28A2 | 15 q15 | Nosač rastvora | [54] |
| CHT1 | Holinski transporter 1 | SLC5A7 | 2 q12 | Nosač rastvora | [54] |
| NBTX | Transporter nukleobaza | ? | ? | [54] | |
| Aktivni odliv | |||||
| MDR1 | P-Glikoprotein | ABCB1 | 7 q21.1 | ATP-vezujuća kaseta | [55] |
| MRP1 | Protein 1 višestruke rezistencije na lijekove | ABCC1 | 16 p13.1 | ATP-vezujuća klaseta | [55] |
| MRP3 | Protein 3 višestruke rezistencije na lijekove | ABCC3 | 17 q22 | ATP-binding cassette | [55] |
| MRP4 | Protein 4 višestruke rezistencije na lijekove | ABCC4 | 13 q32 | ATP-vezujuća kaseta | [55] |
| MRP5 | Protein 5 višestruke rezistencije na lijekove | ABCC5 | 3 q27 | ATP-vezujuća kaseta | [55] |
| BCRP | Protein rezistencije na rak dojke | ABCG2 | 4 q22 | ATP-vezujuća kaseta | [55] |
| OAT3 | Transporter 3 organskih aniona | SLC22A8 | 11 | Nosač rastvora | [6] |
| OATP-A | Transporter A organskih aniona | SLC21A3 | 12 p12 | Nosač rastvora | [6] |
| OATP3A1 | Transporter 3 organskih polipeptidnih aniona | SLCO1A2 | 15 q26 | Nosač rastvora | [6] |
| EAAT1 | Transporter 5 nadražujućih aminokiselina | SLC1A3 | 5 p13 | Nosač rastvora | [6] |
| TAUT | Taurinski transporter | SLC6A6 | 3 p25-q24 | Nosač rastvora | [54] |
| Transport posredovan receptorima | |||||
| INSR | Receptor za inzulin | INSR | 19 p13.2 | [54] | |
| TFR1 | Transferinski receptor | TFRC | 3 q29 | [54] | |
| IGF1R | Recepro inzulinolikog faktora rasta 1 | IGF1R | 15 q25-q26 | [54] | |
| LEPR | Leptinski receptor | LEPR | 1 p31 | [54] | |
| FCGRT | Receptorski transporter Fc fragmenta IgC, | FCGRT | 19 q13.3 | [54] | |
| SCARB1 | Klasa receptora čistača B 1 | SCARB1 | 12 q24.31 | [54] |
Interakcija različitih članova porodice nosača rastvora i ABC transportera izuzetno je efikasan zaštitni mehanizam za krvno- moždanu barijeru kako bi se spriječilo da ksenobiotici uđu u mozak.[56][57]
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Daneman R, Prat A (januar 2015). "The blood-brain barrier". Cold Spring Harbor Perspectives in Biology. 7 (1): a020412. doi:10.1101/cshperspect.a020412. PMC 4292164. PMID 25561720.
- ^ Ballabh P, Braun A, Nedergaard M (juni 2004). "The blood-brain barrier: an overview: structure, regulation, and clinical implications". Neurobiology of Disease. 16 (1): 1–13. doi:10.1016/j.nbd.2003.12.016. PMID 15207256.
- ^ Gupta, Smriti; Dhanda, Saurabh; Sandhir, Rajat (2019). "Anatomy and physiology of blood-brain barrier". Brain Targeted Drug Delivery System. Elsevier. str. 7–31. doi:10.1016/b978-0-12-814001-7.00002-0. ISBN 978-0-12-814001-7. Nepoznati parametar
|name-list-format=zanemaren (prijedlog zamjene:|name-list-style=) (pomoć) - ^ W. Risau et al.: Immune function of the blood-brain barrier: in complete presentation of protein (auto-)antigens by rat brain microvascular endothelium in vitro. In: Journal of Cell Biology 110, 1990, S. 1757–1766. PMID 1692329.
- ^ B. Bauer: In vitro Zellkulturmodelle der Blut-Hirn-Schranke zur Untersuchung der Permeation und P-Glykoprotein-Interaktion von Arzneistoffen. Dissertation, Ruprecht-Karls-Universität Heidelberg, 2002.
- ^ a b c d e S. Ohtsuki: New aspects of the blood-brain barrier transporters; its physiological roles in the central nervous system. In: Biol Pharm Bull. 27, 2004, S. 1489–1496. PMID 15467183 (Review).
- ^ J. C. Lee: Evolution in the concept of the blood-brain barrier phenomen. In: Progress in neuropathology. Band 1. Verlag Grune und Stratton, 1971, ISBN 0-88167-188-6, S. 84–145.
- ^ M. Pavelka, J. Roth: Funktionelle Ultrastruktur. Verlag Springer, ISBN 3-211-83563-6, S. 234–235.
- ^ S. Nobmann: Isolierte Gehirn-Kapillaren als in vitro-Modell der Blut-Hirn Schranke; Dissertation, Ruprecht-Karls-Universität Heidelberg, 2001.
- ^ R. S. el-Bacha, A. Minn: Drug metabolizing enzymes in cerebrovascular endothelial cells afford a metabolic protection to the brain. In: Cell Mol Biol 45, 1999, S. 15–23. PMID 10099836 (Review).
- ^ M. Chat et al.: Drug metabolizing enzyme activities and superoxide formation in primary and immortalized rat brain endothelial cells. In: Life Sci] 62, 1998, S. 151–163. PMID 9488113.
- ^ A. Minn et al.: Drug metabolizing enzymes in the brain and cerebral microvessels. In: Brain Res Brain Res Rev 116, 1991, S. 65–82. PMID 1907518 (Review).
- ^ Y. Takahura et al.: Blood-brain barrier: transport studies in isolated brain capillaries and in cultured brain endothelial cells. In: Adv Pharmacol 22, 1991, S. 137–165. PMID 1958501 (Review).
- ^ S. Meresse et al.: Bovine brain endothelial cells expres tight junctions and monoamine oxidase activity in long-term culture. In: J Neurochem 53, 1989, S. 1363–1371. PMID 2571674.
- ^ R. Perrin et al.: Distribution of cytochrom P450 activities towards alkoxyresorufin derivates in rat brain regions, subcellular fractions and isolated cerebral microvessels. In: Biochem Pharmacol 40, 1990, S. 2145–2151. PMID 2242042.
- ^ R. Bendayan et al.: Functional expression and localization of P-glycoprotein at the blood brain barrier. In: Microsc Res Tech 57, 2002, S. 365–380. PMID 12112443 (Review).
- ^ Y. Su, P. J. Sinko: Drug delivery across the blood-brain barrier: why is it difficult? how to measure and improve it? In: Expert Opin Drug Deliv 3, 2006, S. 419–435. PMID 16640501 (Review).
- ^ B. Nico et al.: Role of aquaporin-4 water channel in the development and integrity of the blood-brain barrier. In: J Cell Sci 114, 2001, S. 1297–1307. PMID 11256996.
- ^ A. M. Butt et al.: Electrical resistance across the blood-brain barrier in anaesthetized rats: a developmental study. In: J Physiol 429, 1990, S. 47–62. PMID 2277354.
- ^ P. Claude, D. A. Goodenough: Fracture faces of zonae occludentes from tight and leaky epithelia. In: J Cell Biol, 58, 1973, S. 390–400. PMID 4199658.
- ^ H. Wolburg et al.: Modulation of tight junction structure in blood-brain barrier endothelial cells. Effects of tissue culture, second messengers and cocultured astrocytes. In: J Cell Sci 107, 1994, S. 1347–1357. PMID 7929640.
- ^ H. B. Newton: Advances in strategies to improve drug delivery to brain tumors. In: Expert Rev Neurother 6, 2006, S. 1495–1509. PMID 17078789 (Review).
- ^ J. L. Madara: Tight junction dynamics: is paracellular transport regulated? In: Cell 53, 1988, S. 497–498. PMID 3286009.
- ^ H. C. Bauer et al.: Proteins of the tight junctions in the blood-brain barrier. In: Blood-spinal Cord and Brain Barriers in Health and Disease. Verlag Elsevier, 2004, S. 1–10.
- ^ R. Cecchell et al.: Modelling of the blood–brain barrier in drug discovery and development. In: Nat Rev Drug Discov, 6, 2007, S. 650–661. PMID 17667956 (Review).
- ^ K. Matter, M. S. Balda: Holey barrier: claudins and the regulation of brain endothelial permeability. In: J Cell Biol, 161, 2003, S. 459–460. PMID 12743096 (Review).
- ^ T. Nitta et al.: Size-selective loosening of the blood–brain barrier in claudin-5-deficient mice. In: J Cell Biol, 161, 2003, S. 653–660. PMID 12743111.
- ^ P. Dore-Duffy: Pericytes: pluripotent cells of the blood brain barrier. In: Curr Pharm Des 14, 2008, S. 1581–1593. PMID 18673199 (Review).
- ^ R. Balabanov, P. Dore-Duffy: Role of the CNS microvascular pericyte in the blood-brain barrier. In: J Neurosci Res 53, 1998, S. 637–644. PMID 9753191 (Review).
- ^ a b H.K. Rucker et al.: Cellular mechanisms of CNS pericytes. In: Brain Res Bull 51, 2000, S. 363–369. PMID 10715555 (Review).
- ^ C. H. Lai, K. H. Kuo: The critical component to establish in vitro BBB model: Pericyte. In: Brain Res Brain Res Rev, 50, 2005, S. 258–265. PMID 16199092 (Review).
- ^ D. Shepro, N.M. Morel: Pericyte physiology. In: FASEB J, 7, 1993, S. 1031–1038. PMID 8370472 (Review).
- ^ P. A. D’Amore: Culture and Study of Pericytes. In: Cell Culture Techniques in Heart and Vessel Research. Verlag Springer, 1990, ISBN 3-540-51934-3, S. 299.
- ^ N. J. Abbott: Neurobiology: Glia and the blood-brain barrier. In: Nature, 325, 1987, S. 195. PMID 3808015.
- ^ K. Fujimoto: Pericyte-endothelial gap junctions in developing rat cerebral capillaries: A fine structural study. In: Anat Rec 242, 1995, S. 562–565. PMID 7486026.
- ^ D. E. Sims: Diversity within pericytes. In: Clin Exp Pharmacol Physiol 27, 2000, S. 842–846. PMID 11022980 (Review).
- ^ L. Diaz-Flores: Microvascular pericytes: A review of their morphological and functional characteristics. In: Histol Histopath 6, 1991, S. 269–286. PMID 1802127 (Review).
- ^ D. E. Sims: Recent advances in pericyte biology—Implications for health and disease. In: Can J Cardiol 7, 1991, S. 431–443. PMID 1768982 (Review).
- ^ I. M. Herman, P. A. D’Amore: Microvascular pericytes contain muscle and nonmuscle actins. In: J Cell Biol, 101, 1985, S. 43–52. PMID 3891763.
- ^ K. K. Hirschi, P. A. D’Amore: Pericytes in the microvasculature. In: Cardiovasc Res, 32, 1996, S. 687–698. PMID 8915187 (Review).
- ^ M. Mato et al.: Evidence for the possible function of the fluorescent granular perithelial cells in brain as scavengers of high-molecular-weight waste products. In: Experientia 40, 1984, S. 399–402. PMID 6325229.
- ^ R. Balabanov et al.: CNS microvascular pericytes express macrophage-like function, cell surface integrin alphaM, and macrophage marker ED-2. In: Microvasc Res 52, 1996, S. 127–142. PMID 8901442.
- ^ W. F. Hickey und H. Kimura: Perivascular microglial cells of the CNS are bone marrow-derived and present antigen in vivo. In: Science 239, 1988, S. 290–292. PMID 3276004.
- ^ Z. Fabry et al.: Differential activation of Th1 and Th2 CD4+ cells by murine brain microvessel endothelial cells and smooth muscle/pericytes. In: J Immunol 151, 1993, S. 38–47. PMID 8100844.
- ^ D. Krause et al.: Cerebral pericytes - a second line of defense in controlling blood-brain barrier peptide metabolism. In: Adv Exp Med Biol 331, 1993, S. 149–152. PMID 8101424.
- ^ W. E. Thomas: Brain macrophages: on the role of pericytes and perivascular cells. In: Brain Res Brain Res Rev 31, 1999, S. 42–57. PMID 10611494 (Review).
- ^ C. Iadecola: Neurovascular regulation in the normal brain and in Alzheimer’s disease. In: Nat Rev Neurosci 5, 2004, S. 347–360. PMID 15100718 (Review).
- ^ Greška kod citiranja: Nevaljana oznaka
<ref>; nije naveden tekst za reference s imenomPMID15805577 - ^ C. E. Johanson: Permeability and vascularity of the developing brain: cerebellum vs. cerebral cortex. In: Brain Res 190, 1980, S. 3–16. PMID 6769537.
- ^ J. Neuhaus et al.: Induction of blood-brain barrier characteristics in bovine brain endothelial cells by rat astroglial cells in transfilter coculture. In: Ann N Y Acad Sci 633, 1991, S. 578–580. PMID 1789585.
- ^ P. A. Stewart, M. J. Wiley: Developing nervous tissue induces formation of blood-brain barrier characteristics in invading endothelial cells: a study using quail–chick transplantation chimeras. In: Dev Biol, 84, 1981, S. 183–192. PMID 7250491.
- ^ H. M. Duvernoy, P. Y. Risold: The circumventricular organs: an atlas of comparative anatomy and vascularization. In: Brain Res Rev 56, 2007, S. 119–147. PMID 17659349 (Review).
- ^ C. Lohmann: Die Blut-Hirn-Schranke in vitro: Regulation der Permeabilität durch Matrixmetalloproteasen. Dissertation, Westfälische Wilhelms-Universität Münster, 2003.
- ^ a b c d e f g h i j k l m n W. M. Pardridge: Blood-brain barrier delivery. In: Drug Discov Today 12, 2007, S. 54–61. PMID 17198973.
- ^ a b c d e f H. Bronger et al.: ABCC drug efflux pumps and organic anion uptake transporters in human gliomas and the blood-tumor barrier. In: Cancer Res 65, 2005, S. 11419–11428. PMID 16357150.
- ^ H. Kusuhara und Y. Sugiyama: Active efflux across the blood-brain barrier: role of the solute carrier family. In: NeuroRx 2, 2005, S. 73–85. PMID 15717059 (Review).
- ^ J. M. Scherrmann: Expression and function of multidrug resistance transporters at the blood-brain barriers. In: Expert Opin Drug Metab Toxicol 1, 2005, S. 233–246.
Vanjski linkovi[uredi | uredi izvor]
| Commons ima datoteke na temu: Krvno-moždana barijera |

