Sirćetna kiselina
Ovaj članak nije preveden ili je djelimično preveden. |
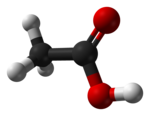
| Acetatna kiselina | |
|---|---|
    | |
| Općenito | |
| Hemijski spoj | Acetatna kiselina |
| Druga imena | acetil hidroksid (AcOH), vodik acetat (HAc), sirćetna kiselina, metankarbonska kiselina |
| Molekularna formula | C2H4O2 |
| CAS registarski broj | 64-19-7 |
| Kratki opis | bezbojna tekućina |
| Osobine1 | |
| Molarna masa | 60,05 g/mol |
| Agregatno stanje | tekuće |
| Gustoća | 1,049 g/cm3 (l) |
| Tačka topljenja | 16,5 °C |
| Tačka ključanja | 118,1 °C |
| Rastvorljivost | velika u vodi |
| Dipolni moment | 1,74 D |
| 1 Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
Acetatna kiselina (prema IUPAC-u: etanska kiselina, trivijalni naziv sirćetna kiselina) je bezbojna, korozivna tekućina karakterističnog mirisa. To je slaba karboksilna kiselina empirijske formule C2H4O2, odnosno sa strukturnom formulom CH3COOH. Kao dodatak hrani označena je kao E260. Vodena otopina acetatne kiseline se u svakodnevnom govoru naziva sirće. Soli i esteri acetatne kiseline zovu se acetati ili etanoati. U biohemiji preferira se naziv acetat, pošto je acetatna kiselina u fiziološkim uslovima prisutna uglavnom deprotonirana kao acetatni anion (CH3COO-).[1][2][3][4]
Nomenklatura[uredi | uredi izvor]

Sirćetna kiselina je uobičajeni naziv, u najširoj upotrebi, posebno u literaturi koja nije direktno vezana za organsku hemiju. Acetatna kiselina je naziv koji priznat od IUPAC koji je također dosta korišten naročito zbog direktne asocijacije sa solima ove kiseline - acetatima. Potiče od latinske reči acetum (=sirće). Prema IUPAC nomenklaturi organskih jedinjenja, sistemsko ime je etanska kiselina ali se ovaj naziv izuzetno rijetko koristi, osim za objašnjenja nomenklature i u nazivima derivata. Glacijalna i,li ledena sirćetna kiselina također je trivijalni naziv koji se koristi za bezvodni, kristalni oblik ove kiseline koji se javlja na temperaturama ispod 16,5 °C.
Skraćeni oblik pisanja sirćetne kiseline je AcOH, gdje je Ac acetatna grupa (CH3C(=O)-). Ovakav vid prikazivanja je praktičan, budući da ističe reaktivni centar spoja. Drugi načini prikazivanja, kao što je onaj kiselog eksplicitnog vodika uz zamjenu cijelog acetatnog aniona, kao što je Ac (AcH), nisu isprevni i stvaraju zabunu. Sve navedene varijante su prihvatljive uglavnom u organskoj hemiji, jer je oznaka Ac standardno rezervirana za element aktinij, pa se njena upotreba u općoj i neorganskoj hemiji izbjegava.

Hemijska svojstva[uredi | uredi izvor]
Kiselost[uredi | uredi izvor]
Sirćetna kiselina je slaba monoprotonska kiselina sa konstantom aciditeta od 4,8. Kiselost potiče od kiselog vodika karboksilne grupe kojeg može otpustiti, kaDA nastaje acetatni anion - konjugirana baza sirćetne kiseline. Jednomolarni rastvor ove kiseline ima PH vrijednost od oko 2,4 što ukazuje da je konstanta disocijacije tek oko 0,4%, tj. da tek taj procenat molekula otpušta proton.
Dimerizacija[uredi | uredi izvor]

Isprekidane linije predstavljaju vodonične veze
Kristalna struktura sirćetne kiseline pokazuje da se njene molekule uparuju u ciklične dimere povezane vodikovom vezom.[5] Dimere je moguće zapaziti i u gasnoj fazi, na temperaturi od 120 °C. Dimeri se pojavljuju i u tečnoj fazi, u rastvorima sa rastvaračima koji new obrazuju vodikove veze[6], a u izvesnom stepenu i u čistoj kiselini; dimerizaciju, međutim, ometaju rastvarači kao što je voda, u kojoj se obrazuju vodonične veze. Entalpija disocijacije dimera je u intervalu 65,0–66,0 kJ/mol, dok je entropija oko 154–157 J mol−1 K−1.[7]. Ovakva svojstva dimerizacije su zajednička za većinu nižih karboksilnih kiselina.
Sirćetna kiselina kao rastvarač[uredi | uredi izvor]
Tečna acetatna kiselina je polaran hidrofilni protični rastvarač, svojstava sličnih vodi i etanolu. Ima umjerenu dielektričku konstantu od 6,2; što omogućava da rastvara ne samo neorganske soli već i brojne nepolarne spojeve, kao što su lipidi i neki elementi (npr. sumpor i jod). Dobro se rastvara i u polarnim rastvaračima , kao što je voda, ali i u nepolarnim – kao što su benzen i hloroform. Dobra rastvorljivost i povoljna rastvaračka svojstva daju ovoj kiselini široke mogućnosti primjene u industriji.
Hemijske reakcije[uredi | uredi izvor]
Sirćetna kiselina djeluje korozijski na veliki broj metala, kao što su željezo, magnezij i cink, pri čemu nastaju metalni acetati, uz izdvajanje vodika. Aluminij je indiferentan na njen uticaj, jer se ovaj, pri izlaganju kisiku iz vazduha, presvlači tankim slojem aluminij-oksida koji sprečava moguću reakciju sa kiselinom. Zato se, u transportu sirćetne kiseline mogu upotrebljavati aluminijske cisterne. Kao i sve kiseline, sa bazama, baznim oksidima i nekim konjugirnim bazama stupa u reakciju neutralizacije. Sa izuzetkom hrom-acetata, gotovo svi acetati su rastvorljivi u vodi:
- Mg(s) + CH3COOH(aq) → Mg(CH3COO)2(aq) + H2 (g)
- HCO3- + CH3COOH ⇌ CH3COO- + H2O + CO2
Sirćetna kiselina učestvuje i u svim reakcijama koje su svojstvene karboksilne kiselinekarboksilnim kiselinama. Njenom redukcijom dobija se etanol, a nukleofilnim acilnom supstitucijom moguće je dobiti derivate kao što su etanoil-halogenidi, koji se mogu koristiti u reakcijama kao što je Fridel-Kraftsovo aciliranje. Drugi važni derivati su anhidrid sirćetne kiseline čijom hidrolizom se dobijaju dva molekula kiseline, te brojni estri (koji se mogu dobiti Fischerovom esterifikacijom) i amidi. Na temperaturama iznad 440 °C dolazi do degradacije kiseline, kada se dobijaju metan i ugljik(IV)-oksid ili keten i voda.
Biohemija[uredi | uredi izvor]
Acetatna grupa, koja je izvedena iz sirćetne kiseline, esencijalna je za biohemiju većine oblika života. Vezana za koenzim A, ona je centar metabolizma ugljikohidrata i masti. Međutim, koncentracija slobodnih oblika sirćetne kiseline u organizmu regulirana je na minimum zbog izbegavanja poremećaja u regulaciji kiselosti ćelijskog sadržaja. Za razliku od viših karboksilnih kiselina (prvenstveno masnih), sirćetne kiseline nema u prirodnim trigliceridima. Veštački triglicerid triacetin se široko upotrebljava kao prehrambeni aditiv, a koristi se i u kozmetičkim proizvodima, te u nekim preparatima u farmaciji.
Sirćetnu kiselinu proizvode iluče neke bakterije, od kojih su, uz Clostridium acetobutylicum, najpoznatiji predstavnici roda Acetobacter. Široko su rasprostranjene u hrani, vodi i zemljištu, a sirćetna kiselina prirodno nastaje pri kvarenju voća i druge hrane. Acetatna kiselina je također i sastojak prirodnog vaginalnog lubrikanta koji se izlučuje kod ljudi i drugih primata, gde se čini da ima ulogu blagog antibakterijskog agensa.[8]
Proizvodnja[uredi | uredi izvor]
Sirćetna kiselina se proizvodi sintetički i bakterijskom fermentacijom. Danas se biološkim putem dobija tek oko 10% svetske proizvodnje, ali ovaj način dobijanja i dalje ima veoma važnu ulogu u biotehnološkoj proizvodnji sirćeta, jer legislativca velikog broja zemalja propisuju da sirće za upotrebu u ishrani mora biti biološkog porekla. Najveći dio svjetskih potreba za ovom kiselinom se podmiruje sintetički, a čak 75% samo procesom karboksilacije metanola, uz manju zastupljenost drugih načina koji ostvaruju oko 15% ukupno proizvedene godišnje količine.
Godišnje se proizvede oko 5 miliona tona sirćetne kiseline, a oko 1,5 miliona tona se dobija reciliranjem, dajući ukupnu veličinu godišnjeg tržišta od oko 6,5 miliona. Najveći dio se proizvodi u SAD (2,5 Mt/a), zatim u Evropi (1 Mt/a) i u Japanu (0,7 Mt/a). Evropska proizvodnja sirćetne kiseline je u opadanju.
Preostale potrebe se podmiruju iz bioloških izvora i petrohemijske industrije. Glavna industrijska postrojenja primjenjuju hemijske reakcije karboksilacije i oksidacije tri prekursora:
Reference[uredi | uredi izvor]
- ^ Atkins P., de Paula J. (2006): Physical chemistry, 8th Ed. W. H. Freeman, San Francisco, ISBN 0-7167-8759-8
- ^ Binder H. H. (1999): Lexikon der chemischen Elemente. S. Hirzel Verlag, Stuttgart, ISBN 3-7776-0736-3.
- ^ Whitten K.W., Gailey K. D. and Davis R. E. (1992): General chemistry, 4th Ed. Saunders College Publishing, Philadelphia, ISBN 0-03-072373-6.
- ^ Petrucci R.H., Harwood W.S. and Herring F.G. (2002): General Chemistry, 8th Ed. Prentice-Hall, New York, ISBN 0-13-014329-4.
- ^ Jones R.E., Templeton, D.H. (1958): The crystal structure of acetic acid. Acta Crystallogr., 11 (7): 484–87.
- ^ Briggs J. M., Nguyen T. B., Jorgensen W. L. (1991): Monte Carlo simulations of liquid acetic acid and methyl acetate with the OPLS potential functions. J. Phys. Chem., 95: 3315-3322.
- ^ Togeas J. B. (2005): Acetic acid vapor: 2. A Statistical Mechanical Critique of Vapor Density Experiments.J. Phys. Chem. A, 109: 5438-5444.doi:10.1021/jp058004j
- ^ Dictionary of Organic Compounds (6th Edn.), Vol. 1 (1996). London: Chapman & Hall. ISBN 0-412-54090-8
- ^ Suresh B. (2003): "Acetic Acid". CEH Report 602.5000, SRI International.
Vanjski linkovi[uredi | uredi izvor]
| Acetic acid na Wikimedia Commonsu. |
- http://www.svethemije.com/?q=node/425
- http://www.npi.gov.au/substances/acetic-acid/index.html National Pollutant Inventory - Acetic acid fact sheet]
- http://www.cdc.gov/niosh/npg/npgd0002.html NIOSH Pocket Guide to Chemical Hazards]
- http://www.cdc.gov/niosh/docs/2003-154/pdfs/1603.pdf Method for sampling and analysis]
- http://www.osha.gov/pls/oshaweb/owadisp.show_document?p_table=STANDARDS&p_id=9992 29 CFR 1910.1000, Table Z-1]

