Amid
Na ovoj stranici konstatovane su greške u izvornom kodu koje možda dovode do nepoželjnih rezultata. |



Amidi su organski spojevi koji imaju funkcijsku grupu sastavljenu od acil grupe (R-C=O) vezane za atom dušika. Naziv se odnosi na tu klasu spojeva, kao i na funkcijsku grupu unutar tih jedinjenja. Naziv amid također označava i deprotonirani oblik amonijaka (NH3) ili amina, često prikazanih kao anioni R2N-. Ovaj članak razmatra amid u karbonilno-dušičnom smislu.
Struktura i vezanje[uredi | uredi izvor]
Najjednostavniji amidi su izvedenice amonijaka u kojima je atom vodika zamijenjen acil grupom (RC(O)NH2). Blisko srodni, a znatno brojniji su amidi koji su izvedeni iz glavnih amina (R'NH2) sa formulom RC(O)NHR'. Amidi su također često izvedeni iz sekundarnih amina (R'RNH) pa je njihova formula RC(O)NR'R.
Amidi se uobičajeno smatraju izvedenicama karboksilnih kiselina, gdje je hidroksilna grupa zamijenjena aminom ili amonijakom.[1][2][3][4][5][6]
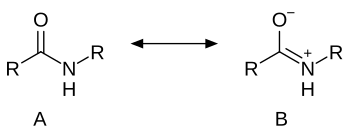
Slobodni elektronski par dušika je delokaliziran na karbonilnu grupu, stvarajući djelimičnu dvostruku vezu između dušika i karbonilnog ugljika. U skladu s tim, dušik u amidima nije piramidan. Acetamid je opisan rezonantnom hemijskom strukturom A sa 62% i B sa 28%.[7]
Nomenklatura[uredi | uredi izvor]
Prema uobičajenoj nomenklaturi, oznaka "amid" se dodaje na korijen imena kiseline. Tako se najjednostavniji amid sirćetne kiseline naziva acetamid (CH3CONH2). IUPAC preporuka je da to bude etanamid, iako se ovo i srodna formalna imena rijetko koriste. Kad je amid izveden iz glavnog ili sekundarnog oblika, zamjene na dušiku se stavljaju na početak imena. Amid koji sadrži dimetilamin i sirćetne kiseline je N,N–dimetilacetamid (CH3CONMe2, gdje je *Me = CH3). Uobičajeno je da se ovo ime dalje pojednostavi kao dimetilacetamid. Ciklični amidi se nazivaju laktamima, a sekundarni su ili tercijarni amidi. Funkcijske grupe koje sadrže –P(O)NR2 i -SO2NR2 su fosfonamidi, odnosno sulfonamidi.
Sinteza[uredi | uredi izvor]
Amidi uglavnom nastaju od karboksilnih kiselina i amina:
- RCO2H + R'R"NH RC(O)NR'R" + H2O.
S obzirom na to, ova reakcija nastanka amida je nepovoljna za ravnotežu, jer postoje mnogi načini da je prebace na desnu stranu. Većina vremena odlazi u "aktiviranje" kiseline, kao naprimjer, pretvarajući je u hlorid acil (R-CO-Cl) uklanjajući HCl zarobljen putem amina.
Proizvod HCl može se neutralisati aminom, ali i dodavanjem senzorskog protona kao što je piridinski.
Najpoznatiji način korištenja ove tehnike je Schotten-Baumannova reakcija.
Druga mogućnost je da se krene od kiseline (R-CO-O-CO-R) sa oslobađanjem karboksilne kiseline, koja reaguje sa drugim ekvivalentnim aminom.
Proizvedena kiselina nije dovoljna da reaguje prilikom stvaranja amida od amina. Također je moguće koristiti aktivirane karboksilne kiseline reagense peptidnih veza, reagujući na karboksilne kiseline i amine da stvaraju soli koje se dehidracijom mogu pretvoriti u amid ili iz okima, kao u Beckmanovoj reakciji.
- Reakcije za sintezu amida
| Reakcija | Reaktanti | Detalji |
| Beckmannov rearanžman | Ciklični keton | Reaktanti : Hidroksilamin i kiselina |
| Schmidtova reakcija | Ketoni, dušična kiselina | |
| Hidroliza nitrila | Nitril, voda | Kisela kataliza |
| Willgerodt-Kindlerova reakcija | Arilalkilcetini, sumpor i amin (morfolin) | |
| Passerinijeva reakcija | Karboksilna kiselina, ketoni i aldehidi | |
| d'Ugijeva reakcija | Izocijanat, karboksilna kiselina, keton, glavni amin | |
| Bodroux reakcija[8] ·[9] | Karboksilna kiselina, organomagnezij sa derivatom anilina (ArNHR') | 
|
| Chapmanov rearanžman[10][11] | Arilski imino eter | Za N, - Dialil amid. Mehanizam reakcija zasniva se na aromatskoj nukleofilnoj supstituciji[12] 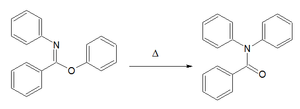
|
| Leuckartova sinteza amida[13] | Izocijanat | Reakcija sa izocijanatom katalizirano aluminij kloridom, uz aromatskog amida. |
Ostale metode[uredi | uredi izvor]
Jednostavna reakcija između alkohola i amina nikada nije pokušana prije 2007. godine, kada je prijavljen katalizator na bazi jezgre rutenija, koji je sposoban za obavljanje "dehidrogenizacijske acilacije"
Generisanje divodikovog gasa nadoknađuje nepovoljnu termodinamiku. Smatra se da se ova reakcija odvija putewm alkoholne dehidratacije aldehida, a zatim slijedi nastanak hemiamina, pa druga dehidratacija kojom nastaje amid. Nije uočeno da prilikom obezvodnjavanja hemiamina nastaje imin.
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Harrison L. G. (2011): The shaping of life: The generation of biological pattern. Cambridge University Press, ISBN 978-0-521-55350-6; http://books.google.com/books?id=-IPG-vg7Pr8C.
- ^ Hadžiselimović R., Pojskić N. (2005): Uvod u humanu imunogenetiku. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-3-4.
- ^ Alberts B. (2002)ː Molecular biology of the cell. Garland Science, New York, ISBN 0-8153-3218-1.
- ^ Bajrović K, Jevrić-Čaušević A., Hadžiselimović R., Ed. (2005): Uvod u genetičko inženjerstvo i biotehnologiju. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 9958-9344-1-8.
- ^ Kapur Pojskić L., Ed. (2014): Uvod u genetičko inženjerstvo i biotehnologiju, 2. izdanje. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo, ISBN 978-9958-9344-8-3.
- ^ Hall J. E., Guyton A. C. (2006): Textbook of medical physiology, 11th edition. Elsevier Saunders, St. Louis, Mo, ISBN 0-7216-0240-1.
- ^ Carl R. Kemnitz and Mark J. Loewen (2007). "Amide Resonance Correlates with a Breadth of C-N Rotation Barriers". J. Am. Chem. Soc. 129 (9): 2521–2528. doi:10.1021/ja0663024.
- ^ Bodroux F., Bull. Soc. Chim. France, 1905, 33, 831
- ^ Bodroux reaction at the Institute of Chemistry, Skopje, Macedonia Link Arhivirano 24. 9. 2015. na Wayback Machine
- ^ Schulenberg, J. W.; Archer, S. Org. React. 1965, 14.
- ^ A. W. Chapman, CCLXIX. - Imino-aryl ethers. Part III. The molecular rearrangement of N-phenylbenziminophenyl ether, Journal of the Chemical Society, Transactions, 127: 1992-1998, 1925. doi:10.1039/CT9252701992
- ^ Jerry March J.: Organic Chemistry, Reactions, mechanisms and structure, Šablon:3eŠablon:Éd. ISBN 0-471-85472-7
- ^ Leuckart R. (1885): Ueber einige Reaktionen der aromatischen Cyanate, Berichte der deutschen chemischen Gesellschaft, Šablon:Vol.18, issue 1, Šablon:P.873-877, doi:10.1002/cber.188501801182
Vanjski linkovi[uredi | uredi izvor]
- https://web.archive.org/web/20131026144026/http://www.organic-reaction.com/synthetic-protocols/coupling-reagents-in-amide-synthesis Sinteza amida]
- http://www.rsc.org/Chemsoc/Chembytes/IUPACGoldbook.asp IUPAC
| Commons ima datoteke na temu: Amid |