Enzim razgradnje glikogenskih grana
| Amilo-α-1,6-glukozidaza | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifikatori | |||||||||
| EC broj | 3.2.1.33 | ||||||||
| CAS broj | 9012-47-9 | ||||||||
| Baze podataka | |||||||||
| IntEnz | IntEnz pregled | ||||||||
| BRENDA | BRENDA unos | ||||||||
| ExPASy | NiceZyme pregled | ||||||||
| KEGG | KEGG unos | ||||||||
| MetaCyc | metabolički put | ||||||||
| PRIAM | profil | ||||||||
| PDB strukture | RCSB PDB PDBj PDBe PDBsum | ||||||||
| Ontologija gena | AmiGO / QuickGO | ||||||||
| |||||||||

Enzim razlaganjs glikogenskih grana ili Enzim kresanja grana je molekula koja pomaže olakšavanju razgradnje glikogena, koji služi kao skladište glukoze u tijelu, aktivnošću glukoziltransferaza i glukozidaza. Zajedno sa fosforilazama, ovi enzimi mobiliziraju rezerve glukoze iz glikogenskih naslaga u mišićima i jetri. Ovo predstavlja glavni izvor energetskih rezervi u većini organizama. Razgradnja glikogena u tijelu je visoko regulirana, posebno u jetri, putem raznih hormona, uključujući insulin i glukagon, da bi se održao homeostatski balans razine glukoze u krvi. Kada je razgradnja glikogena ugrožena mutacijama u sintezi ovog enzima, javljaju se metaboličke bolesti, kao što je bolest bolest glikogenske pothranjenosi tipa III.
Kod sisara, kvasca i nekih bakterija, glukoziltransferaza i glukozidaza se priređuju jednim enzimom, dok u E. coli i drugih bakterija, to čine dva različita enzima, što komplicira nomenklaturu. Proteini koji kataliziraju obje funkcije se nazivaju glikogen enzimi za rszlaganje glikogenskih grana ili enzimi kresanja glikogenskih grana (GDE). Kada se glukoziltransferaza i glukozidaza kataliziraju različitim enzimima, "glikogena za skidanje grana" obično se odnosi na glukozidazni enzim. U nekim izvorima, enzim koji je sposoban samo za glukozidaze se naziva "kresajući enzim ".[5][6]
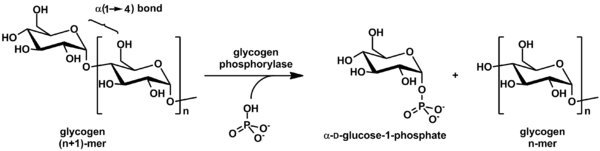
.
Struktura i aktivnost[uredi | uredi izvor]
Dva enzima[uredi | uredi izvor]
U Escherichia coli i drugih bakterija, glukoziltransferaza i glukozidaza djeluju putem dva različita enzima. U E. coli , transfer glukoze obavlja 4-alfa-glukanotransferaza, protein od 78,5 kDa,koji je kodiran genom malQ. Drugi protein, zvani enzim za otklanjane grana, razlaganje obavlja alfa-1 , 6-glukoza. Ovaj enzim ima molekulsku masu od 73,6 kDa, a kodiran genom glgX. Aktivnost ova dva enzima ne odvija se uvijek nužno zajedno. U E. coli glgX selektivno katalizira razlaganje 4-podjedinične grane, bez akcije glukanotransferaze. Proizvod ovog razlaganja, maltotetraoza, dodatno degradira maltodekstrin fosforilaza.[7][8][9]
Gen GlgX E. coli je strukturno sličan proteinu izoamilazi. Monomerni protein sadrži centraln domen u kojem je osam paralelnih beta-lanaca okružeo sa osam paralelnih alfa niti. Unutar ove strukture je rascjep dužine 26 angstrema, a širok 9 angstrema, koji sadrži aromatske ostatke za koje se smatra da, prije razlaganja, stabiliziraju četveroglukozne grana.[5]
Jedan enzim sa dva katalitska mjesta[uredi | uredi izvor]
Kod sisara i kvasaca, jedan enzim obavlja obje funkcije uklanjanja glikogenskih grana. Ljudski enzim uklanjanja grana glikogena debranching (gen: AGL) je monomer s molekulskom masom od 175 kDa. Dokazano je da dvije katalitske akcije AGL mogu funkcionirati neovisno jedna od druge, što pokazuje da je prisutno više aktivnih smjesta. Ova pojava je ojačana aktivnim mjestom inhibitora, kao što je polihidroksiamin, za koji je utvrđeno da inhibiraj glukozidaznu aktivnost dok transferazna nije mjerljivo promijenjena. Enzim za razlaganje glikogenskih grana je jedini poznati eukariotski enzim koji sadrži više katalitskih mjesta i koji je aktivan kao monomer.
Neke studije su pokazale da je pola kvašćevih GDE C-krajeva je povezano sa glukozidaznom aktivnosti, dok je pola N-krajeva povezano sa aktivnosti glukoziltransferaze. Osim ova dva aktivna mjesta, čini se da AGL sadrži itreće aktivno mjesto koji omogućava da se veže za glikogenski polimer. Iako je kompletna struktura GDE kod eukariota tek treba da se utvrdi, misli se da se vežu za šestomolekulske lance glukoze kao i razgranate glukoze, što odgovara sedam podjedinice u aktivnom mjestu, kao što je prikazano na slici ispod.[10][11][12][13][14][15][16][17][18][19][20]
Može se uočiti da kada je glukoza u aktivnom mjesatu 'A', 'B', 'C' i '0, hidrolizira se najbrže. Ovo ukazuje da je ovaj region veza lanca glikogena najjači na aktivnom mjestu, jer jača interakcija između enzima i supstrata dovodi do brže hidrolize. Unatoč ovom napretku, kompletna strukturu GDE u eukariota tek treba da se utvrdi. Enzimi koji razlažu glikogen u archaea Sulfolobus solfataricus je bolje okarakterizran od onih kod eukariota. GDE u S. solfataricus je poznat kao Trex. Iako, kao i sisarski GDE, Trex ima i amilozidazne i glukanotransferazne funkcije, Trex je strukturno sličan glgX i ima masu od 80 kD i jedno aktivno mjesto. Za razliku od glgX ili AGL, međutim, Trex u otopini postoji kao dimer i tetramer. Izgleda da oligomerni oblik Trex-a ima značajnu ulogu u izmjeni i oblik i funkcije enzima. Smatra se da dimerizacija stabilizira "fleksibilne petlje" koje se nalaze u neposrednoj blizini aktivnog mjesta. To može biti ključ za objašnjenje zašto TREX (i ne glgX) ispoljava glukoziltransferaznu aktivnost. Kao tetramera, katalitske efikasnosti TREX su povećana četiri puta, u odnosu na svoj dimerni oblik.[5][11][12][15]
Genetička lokcija[uredi | uredi izvor]
Službeni naziv za gen je "amylo- α-1,6- glukozidaza, α- glukanotransferaze 4-", sa službenim simbolom AGL. AGL je autosomni gen koji se nalazi na hromosomu 21, pozicija: lp21. AGL gen sadrži upute za izradu nekoliko različitih verzija, poznatih kao [[izoforma|izoformegg, enzima za razlaganje glikogenskih grana. Ove izoforme razlikuju se po veličini i ispoljavaju se u različitim tkivima, kao što su jetra i mišići. Ovaj gen je studiran u detalje, jer njegova mutacija je uzrok bolesti skladištenja glikogena, tipa III. Gen je dug 85 kb, a ima 35 egzona i kodira za 7,0 kb-iRNK. Translacija gena počinje u egzonu 3, koji kodira prvih 27 aminokiselina AGL, jer su prva dva egzona (68kb) sadrže neprevedene 5' regije. Eksoni 4-35 kodiraju preostalih 1.505 aminokiselina koje kodira AGL gen.[21][22][23][24]
Klinički značaj[uredi | uredi izvor]
Kada je ugrožena aktivnost GDE, tijelo ne može efikasno otpuštati uskladišteni glikogen, pa se jvlja tip III bolesti skladištenja glikogena (zbog nedostatka enzima), što je autosomno recesivni poremećaj. Razgradnja GSD III glikogen je nepotpuna i ne postoji akumulacija abnormalnog glikogena sa kratkim vanjskim granama.
Većina pacijenata pokazuju nedostatak GDE iu jetri i mišićima (tp IIIa), iako 15% pacijenata sadrži GDE u mišićima, a koji je odsutan iz jetri (Tip IIIb). Ovisno o mjestu mutacije, različite mutacije u AGL genu mogu uticati na različite izoforme ekspresije gena. Naprimjer, mutacije koje se javljaju na egzonu 3, utiču na oblik koji djeluje na izoforme koje su je prvenstveno izražene u jetri; to dovodi do pojave GSD tip III.
Ove različite manifestacije proizvode raznovrsne simptome, koji mogu biti gotovo isti kao kod tipa I GSD, uključujući i hepatomegaliju, hipoglikemiju kod djece, nizak rast, miopatije i kardiopatije.
Pacijenti sa tipom IIIa često imaju simptome koji se odnose na bolesti jetre i progresiju u mišićnima, sa varijacijama koji su uvjetovani godinom početka, stopom progresije i ozbiljnosti bolesti. Pacijenti s Tip IIIb obično simptome koji se odnose na bolest jetre.[24] Pacijenti sa tipom III se razlikuju po povišenim enzimom jetre, sa normalnim razinam mokraćne kiseline i laktata u krvi, za razliku od drugih oblika GSD. U pacijenata sa uključenošću mišića, tip IIIa, mišićn slabost postaje dominantna u odrasloj dobi i može dovesti do hipertrofije srčanih komora i distalnih mišića.
Reference[uredi | uredi izvor]
- ^ a b c GRCh38: Ensembl release 89: ENSG00000162688 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000033400 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b c Song HN, Jung TY, Park JT, Park BC, Myung PK, Boos W, Woo EJ, Park KH (juni 2010). "Structural rationale for the short branched substrate specificity of the glycogen debranching enzyme GlgX". Proteins. 78 (8): 1847–55. doi:10.1002/prot.22697. PMID 20187119.CS1 održavanje: upotreba parametra authors (link)
- ^ Bao Y, Dawson TL, Chen YT (decembar 1996). "Human glycogen debranching enzyme gene (AGL): complete structural organization and characterization of the 5' flanking region". Genomics. 38 (2): 155–65. doi:10.1006/geno.1996.0611. PMID 8954797.CS1 održavanje: upotreba parametra authors (link)
- ^ Chen YT, He JK, Ding JH, Brown BI (decembar 1987). "Glycogen debranching enzyme: purification, antibody characterization, and immunoblot analyses of type III glycogen storage disease". Am. J. Hum. Genet. 41 (6): 1002–15. PMC 1684360. PMID 2961257.CS1 održavanje: upotreba parametra authors (link)
- ^ "Glycogen debranching enzyme - Homo sapiens (Human)". UniProt.
- ^ Gillard BK, White RC, Zingaro RA, Nelson TE (septembar 1980). "Amylo-1,6-glucosidase/4-alpha-glucanotransferase. Reaction of rabbit muscle debranching enzyme with an active site-directed irreversible inhibitor, 1-S-dimethylarsino-1-thio-beta-D-glucopyranoside". J. Biol. Chem. 255 (18): 8451–7. PMID 6447697.CS1 održavanje: upotreba parametra authors (link)
- ^ Gillard BK, Nelson TE (septembar 1977). "Amylo-1,6-glucosidase/4-alpha-glucanotransferase: use of reversible substrate model inhibitors to study the binding and active sites of rabbit muscle debranching enzyme". Biochemistry. 16 (18): 3978–87. doi:10.1021/bi00637a007. PMID 269742.CS1 održavanje: upotreba parametra authors (link)
- ^ a b Woo EJ, Lee S, Cha H, Park JT, Yoon SM, Song HN, Park KH (oktobar 2008). "Structural insight into the bifunctional mechanism of the glycogen-debranching enzyme TreX from the archaeon Sulfolobus solfataricus". J. Biol. Chem. 283 (42): 28641–8. doi:10.1074/jbc.M802560200. PMC 2661413. PMID 18703518.CS1 održavanje: upotreba parametra authors (link)
- ^ a b "TreX - Actinoplanes sp. SN223/29". UniProt.
- ^ "Glycogen debranching enzyme - Escherichia coli O139:H28 (strain E24377A / ETEC)". UniProt.
- ^ "4-alpha-glucanotransferase - Escherichia coli (strain K12)".
- ^ a b Park JT, Park HS, Kang HK, Hong JS, Cha H, Woo EJ, Kim JW, Kim MJ, Boos W, Lee S, Park KH (2008). "Oligomeric and functional properties of a debranching enzyme (TreX) from the archaeon Sulfobus solfataricus P2". Biocatalysis and Biotransformation. 26: 76–85. doi:10.1080/10242420701806652.CS1 održavanje: upotreba parametra authors (link)
- ^ Talente GM, Coleman RA, Alter C, Baker L, Brown BI, Cannon RA, Chen YT, Crigler JF, Ferreira P, Haworth JC, Herman GE, Issenman RM, Keating JP, Linde R, Roe TF, Senior B, Wolfsdorf JI (februar 1994). "Glycogen storage disease in adults". Ann. Intern. Med. 120 (3): 218–26. doi:10.7326/0003-4819-120-3-199402010-00008. PMID 8273986.CS1 održavanje: upotreba parametra authors (link)
- ^ Satdarshan P. S. Monga (2010). Molecular Pathology of Liver Diseases (Molecular Pathology Library). Berlin: Springer. ISBN 1-4419-7106-8.
- ^ Hondoh H, Saburi W, Mori H et al. (maj 2008). "Substrate recognition mechanism of alpha-1,6-glucosidic linkage hydrolyzing enzyme, dextran glucosidase from Streptococcus mutans". J. Mol. Biol. 378 (4): 913–22. doi:10.1016/j.jmb.2008.03.016. PMID 18395742. Eksplicitna upotreba et al. u:
|authors=(pomoć)CS1 održavanje: upotreba parametra authors (link) - ^ McCarter JD, Withers SG (decembar 1994). "Mechanisms of enzymatic glycoside hydrolysis". Curr. Opin. Struct. Biol. 4 (6): 885–92. doi:10.1016/0959-440X(94)90271-2. PMID 7712292.CS1 održavanje: upotreba parametra authors (link)
- ^ Yamamoto E, Makino Y, Omichi K (maj 2007). "Active site mapping of amylo-alpha-1,6-glucosidase in porcine liver glycogen debranching enzyme using fluorogenic 6-O-alpha-glucosyl-maltooligosaccharides". J. Biochem. 141 (5): 627–34. doi:10.1093/jb/mvm065. PMID 17317688.CS1 održavanje: upotreba parametra authors (link)
- ^ Chiba S (august 1997). "Molecular mechanism in alpha-glucosidase and glucoamylase". Biosci. Biotechnol. Biochem. 61 (8): 1233–9. doi:10.1271/bbb.61.1233. PMID 9301101.
- ^ "Genes (Genetic Home Reference a service of U.S. National Library of Medicine". Pristupljeno 29. 2. 2012.
- ^ Shen J, Bao Y, Liu HM, Lee P, Leonard JV, Chen YT (juli 1996). "Mutations in exon 3 of the glycogen debranching enzyme gene are associated with glycogen storage disease type III that is differentially expressed in liver and muscle". J. Clin. Invest. 98 (2): 352–7. doi:10.1172/JCI118799. PMC 507437. PMID 8755644.CS1 održavanje: upotreba parametra authors (link)
- ^ a b Kishnani PS, Austin SL, Arn P et al. (juli 2010). "Glycogen storage disease type III diagnosis and management guidelines". Genet. Med. 12 (7): 446–63. doi:10.1097/GIM.0b013e3181e655b6. PMID 20631546. Eksplicitna upotreba et al. u:
|authors=(pomoć)CS1 održavanje: upotreba parametra authors (link)
Vanjski linovi[uredi | uredi izvor]
- GeneReviews/NCBI/NIH/UW entry on Glycogen Storage Disease Type III
- OMIM entries on Glycogen Storage Disease Type III
- reactome.org: Debranching enzyme transfers 3-glucose blocks from branches in limit dextrin[mrtav link]
- reactome.org: (1,6)-alpha-glucose residues are removed, as D-glucose, from limit dextrin by debranching enzyme[mrtav link]
- Glycogen debranching enzyme na US National Library of Medicine Medical Subject Headings (MeSH)
| Glycogenesis and glycogenolysis enzymes na Wikimedia Commonsu. |
| Sugar hydrolases na Wikimedia Commonsu. |







