Dicer
Dicer, znan i kao endoribonukleaza Dicer ili helikaza s RNKaznim motivom, jest enzim koji je kod ljudi kodiran genom DICER1 sa hromosoma 14. Budući da je dio porodice RNaza III, Dicer cijepa dvolančanu RNK (dsRNK) , pre-mikroRNK (pre-miRNK) u kratke dvolančane fragmente RNK zvane mala interferirajuća RNK odnosno i mikroRNK, respektivno. Ovi fragmenti su dugi otprilike 20-25 baznih parova sa dvobaznim prevjesom na 3' krajevima. Dicer olakšava aktivaciju RNK-induciranog kompleksa utišavanja (RISC), koji je neophodan za RNK- interferenciju. RISC ima katalitsku komponentu Argonaut, koja je endonukleaza sposobna da razgradi iRNK (mRNK).
Funkcionalni domeni
[uredi | uredi izvor]
Ljudski dicer (također poznat kao hsDicer ili DICER1) je klasificiran kao ribonukleaza III jer sadrži i helikazu i PAZ (Piwi/argonaut/Zwille) proteinski domen.[6][7] Pored ovih domena, hsDicer sadrži još četiri funkcionalna domena: dva Rnazna III domena i dva dvolančana RNK-vezujuća domena (domen nepoznate funkcije DUF283 i dsRBD).[8]
Sadašnja istraživanja sugeriraju da je PAZ domen sposoban da veže dva nukleotida 3' preko dsRNK dok katalitski domeni RNKaza III formiraju pseudo-dimere oko dsRNK da iniciraju cijepanje lanaca. Ovo rezultira funkcionalnim skraćivanjem lanca dsRNK. Udaljenost između domena PAZ i RNazaIII određena je uglom heliksa konektora i utiče na dužinu proizvoda mikro RNK. dsRBD domen vezuje dsRNK, iako specifično mjesto vezanja domena nije definirano. Moguće je da ovaj domen radi kao dio kompleksa sa drugim regulatornim proteinom (TRBP kod ljudi, R2D2, Loqs kod Drosophila), kako bi se efikasno pozicionirali domeni Rnaza III i tako kontrolirala specifičnost proizvoda sRNK.[9] Domen helikaze uključen je u preradu dugih supstrata.
Uloga u interferenciji RNK
[uredi | uredi izvor]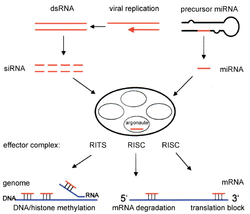
Interferencija RNK je proces u kojem razlaganje molekula RNK u miRNK inhibira ekspresiju gena specifičnih sekvenci mRNK domaćina. miRNA se proizvodi unutar ćelije počevši od primarne miRNK (pri-miRNA) u jezgro. Ove dugačke sekvence se cijepaju na manje prekursorske miRNA (pre-miRNA), koje se obično sastoje od 70 nukleotida sa strukturom ukosnice. Pri-miRNA identifikuje DGCR8 i cijepa Drosha kako bi se formirala pre-miRNA, proces koji se odvija u jezgru. Ove pre-miRNA se zatim izvoze u citoplazmu, gdje ih Dicer cijepa da formira zrelu miRNA.[11]
Mala interferirajuća RNK
[uredi | uredi izvor]Male interferirajuće RNK (siRNA) proizvode se i funkcioniraju na sličan način kao miRNK, cijepanjem dvolančane RNK dicerom na manje fragmente, dužine 21 do 23 nukleotida.[9] Obje, imiRNK i siRNK aktiviraju RNK-inducirani kompleks za utišavanje (RISC), koji pronalazi komplementarnu ciljnu sekvencu iRNK i cijepa RNK pomoću RNkaza.[12] Utišavanje pojedinih gena obavlja se putem interferencije RNK.[13] siRNK i miRNK se razlikuju po činjenici da su siRNA tipski specifične za sekvencu iRNK, dok miRNK nisu u potpunosti komplementarne sekvenci iRNK. miRNK mogu komunicirati s ciljevima koji imaju slične sekvence, što inhibira translaciju različitih gena.[14] Općenito, RNK-interferencija je bitan dio normalnih procesa u organizmima kao što su ljudi, i to je područje koje se istražuje kao dijagnostički i terapeutski alat za mete raka.[11]

Klinički značaj
[uredi | uredi izvor]Makulska degeneracija
[uredi | uredi izvor]Starosna makulska degeneracija je istaknuti uzrok sljepoće u razvijenim zemljama. Dicerova uloga u ovoj bolesti postala je očigledna nakon što je otkriveno da oboljeli pacijenti pokazuju smanjene razine dicera u svom retinskom pigmentnom epitelu (RPE). Miševi s nokautiranim dicerom, kojima je nedostajao samo u nihovom RPE, pokazali su slične simptome. Međutim, drugi miševi kojima nedostaju važni proteini RNAi puta poput Drosha i Pasha, nisu imali simptome makulne degeneracije kao sicer-nokaut-miševi. Ovo zapažanje sugerira da dicer ima specifičnu ulogu u zdravlju mrežnjače koja je neovisna o RNKi putu i stoga nije funkcija generiranja si/miRNK. Utvrđeno je da je oblik RNK zvani Alu RNK (RNK transkripti alu elementa) povišen kod pacijenata sa nedovoljnim nivoom dicera. Ovi dugi nekodirajući lanci RNK mogu u petlji formirati strukture dsRNK koje bi Dicer razgradio u zdravoj retini. Međutim, sa nedovoljnim nivoom dicera, akumulacija alu RNK dovodi do degeneracije RPE, kao posljedice upale.[15][16]
Kancer
[uredi | uredi izvor]Promijenjeni profili ekspresije miRNK kod malignih karcinoma ukazuju na ključnu ulogu miRNK, a time i dicera u razvoju i prognozi raka. miRNK mogu funkcionirati kao supresori tumora i stoga njihova izmijenjena ekspresija može rezultirati tumorigenezom.[17] U analizi karcinoma pluća i jajnika, loša prognoza i smanjeno vrijeme preživljavanja pacijenata koreliraju sa smanjenom ekspresijom dicera i drosha. Smanjeni nivoi iRNK dicera koreliraju sa uznapredovalim stadijem tumora. Međutim, visoka ekspresija dicera kod drugih karcinoma, poput prostate[18] i jednjaka pokazalo se da korelira sa lošom prognozom za pacijenata. Ova neslaganja između tipova raka sugerira da se jedinstveni RNAi regulatorni procesi koji uključuju dicer razlikuju među različitim tipovima tumora.[11]
Dicer je također uključen u popravak DNK. Oštećenje DNK se povećava u ćelijama sisara sa smanjenom ekspresijom dicera, kao posljedica smanjene efikasnosti popravljanja oštećenja DNK i drugih mehanizama. Naprimjer, siRNK iz prekida dvostrukog lanca (koji proizvodi dicer) može djelovati kao vodič za proteinske komplekse koji su uključeni u mehanizme popravke dvostrukog lanca i također može usmjeravati modifikacije hromatina. Osim toga, obrasci ekspresije miRNK se mijenjaju kao posljedica oštećenja DNK, uzrokovanog ionizujućim ili ultraljubičastim zračenjem. Mehanizmi RNKi odgovorni su za utišavanje transpozona i u njihovom odsustvu, kao kada je D dicer nokautiran/dauniran, mogu dovesti do aktiviranih transpozona koji uzrokuju oštećenje DNK. Akumulacija oštećenja DNK može rezultirati ćelijama sa onkogenim mutacijama, a time i razvojem tumora.[11]
Diceroliki proteini
[uredi | uredi izvor]Biljni genomi kodiraju proteine poput dicera sa sličnim funkcijama i proteinskim domenima kao životinjski, uključujući i insekte. Naprimjer, u modelnom organizmu Arabidopsis thaliana, napravljena su četiri proteina nalik na kockice i označena su od DCL1 do DCL4. DCL1 je uključen u stvaranje miRNK i proizvodnju sRNK iz invertiranih ponavljanja. DCL2 stvara siRNK iz cis-djelovanja antisens transkripata koji pomažu u imunosti na viruse i odbrani. DCL3 generira siRNK koja pomaže u modifikaciji hromatina, a DCL4 je uključen u metabolizam trans-aktivne siRNK i utišavanje transkripta na posttranskripcionom nivou. Dodatno, DCL 1 i 3 su važni za cvjetanje u rodu Arabidopsis. Kod arabidopsisa, nokaut DCL ne uzrokuje ozbiljne probleme u razvoju. Riža i grožđe također proizvode DCL, jer je mehanizam kockice uobičajena odbrambena strategija mnogih organizama. Riža je razvila druge funkcije za pet DCL-a koje proizvodi i oni imaju važniju ulogu u funkciji i razvoju nego u arabidopsisu. Osim toga, obrasci ekspresije se razlikuju među različitim vrstama biljnih ćelija riže, dok je ekspresija u arabidopsisu više homogena. Na ekspresiju DCL-a riže mogu uticati uslovi biološkog stresa, uključujući sušu, salinitet i hladnoću, tako da ovi stresori mogu smanjiti otpornost biljaka na viruse. Za razliku od arabidopsisa, gubitak funkcije proteina DCL uzrokuje razvojne defekte riže.[19]
Također pogledajte
[uredi | uredi izvor]- Ekspresija gena
- RISC
- RNK interferencija
- mikroRNK
- Mala interferirajuća RNK
- Drosha
- Ribonukleaza III
- iRNK
Reference
[uredi | uredi izvor]- ^ a b c GRCh38: Ensembl release 89: ENSG00000100697 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000041415 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Macrae IJ, Zhou K, Li F, Repic A, Brooks AN, Cande WZ, Adams PD, Doudna JA (Jan 2006). "Structural basis for double-stranded RNA processing by Dicer". Science. 311 (5758): 195–8. Bibcode:2006Sci...311..195M. doi:10.1126/science.1121638. PMID 16410517. S2CID 23785494.
- ^ "Entrez Gene: DICER1 Dicer1, Dcr-1 homolog (Drosophila)".
- ^ Matsuda S, Ichigotani Y, Okuda T, Irimura T, Nakatsugawa S, Hamaguchi M (Jan 2000). "Molecular cloning and characterization of a novel human gene (HERNA) which encodes a putative RNA-helicase". Biochimica et Biophysica Acta (BBA) - Gene Structure and Expression. 1490 (1–2): 163–9. doi:10.1016/S0167-4781(99)00221-3. PMID 10786632.
- ^ Hammond SM (Oct 2005). "Dicing and slicing: the core machinery of the RNA interference pathway". FEBS Letters. 579 (26): 5822–9. doi:10.1016/j.febslet.2005.08.079. PMID 16214139. S2CID 14495726.
- ^ a b Cenik ES, Fukunaga R, Lu G, Dutcher R, Wang Y, Tanaka Hall TM, Zamore PD (Apr 2011). "Phosphate and R2D2 restrict the substrate specificity of Dicer-2, an ATP-driven ribonuclease". Molecular Cell. 42 (2): 172–84. doi:10.1016/j.molcel.2011.03.002. PMC 3115569. PMID 21419681.
- ^ Hammond SM, Bernstein E, Beach D, Hannon GJ (Mar 2000). "An RNA-directed nuclease mediates post-transcriptional gene silencing in Drosophila cells". Nature. 404 (6775): 293–6. Bibcode:2000Natur.404..293H. doi:10.1038/35005107. PMID 10749213. S2CID 9091863.
- ^ a b c d Merritt WM, Bar-Eli M, Sood AK (Apr 2010). "The dicey role of Dicer: implications for RNAi therapy". Cancer Research. 70 (7): 2571–4. doi:10.1158/0008-5472.CAN-09-2536. PMC 3170915. PMID 20179193.
- ^ Vermeulen A, Behlen L, Reynolds A, Wolfson A, Marshall WS, Karpilow J, Khvorova A (maj 2005). "The contributions of dsRNA structure to Dicer specificity and efficiency". RNA. 11 (5): 674–82. doi:10.1261/rna.7272305. PMC 1370754. PMID 15811921.
- ^ Watson JD (2008). Molecular Biology of the Gene. San Francisco, CA: Cold Spring Harbor Laboratory Press. str. 641–648. ISBN 978-0-8053-9592-1.
- ^ Zeng Y, Yi R, Cullen BR (Aug 2003). "MicroRNAs and small interfering RNAs can inhibit mRNA expression by similar mechanisms". Proceedings of the National Academy of Sciences of the United States of America. 100 (17): 9779–84. Bibcode:2003PNAS..100.9779Z. doi:10.1073/pnas.1630797100. PMC 187842. PMID 12902540.
- ^ Meister G (Mar 2011). "Vision: Dicer leaps into view". Nature. 471 (7338): 308–9. Bibcode:2011Natur.471..308M. doi:10.1038/471308a. PMID 21412326.
- ^ Tarallo V, Hirano Y, Gelfand BD, Dridi S, Kerur N, Kim Y, Cho WG, Kaneko H, Fowler BJ, Bogdanovich S, Albuquerque RJ, Hauswirth WW, Chiodo VA, Kugel JF, Goodrich JA, Ponicsan SL, Chaudhuri G, Murphy MP, Dunaief JL, Ambati BK, Ogura Y, Yoo JW, Lee DK, Provost P, Hinton DR, Núñez G, Baffi JZ, Kleinman ME, Ambati J (maj 2012). "DICER1 loss and Alu RNA induce age-related macular degeneration via the NLRP3 inflammasome and MyD88". Cell. 149 (4): 847–59. doi:10.1016/j.cell.2012.03.036. PMC 3351582. PMID 22541070.
- ^ Tang KF, Ren H (2012). "The role of dicer in DNA damage repair". International Journal of Molecular Sciences. 13 (12): 16769–78. doi:10.3390/ijms131216769. PMC 3546719. PMID 23222681.
- ^ Chiosea S, Jelezcova E, Chandran U, Acquafondata M, McHale T, Sobol RW, Dhir R (Nov 2006). "Up-regulation of dicer, a component of the MicroRNA machinery, in prostate adenocarcinoma". The American Journal of Pathology. 169 (5): 1812–20. doi:10.2353/ajpath.2006.060480. PMC 1780192. PMID 17071602.
- ^ Liu Q, Feng Y, Zhu Z (Aug 2009). "Dicer-like (DCL) proteins in plants". Functional & Integrative Genomics. 9 (3): 277–86. doi:10.1007/s10142-009-0111-5. PMID 19221817. S2CID 28801338.
Vanjski linkovi
[uredi | uredi izvor]