Prokariotski citoskelet
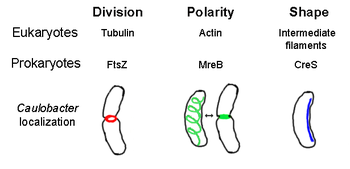
Elementi prokariotskog citoskeleta se poklapaju sa njihovim eukariotskim homolozima i hipotetskom ćelijskom funkcijom.[1]
Prokariotski citoskelet je zajednički naziv za sva strukturna vlakna prokariota. Nekada se mislilo da prokariotske ćelije nemaju citoskeleta, ali su napredak u tehnologiji vizualizacije i prepoznavanju struktura doveli do otkrića niti i u ovim ćelijama, tokom ranih 1990-ih. Ne samo da imaju analoge za sve glavne citoskeletne proteine eukariota koji su pronađena u prokariota, takođe su otkriveni i citoskeletni proteini bez poznatih eukariotskih analoga. [2][3][4][5] Citoskeletni elementi imaju ključnu ulogu u ćelijskoj diobi, zaštiti, obliovanju i određivanju polarnosti raznih prokariota.[6][7]
FTSz[uredi | uredi izvor]
FTSz, prvi identificirfani element prokariotskog citoskeleta, formira vlaknaste prstenaste strukture koje se nalaze u sredini ćelije, zvane Z-prsten koji je sužava u diobi, slično kao aktin-miozin kontraktilni prsten u eukariota. Z-prsten je vrlo dinamičra struktura koja se sastoji od brojnih snopova protofilamenata koji se istežu i skraćuju, iako je nejasan mehanizam kontrakcije Z-prstenova i broj uključenih protofilamenta.[1] FTSz djeluje kao organizator proteina i potreban je za podjelu ćelija. To je prva komponenta pregrade u citokinezi, a angažira sve druge poznate proteine podjele u tekućoj podjeli ćelije[8]
Unatoč tome, funkcionalne sličnosti aktina i FTSz je homologni eukariotski tubulin. Iako poređenje primarne strukture FTSz i tubulina otkriva slabu sličnost, njihove 3-dimenzijske strukture su izuzetno slične. Osim toga, kao što je tubulin monomer, FTSz je vezan za GTP i polimerizira sa drugim FTSz monomerima s hidrolizom GTP u mehanizmu koji je sličan tubulinskom. FTSz je od suštinskog značaja za podjelu ćelija bakterija, pa je ovaj protein je meta za dizajn novih antibiotika.
Postoji nekoliko modela i mehanizama koji reguliraju formiranje Z-prstena. Jedan od njih su predložili Rashid Aijaz i Sing Perminder. Model kritičnog gradijenta koncentracije kod bakterijskih ćelijskih dioma dostupn je u Nature Precedings.[9] U ovom modelu postoje pozitivni i negativni regulatori skupova FTSz koji formiraju gradijent unutar bakterijske ćelije. Gradijent je takav da kritična koncentracija FTSz potrebnih za okupljanje FTSz ima minimum na medijalnom položaju ćelije, pa zato Z-prsteni na kraju formira divisomni kompleks na sredini ćelije.
MreB[uredi | uredi izvor]
MreB je bakterijski protein za koji se nagađa da je analog eukariotskom aktinu. MreB i aktin imaju slabo poklapanje primarne strukture, ali su vrlo slični po 3-D strukturi i polimerizaciji filamenata.
Gotovo sve ne-sferne bakterije, u formiranju oblika, oslanjaju se na MreB. MreB se kondenzira iz svoje normalne spiralne mreže i formira uski prsten na septumu Caulobacter crescentus, neposredno prije podjele ćelije, što je mehanizam za koji se vjeruje da pomaže u pronalaženju svog centra pregrade (septuma).[10] MreB određuje oblik ćelije posredujućo poziciju polova ćelije i aktivnost enzima koji kataliziraju sintezu peptidoglikana. Djelujuje i kao čvrsti filament ispod ćelijske membrane, koji ublažava vanjski pritisak, čime utiče na oblikovanje i očvrščavanje ćelije.
Krescentin[uredi | uredi izvor]
Krescentin (kodiran Cres genom) je analog eukariotskih intermedijarnih filamenata (IF). Za razliku od drugih (pominjanih) analognih odnosa, krescentin ima prilično veliku homologiju primarne strukture fa IF proteinima, uz trodimenzijsku sličnost –s ekvenca Cres ima 25% identiteta poklapanja i 40% sličnostisa citokeratinom 19 i 24% identitetičnih poklapanja, a 40% sličnosti sa jedrovom laminom A. Osim toga, krescentinska vlakna imaju promjer oko 10 nm i time ulaze u raspon promjera eukariotskih IF (8-15 nm)[11] Krescentin formira kontinuirani vlakno od pola do pola uz unutrašnje, konkavne strane u obliku polumjeseca, kod bakterije Caulobacter crescentus. Oba, i MreB i krescentin su neophodni za C. crescentus u svom karakterističnom obliku; vjeruje se da MreB oblikuje ćelije u obliku štapa, a krescentin savija ovaj oblik u polumjesec.
Parm i SopA[uredi | uredi izvor]
Parm je citoskeletni element koji ima sličnu strukturu kao aktin, iako se funkcijski ponaša fkao tubulin. Nadalje, polimerizira dvosmjerno, što pokazuje dinamičku nestabilnost, a oba ponašanja su karakteristična za polimerizaciju tubulina. Formira sistem sa Parr i Parc koja je odgovoran za razdvajanja plazmida R1. Parm se pričvršćuje na Parr, protein DNK-vezanja koji se posebno veže za 10 direktnih ponavljanja u Parc regiji na R1 plazmidu. Ovo se obavezujuće javlja na oba kraja Parr filamenta. Ovaj filament se tada proširuje, razdvajajući plazmid Sistem je analogan segregaciji eukariotskih hromosoma, a Parm se ponaša kao eukariotski tubulin u diobenom vretenu mitoze, dok Parr djeluje poput kinetohornog kompleksa, i dijelova PARC, kao što su centromere u hromosomima.[12][13][14][14]
Kod F plazmid segregacija se javlja u sličnom sistemu u kojem SOPA djeluje kao citoskeletno vlakno,a SopB se veže za sekvence SOPC u F plazmidu, kao što su kinetohor i centromera.[14]
Sistem MinCDE[uredi | uredi izvor]
MinCDE sistem je filamentni sistem koji pravilno pozicionira septum u sredini ćelije u Escherichia coli . Prema Shih et al., MiNC inhibira formiranje septuma sprečavanjem polimerizacije Z-prstena. MiNC, uma, a MinE formiraju heliksne strukturu koja vjetrovi oko ćelije i vezan za membranu um. Heliks MinCDE zauzima pol i završava u vlaknastoj strukturi pod nazivom E-prsten, na rubu sredine većine polarne zone. Iz ove konfiguracije, E-prsten će ugovoriti i krenuti ka polovima, rastavljajući MinCDE spiralu dok se kreće zajedno. Istovremeno, j rastavljeni fragmenti se okupljaju na suprotnom polarnom kraju, preoblikujući MinCDE zavojnice na suprotnom polu, a reducira MinCDE heliks. Ovaj proces se onda ponavlja, sa MinCDE spiralom, oscilirajući od pola do pola. Ova oscilacija javlja se više puta u toku ćelijskog ciklusa, čime se čuva MiNC (i njegove septum inhibirajući učinak) na nižoj koncentraciji vremena u prosjeku na sredini ćelije nego na krajevima ćelije. Dinamičko ponašanje Min proteina se rekonstituira in vitro, pomoću veštačkog lipidnog dvosloja koji imitira ćelijske membrane. MinE i MinD se samoorganiziraju u paralelne spirale valovitih proteina u reakciji mehanizma difuzije.[12][13][14]
Baktofilin[uredi | uredi izvor]
Baktofilin je element citoskeleta koji formira vlakna u cijeloj ćeliji. Proteobacterium bacili u obliku štapa kod Myxococcus xanthus. Baktofilinski protein, BacM, je neophodan za pravilno održavanje oblika ćelije i integritet ćelijskog zida. Ćelijama M. xanthus nedostaje BacM pa imaju deformiranu morfologiju i odlikuju ih savijena tijela ćelija, a bacM mutanti imaju smanjenu otpornost na antibiotike usmjerene na zid bakterijske ćelije. BacM protein M. Xanthus se cijepa iz dugolinijskog obrasca kako bi se omogućila polimerizacija. Baktofilini su uključeni u regulaciju ćelijskog oblika i u drugih bakterija, uključujući i zakrivljenost ćelija Proteus mirabilis, [15][16][17][18]i spiralni oblik Helicobacter pylori .
Krenaktin[uredi | uredi izvor]
Krenaktin je homolog aktina homolog koji je jedinstven za carstvo Archaea koji je pronađen u redovima Crenarchaeota Thermoproteales. On ima dužu sekvencu sličnosti sa eukariotskim aktinima od svih poznatih aktinskih analoga.[19][20] Krenactin je dobro karakteriziran kod Pyryobaculum calidifontis, gdje pokazuje visoku specifičnost za ATP i GTP.[19][19][21]
Svi specifični krenaktini su kao šipke ili igličastog oblika, kao i kod P. calidifontis. Pokazalo se da krenaktin formira spiralne strukture koje obuhvataju dužinu ćelije, što ukazuje na njegovu ulogu u određivanju oblika, slično onom kod MreB u drugim prokariotima. [19]
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ a b Gitai, Z. (2005). "The New Bacterial Cell Biology: Moving Parts and Subcellular Architecture". Cell. 120 (5): 577–586. doi:10.1016/j.cell.2005.02.026. PMID 15766522.
- ^ Gunning PW, Ghoshdastider U, Whitaker S, Popp D, Robinson RC (2015). "The evolution of compositionally and functionally distinct actin filaments". Journal of Cell Science. 128 (11): 2009–19. doi:10.1242/jcs.165563. PMID 25788699.CS1 održavanje: upotreba parametra authors (link)
- ^ Popp D, Narita A, Lee LJ, Ghoshdastider U, Xue B, Srinivasan R, Balasubramanian MK, Tanaka T, Robinson RC (2012). "Novel actin-like filament structure from Clostridium tetani". The Journal of Biological Chemistry. 287 (25): 21121–9. doi:10.1074/jbc.M112.341016. PMC 3375535. PMID 22514279.CS1 održavanje: upotreba parametra authors (link)
- ^ Popp D, Narita A, Ghoshdastider U, Maeda K, Maéda Y, Oda T, Fujisawa T, Onishi H, Ito K, Robinson RC (2010). "Polymeric structures and dynamic properties of the bacterial actin AlfA". Journal of Molecular Biology. 397 (4): 1031–41. doi:10.1016/j.jmb.2010.02.010. PMID 20156449.CS1 održavanje: upotreba parametra authors (link)
- ^ Wickstead B, Gull K (2011). "The evolution of the cytoskeleton". The Journal of Cell Biology. 194 (4): 513–25. doi:10.1083/jcb.201102065. PMC 3160578. PMID 21859859.CS1 održavanje: upotreba parametra authors (link)
- ^ Shih YL, Rothfield L (2006). "The bacterial cytoskeleton". Microbiol. Mol. Biol. Rev. 70 (3): 729–54. doi:10.1128/MMBR.00017-06. PMC 1594594. PMID 16959967.CS1 održavanje: upotreba parametra authors (link)
- ^ Michie KA, Löwe J. format: https://web.archive.org/20061117lmb.cam.ac.uk:80/SS/Lowe_J/group/PDF/annrev2006.pdf. "Dynamic filaments of the bacterial cytoskeleton" Provjerite vrijednost parametra
|url=(pomoć). Annu. Rev. Biochem. 75: 467–92. PMID 16756499.CS1 održavanje: upotreba parametra authors (link)[mrtav link] - ^ Graumann, P.L. (2004). "Cytoskeletal elements in bacteria". Current Opinion in Microbiology. 7 (6): 565–571. doi:10.1016/j.mib.2004.10.010. PMID 17506674.
- ^ http://hdl.handle.net/10101/npre.2010.4659.1> (2010).
- ^ Baumeister, W.; Medalia, O.; Linaroudis, A.A. (2004). "New insights into the structural organization of eukaryotic and prokaryotic cytoskeletons using cryo-electron tomography". Exp Cell Res. 301 (1): 38–42. doi:10.1016/j.yexcr.2004.08.005. PMID 15501443.
- ^ Ausmees, N.; Kuhn, J.R.; Jacobs-Wagner, C. (2003). "The Bacterial Cytoskeleton An Intermediate Filament-Like Function in Cell Shape". Cell. 115 (6): 705–713. doi:10.1016/S0092-8674(03)00935-8. PMID 14675535.
- ^ a b Garner, E.C.; Campbell, C.S.; Mullins, R. D. (2004). "Dynamic Instability in a DNA-Segregating Prokaryotic Actin Homolog". Science. 306 (5698): 1021–1025. doi:10.1126/science.1101313. PMID 15528442.
- ^ a b Moller-Jensen, J.; Jensen, R.B.; Löwe, J.; Gerdes, K. (2002). "Prokaryotic DNA segregation by an actin-like filament". The EMBO Journal. 21 (12): 3119–3127. doi:10.1093/emboj/cdf320. PMC 126073. PMID 12065424.
- ^ a b c d Gitai, Z. (2006). "Plasmid Segregation: A New Class of Cytoskeletal Proteins Emerges". Current Biology. 16 (4): 133–136. doi:10.1016/j.cub.2006.02.007. PMID 16488865.
- ^ Koch, M.K.; McHugh, C.A.; Hoiczyk, E. (2010). "BacM, an N-terminally processed bactofilin of Myxococcus xanthus, is crucial for proper cell shape". Molecular Microbiology. 80 (4): 1031–1051. doi:10.1111/j.1365-2958.2011.07629.x. PMC 3091990. PMID 21414039.
- ^ Hay, N.A.; Tipper, D.J.; Gygi, D.; Hughes, C. (1999). "A novel membrane protein influencing cell shape and multicellular swarming of Proteus mirabilis". Journal of Bacteriology. 181 (7): 2008–2016. PMC 93611. PMID 10094.
- ^ Kühn, J.; Briegel, A.; Mörschel, E.; Kahnt, J.; Leser, K.; Wick, S.; Jensen, G.J.; Thanbichler, M. (2010). "Bactofilins, a ubiquitous class of cytoskeletal proteins mediating polar localization of a cell wall synthase in Caulobacter crescentus". The EMBO Journal. 29 (2): 327–339. doi:10.1038/emboj.2009.358. PMC 2824468. PMID 19959992.
- ^ Sycuro, L.K.; Pincus, Z.; Gutierrez, K.D.; Biboy, J.; Stern, C.A.; Vollmer, W.; Salama, N.R. (2010). "Peptidoglycan crosslinking relaxation promotes Helicobacter pylori 's helical shape and stomach colonization". Cell. 141 (5): 822–833. doi:10.1016/j.cell.2010.03.046. PMC 2920535. PMID 20510929.
- ^ a b c d Ettema, T.J.; Lindas, A.; Bernander, R. (2011). "An actin-based cytoskeleton in archaea". Molecular Microbiology. 80 (4): 1052–61. doi:10.1111/j.1365-2958.2011.07635.x. PMID 21414041.
- ^ Yutin, N.; Wolf,M.Y.; Wolf, Y.I., Koonin, E.V. (2009). "The origins of phagocytosis and eukaryogenesis". Biology Direct. 4: 9. doi:10.1186/1745-6150-4-9. PMC 2651865. PMID 19245710.CS1 održavanje: više imena: authors list (link)
- ^ Ghoshdastider U, Jiang S, Popp D, Robinson RC (2015). "In search of the primordial actin filament". Proc Natl Acad Sci U S A. 112 (30): 9150–1. doi:10.1073/pnas.1511568112. PMID 26178194.CS1 održavanje: upotreba parametra authors (link)
Vanjski linkovi[uredi | uredi izvor]
| Prokaryotic cytoskeleton na Wikimedia Commonsu. |

