Receptori spregnuti sa G-proteinom
| GPCR | |
|---|---|
 | |
| Identifikatori | |
| Simbol | 7tm-1 |
G-protein spregnuti receptori (GPCR) – poznati i kao sedmotransmembranski domen receptori, 7TM receptori, heptaheliksni receptori, serpentinski receptori i G protein-vezani receptori (GPLR) – su velika proteinska porodica transmembranskih receptora koji reagiraju na vanćelijske molekule i aktiviraju unutrašnje puteve transdukcije signala. Krajnji rezultat te uloge je ćelijski odgovor. G protein spregnuti receptori su prisutni samo kod eukariota, uključujući kvasac, hoanoflagelate[1] i životinje. Ligandi koji se vežu i aktiviraju ove receptore su: fotosenzitivni spojevi, mirisi, feromoni, hormoni i neurotransmiteri. Oni, po veličini, variraju od malih molekula do peptida i velikih proteina. G protein spregnuti receptori imaju učešća u mnogim bolestima i pa su zato biološka meta za preko 30% svih modernih lijekova.[2][3] Brajan Kobilka i Robert Lefkovic su 2012. dobili Nobelovu nagradu za hemiju za rad koji je bio „presudan za razumijevanje načina na koji funkcioniraju G protein spregnuti receptori“.[4]
Postoje dva osnovna načina prijenosa signala posredstvom G protein spregnutih receptora:
- cAMP signalni put i
- fosfatidilinozitolni signalni put.[5]
Kada se ligand veže za GPCR, izaziva konformacijsku promjenu receptora, omogućavajući mu da deluje kao faktor razmjene guanin nukleotida (GEF). Nakon vezanja liganda, GPCR može aktivirati vezani G-protein, zamjenom za njega vezanog GDP-a sa GTP-om. G proteinska α podjedinica, skupa sa vezanim GTP-om, pa tada može disocirati do β i γ podjedinica i formirati interakcije sa unutarćelijskim signalnim proteinima ili direktno sa ciljnim funkcionalnim proteinima, zavisno od tipa α podjedinice (Gαs, Gαi/o, Gαq/11, Gα12/13).[6]:1160
Klasifikacija[uredi | uredi izvor]

Klasa A (Rodopsinoliki)
Klasa B (Sekretinoliki),
Klasa C (Glutamat receptoroliki),
Ostali: Adezijski (33), Uvojiti (11), Okusni tip-2 (25), neklasificirani (23).[7]
Precizna veličina GPCR superfamilije je nepoznata. Na osnovu kodirajućeg genomski kodirajućih sekvenci proteina, pretpostavljeno je da u njihovoj kontroli učestvuje oko 800 različitih ljudskih gena (ili ≈4% celokupnog protein-kodirajućeg genoma). Iako su prednožene brojne klasifikacifikacije, ova superfamilija se klasično dijeli u tri glavne klase: A, B i C. Između ovih klasa nema značajne aminokiselinske homologije. Daleko najveća među njima je klasa A, koja sačinjava skoro 85% GPCR gena. Od receptora klase A, preko polovine kodira olfaktorne receptore, dok su ligandi preostalih receptora poznat endogeni spojevi ili su klasificirani kao orfan receptori. Uprkos odsustva aminokiselinske homologije između klasa, svi GPCR receptori imaju zajedničku strukturu i mehanizam prenosa signala.[8][9][10]
Na osnovu aminokiselinske homologije i funkcionalne sličnosti, GPCR receptori se mogu svrstati u šest klasa:[11][12][13][14]
- Klasa A (ili 1) (Rodopsinu-slični)
- Klasa B (ili 2) (Sekretinska receptorska familija)
- Klasa C (ili 3) (Metabotropni glutamat/feromon)
- Klasa D (ili 4) (Gljivični feromonski receptori)
- Klasa E (ili 5) (Ciklični AMP receptori)
- Klasa F (ili 6) (Uvojiti/Zaglađeni)
Velika rodopsin A grupa je podeljena u 19 podgrupa (A1-A19).[15] Također je predložen i jedan alternativni klasifikacijski sistem pod imenom GRAFS (glutamat, rodopsin, adhezija, uvojiti/okus, Sekretin).[16]
Ljudski genom kodira skoro 1.000 G protein-spregnutih receptora,[17] od kojih oko 350 detektira hormone, faktora rasta i druge endogene ligande. Približno oko 150 GPCR receptora ljudskog genoma nema poznatu funkciju. Za predviđanje tih odnosa, postoji više bioinformatičkih metoda[18][19] GPCR funkcije, kao i za njihovu klasifikaciju prema aminokiselinskoj sekvenci. Neki od njih koriste pristup pseudo aminokiselinske kompozicije.[20]
Fiziološka uloga[uredi | uredi izvor]
GPCR receptori učestvuju u širokom varijetetu fizioloških procesa. Primeri tih fizioloških uloga su:
- Čulo vida: opsini, za translaciju elektromagnetske radijacije, koriste reakciju fotoizomerizacije u ćelijske signale. Rodopsin, naprimjer, u tu svrhu koristi konverziju 11-cis-retinala u sve-trans-retinal.
- Čulo mirisa: receptori mirisnog epitela (mirisni receptori) vezuju odorante i feromone (vomeronosni receptori).
- Regulacija ponašanja i raspoloženja: receptori u mozgu sisara vežu više različitih neurotransmitera, kao što su serotonin, dopamin, GABA i glutamat.
- Regulacija aktivnosti imunskog sistema i upala: hemokinski receptori vežu ligande koji posreduju međućelijsku komunikaciju između ćelija imunskog sistema; receptori poput histaminskog receptora vežu inflamatorne posrednike i dejstvuju na ciljne ćelijske tipove upalnog odgovora
- Prijenos signala autonomnog nervnog sistema: simpatički i parasimpatički nervni sistemi su regulirani GPCR putevima, koji su odgovorni za kontrolu mnogih automatskih tjelesnih funkcija, kao što su krvni pritisak, srčani puls i procesi varenja.
- Indikacija ćelijske gustine: nova GPCR uloga je u regulaciji ćelijske gustine.
Struktura receptora[uredi | uredi izvor]

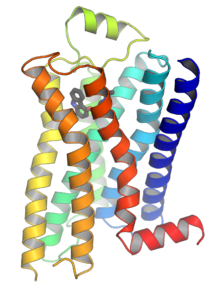
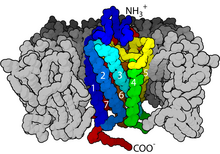
GPCR receptori su integralni membranski proteini koji imaju sedam transmembranskih domena ili transmembranskih heliksa. Vanćelijski dijelovi receptora mogu biti glikozilirani. Te vanćelijke petlje također sadrže dva visokokonzervirana cisteinska ostatka koji formiraju disulfidni most kojim se stabilizira struktura receptora. Neki od sedmotransmembranskih heliksnih proteina (kanalni rodopsin), koji podsjećaju na GPCR receptore, unutar pripadajućih proteina, mogu sadravati ionske kanale. Rani modeli strukture GPCR receptora su bili zasnovani na njihovoj slaboj analogiji sa bakteriorodopsinom, čija struktura je bila utvrđena pomoću elektronske difrakcije (2BRD, 1AT9)[21][22] i Rendgenske strukturne analize (1AP9).[23] U 2000. godini, bila je riješena prva kristalna struktura GPCR receptora sisara, goveđeg rodopsina (1F88).[24] Dok su glavne osobine, sedmoransmembranskih heliksa očuvane, relativna orijentacija heliksa se znatno razlikuje od bakteriorodopsina. U 2007. godini je riješena prva struktura ljudskog GPCR receptora: (2R4R, 2R4S).[25] Ubrzo je slijedilo određivanje strukture visoke rezolucije istog receptora (2RH1).[26][27] Za strukturu ljudskog GPCR β2-adrenergičkog receptora, se ispostavilo da je, u pogledu relativne orijentacije sedam-transmembranskih heliksa, veoma slična goveđem rodopsinu. Međutim, konformacija druge vanćelijske petlje je potpuno drugačija nego ove dvije strukture. Kako ta petlja čini „poklopac“ vrha ligand vezujućeg mjesta, ova konformacijska razlika je dobra ilustracija poteškoća u konstruiranju homolognih modela drugih GPCR receptora, na osnovu strukture rodopsina.
Strukturno-funkcijski odnosi[uredi | uredi izvor]
Struktura GPCR receptora sadrži karakteristični vanćelijski N-kraj, čemu slijedi sedam transmembranskih (7-TM) α-heliksa (TM-1 do TM-7), koji su povezani sa tri unutarćelijske (IL-1 do IL-3) i tri vanćelijske petlje (EL-1 to EL-3), i konačno unutarćelijski C-kraj. GPCR formira tercijarnu strukturu koja podsjeća na bure. Sedmotransmembranski heliks formira šupljinu unutar ćelijske membrane koja služi kao ligand-vezni domen, koji je često prekriven pomoću EL-2. Ligandi također mogu da se vežu na drugim mjestima, kao što je slučaj sa glomaznijim ligandima (npr., proteinima, ili velikim peptidima) koji ragiraju sa vanćelijskim petljama, ili, kao što je slučaj klase C metabotropnih glutamatnih receptora (mGluR), sa domenom N-kraja. GPCR receptori klase C imaju povelik rep N-kraja, sa dobro definisatom tercijarnom strukturom. On sadrži ligand-vezujući domen. Nakon vezanja glutamata za mGluR receptor, N-terminalni rep prolazi kroz konformacijsku promjenu, koja dovodi do njegove interakcije sa ostacima vanćelijskih petlji i TM domenom. Krajnji efekt svih tipova agonist-inducirane aktivacije je promjena relativne orijentacije TM heliksa (praćena uvijajućim kretanjem). To vodi ka povećanjun unutarćelijske površine i otvaranja pristupa dodatnim aminokiselinskim ostacima TM domena, koji su bitni za funkciju prijenosa signala (npr. za interakciju sa G-proteom). Inverzni agonisti i antagonisti se mogu vezati na istom i nekoliko drugih mesta. Njihov efekat je sprečavanje stabilizacije TM heliksne orijentacije, koja je podesna za prijenos signala.
Struktura N- i C-kraja GPCR receptora, pored vezanja liganda, može imati i druge važne funkcije. Specifično, C-kraj često sadrži serin (Ser) ili treonin (Thr) ostatke koji nakon fosforilacije, povećavaju afinitet intracelularne površine za vezanje skeletalnih proteina, poznatih kao β-arestini (β-arr). Jednom vezani, β-arestini sterno sprečavaju formiranje G-proteinske sprege, i mogu uključiti druge proteine, što dovodi do stvaranja signalnih kompleksa, koji učestvuju u aktivaciji ERK signalnog puta ili receptorske endocitoze (internalizacije). Pošto se fosforilacija tih Ser i Thr ostataka često javlja usljed GPCR aktivacije, β-arr-posredovano G-protein-razdvajanje i internalizacija GPCR receptora su značajni mehanizmi smanjenja senzitivnosti (desenzitizacije).[28]
Zajednički strukturni motiv GPCR receptora je i palmitoilacija jednog ili više mesta C-krajeva ili unutarćelijskih petlji. Palmitoilacija je kovalentna modifikacija cisteinskih (Cys) ostataka, putem dodavanja hidrofobnih acil grupa. Ona ima efekte usmjeravanja receptora ka holesterolom i sfingolipidom bogatim mikrodomenima plazma membrane koji se nazivaju lipidni splavovi. Pošto su mnogi nizvodnr transduktorske i efektorske molekule GPCR receptora (u šta se uvrštavaju i oni koji učestvuju u negativnim povratnim signalnim putevima) također usmjereni ka lipidnim splavovima, neto efekt palmitoilacije je veoma brza receptorska signalizacija.
GPCR receptori odgovaraju na vanćelijske signale koji su posredovani velikim brojem različitih agonista, od proteina do biogenih amina i protona. Svi oni prenose signal putem mehanizma G-proteinske sprege. To omogućava faktor razmjene guanin-nukleotida (GEF) – domen koji je formiran kombinacijom unutarćelijskih petlji IL-2, IL-3 i obližnjih aminokiselinskih ostataka TM heliksa.
Mehanizam[uredi | uredi izvor]
G protein-spregnuti receptor se aktivira spoljašnjim signalom u vidu liganda ili nekog drugog signalnog posrednika. To uzrokuje konformacijsku promjenu receptora, pa dolazi do aktivacije G-proteina. Dalji efekt zavisi od tipa G-proteina.
Vezanje liganda[uredi | uredi izvor]
GPCR receptori obuhvataju prijemnike senzornih signalnih posrednika (npr., svjetlo i mirisne stimulatorne molekule); adenozin, bombezin, bradikinin, endotelin, γ-aminobuterna kiselina (GABA), faktor rasta hepatocita (HGF), melanokortini, neuropeptid Y, opioid peptidi, opsini, somatostatin, tahikinini, članovi familije vazoaktivnih intestinalnih peptida i vazopresin, biogeni amini (npr., dopamin, epinefrin, norepinefrin, histamin, glutamat (metabotropni efekat), glukagon, acetilholin (muskarinski efekt), i serotonin); hemokini; lipidni medijatori upale (npr., prostaglandini, prostanoidi, trombocit-aktivirajući faktor, i leukotrieni) i peptidni hormoni (npr., kalcitonin, C5a anafilatoksin, folikul-stimulirajući hormone (FSH), gonadotropin-oslobađajuće hormone (GnRH), neurokinin, tireotropin-oslobađajuće hormone (TRH), i oksitocin). GPCR receptori reagiraju na stimulanse koji još nisu bili identificirani, poznati su kao orfan receptori.
Dok se kod drugih receptorskih tipova ligandi uglavnom vežu sa vanjske strane membrane, GPCR ligandi se većinom vežu unutar transmembranskog domena. Specijalni slučaj su proteazom-aktivirani receptori, koje aktivira odsjecanje dijela njihovog vanćelijskog domena.[29]
Konformacijske promjene[uredi | uredi izvor]
Transdukcija signala kroz membranu, preko receptora, nije potpuno razjašnjena. Poznato je da je neaktivni G-protein vezan za receptor u njegovom neaktivnom stanju. Nakon vezanja liganda, receptor mijenja konformaciju i tako mehanički aktivira G protein, koji se odvaja od receptora. Zatim receptor može ili da aktivira još jedan G protein, ili da se vrati u neaktivno stanje. Iako je ovo objašnjenje suviše pojednostavljeno, ono dovoljno ilustrira sveukupni set akcija. Smatra se da je molekula receptora u konformacijskoj ravnoteži između aktivnih i neaktivnih biofizičkih stanja.[30] Vezanje liganda za receptor može ravnotežu pomjeriti ka aktivnom stanju receptora.[31] Postoje tri tipa liganda:
- Agonisti su ligandi koji pomeraju ravnotežu u korist aktivnih stanja;
- inverzni agonisti su ligandi koji pomeraju ekvilibrijum u korist neaktivnih stanja; i *neutralni antagonisti su ligandi koji ne utiču na ekvilibrij. Još uvijek nije poznato kako se tačno međusobno razlikuju aktivna i neaktivna stanja.
G-proteinski ciklus aktivacije/deaktivacije[uredi | uredi izvor]
Kada je receptor neaktivan, GEF domen može biti vezan za jednu također neaktivnu α-podjedinicu heterotrimernog G-proteina. G-proteini su trimeri α, β i γ podjedinica (poznatih kao Gα, Gβ i Gγ) koje su neaktivne ako su povratno vezane za Guanozin-difosfat (GDP) (ili alternativno, bez guaninskog nukleotida). One su aktivne kada su vezane za Guanozin-trifosfat (GTP). Nakon aktivacije receptora, GEF domen alosterno aktivira G-protein, putem razmjene molekula GDP za GTP na G-protein α-podjedinici. Ćelije održavaju odnos 10:1 citosolnog GTP:GDP, tako da je obezbijeđena razmjena za GTP. Podjedinice G-proteina se postepeno odvajaju od receptora, kao i međusobno, da bi proizvele Gα-GTP monomer, čvrsto interagujući Gβγ dimere, koji su tada slobodni za moduliranje aktivnosti drugih intracelularnih proteina. Do kog stupnja može da dođe do njihove difuzije, međutim, je ograničeno Gα palmitoilacijom i prisustvom glikozil-fosfatidilinozitol (GPI) molekula kovalentno dodatih na Gγ C-kraju. Fosfatidilinozitolni dio GPI molekula sadrži dvije hidrofobne acil grupe koje učvršćuju GPI-vezane proteine (npr. Gβγ) za membranu plazme, i isto tako u određenoj meri, za lokalni lipidni splav. (Uporediti sa uticajem palmitoilacije na GPCR lokalizaciju, što je gore raspravljano).
Budući da Gα takođe ima sposobnost spore GTP→GDP hidrolize, neaktivna forma α-podjedinice (Gα-GDP) se vremenom regenerira, čime se omogućava reasocijacija sa Gβγ dimerom i formiranje “odmarajućeg” G-proteina, koji se ponovo može vezati za GPCR i čeka na aktivaciju. Brzina GTP hidrolize je često povećana akcijama jedne druge familije alosterno moduliranih proteina, zvanih regulatori G-protein signalizacije ili RGS proteini. Oni su tip aktivirajućeg proteina GTPaze ili GAP. Poznato je da mnogi od primarnih efektorskih proteina (npr. adenilat ciklaze), koji postaju aktivirani/deaktivirani nakon interakcije sa Gα-GTP, također imaju akti vnost GAP-a. Na taj način, čak i u ovoj ranoj fazi procesa, GPCR-inicirana signalizacija je sposobna za samo-okončanje.
GPCR signalizacija[uredi | uredi izvor]
Ako aktivni receptor dođe u kontakt sa G-proteinom, on ga može aktivirati. Postoje dokazi da su receptori i G proteini zapravo pre-spregnuti. Naprimjer, vezanje G proteina za receptore ima uticaj na afinitet receptora za ligande. Aktivirani G proteini su vezani za GTP.
Dalji prijenos signala ovisti o tipu G proteina. Enzim adenilat-ciklaza je primjer ćelijskog proteina koji može biti reguliran G proteinom, u ovom slučaju G proteinom Gs. Adenilat ciklaza je aktivirana onda kada se veže za podjedinicu aktiviranog G proteina. Aktivacija adenilat ciklaze se završava kad se G protein vrati u GDP-vezano stanje.
Adenilat ciklaze, od kojih je kod ljudi poznato 9 formi koje su vezane za membranu i jedna citosolna forma, mogu također biti aktivirane ili inhibirane na druge načine, naprimjer putem vezivanja Ca2+/kalmodulina. Ovo može promijeniti aktivnost tih enzima na aditivan ili sinergistički način, uporedo sa G proteinima.
GPCR aktivirani signalni putevi su ograničeni primarnom sekvencom i tercijarnom strukturom GPCR receptora. Nezamjenljivo su određene specifičnom konformacijom koja je stabilizirana datim ligandom, kao i dostupnošću transduktorskih molekula. Smatra se da GPCR receptori koriste dva primarna tipa transduktora: G-proteine i β-arestine. Pošto β-arestini imaju visok afinitet za fosforiliranu formu većine GPCR receptora, najveći dio prenosa signala je nezaobilazno zavisan od G-proteinske aktivacije. Međutim, tu nema G-protein nezavisnog prijenosa signala, jer uvijek postoji mogućnost odvijanja oba tipa interakcija.
Signalizacija zavisna od G proteina[uredi | uredi izvor]
Postoje tri glavna G-proteinom posredovana signalna puta. Oni zavise od četiri potklase G-proteina, koje se međusobno razlikuju po homologiji sekvence (Gαs, Gαi/o, Gαq/11, i Gα12/13). Svaka potklasa G-proteina se sastoji od više proteina, od kojih je svaki pritom produkt više gena i/ili alternativne varijacije prerade RNK, što može da proizvede razlike koje se kreću od suptilnih do očiglednih signalnih osobina, iako su općenito dosta dobro grupirane u okviru četiri klase. Pošto su svojstva prijenosa signala raznih mogućih βγ kombinacija međusobno slična, te klase su definirane na temelju izoforme njihove α-podjedinice.[6]:1163
Dok većina GPCR receptora može aktivirati više od jednog Gα-podtipa, oni imaju sklonost za jedan od podtipova. Kad je aktivirani podtip zavisan od liganda koji je vezan za GPCR, to se naziva funkcijska selektivnost (koja je također poznata i kao agonist-usmjerena razmjena ili konformacijsko specifični agonizam). Međutim, vezanje bilo kojeg pojedinačnog agonista može također inicirati aktivaciju više različitih G-proteina, ako on ima sposobnost stabilizacije više konformacija GPCR GEF domena, čak i u toku jedne interakcije. Pored toga, konformacija koja prvenstveno aktivira jednu Gα izoformu može aktivirati neku drugu izoformu, ako je preferirani protein manje dostupan. Pored toga, putevi povratne sprege mogu rezultirati i u posttranslacijskim modifikacijama receptora (npr. fosforilacijama), koje mijenjaju G-proteinske sklonosti. Pored svih tih nijansi, uobičajeni GPCR parter je obično definiran na temelju G-proteina, koji je najočevidnije aktiviran endogenim ligandom pod fiziološkim i/ili eksperimentalnim uvjetima.
Gα signalizacija[uredi | uredi izvor]
- Efektor Gαs i Gαi/o puteva je ciklični adenozin monofosfat (cAMP) generirajući enzim adenilat ciklaza ili AC. Kod sisara, postoji deset različitih AC genskih produkata, od kojih je svaki suptilno specifičan po tkivnoj distribuciji i/ili funkciji. Svi oni kataliziraju pretvaranje citosolnog adenozin trifosfata (ATP) u cAMP i svi su direktno stimulirani G-proteinima Gαs klase. U kontrastu s tim, interakcija sa Gα podjedinicama tipa Gαi/o , inhibira gewneriranje AC cAMP. Na taj način, GPCR receptori spregnuti sa Gαs neutraliziraju akcije receptora spregnutih sa Gαi/o i obratno. Razina citozolnog cAMP može uvjetovati aktivnost raznih cikličnim nukleotidima-kontroliranih ionskih kanala, kao i članova porodice serin/treonin-specifične proteinske kinaze|Ser/Thr- specifičnih proteinska kinaza A (PKA). Zato se cAMP smatra sekundarnim glasnikom, a PKA sekundarnim efektorom.
- Efektor Gαq/11 puta fosfolipaza C-β (PLCβ), koja katalizira rascijep membranski vezanog fosfatidilinozitol 4,5-bifosfata (PIP2) u sekundarne glasnike inozitol (1,4,5) trifosfat (IP3) i diacilglicerol (DAG). IP3 djeluje na IP3 receptore koji su na membrani endoplazmatskog retikuluma (ER) i pobuđuje oslobađanje Ca2+ iz ER, dok DAG difundira duž plazma membrane gdje može aktivirati bilo koju formu sekundarne Ser/Thr kinaze lokalizirane na membrani, tzv. proteinske kinaze C (PKC). Pošto su mnoge izoforme PKC također aktivirane povećanim razinama unutarćelijskog Ca2+, ova dva puta mogu međusobno konvergirati i prenijeti u signal preko istog sekundarnog efektora. Povišeni unutarćelijski Ca2+ se također veže i alosterno aktivira kalmodulinske proteine, koji, nakon toga, vežu i alosterno aktiviraju enzime kao što su Ca2+/kalmodulin-zavisne kinaze (CAMK).
- Efektori Gα12/13 puta su tri RoGEF proteina (p115-RoGEF, PDZ-RoGEF, i LARG), koji kad su vezani za Gα12/13 alosterno aktiviraju citosolnu malu GTPazu, Ro. Jednom vezana za GTP, Ro može aktivirati razne proteine koji su odgovorni za regulaciju citoskeleta, kao što je Ro-kinaze (ROCK). Većina GPCR receptora koji su spregnuti sa Gα12/13 također mogu formirati sprege i sa drugim potklasama, često sa Gαq/11.
Signalizacija Gβγ[uredi | uredi izvor]
Gornji opis ne uzima u obzir efekte Gβγ–signalizacije, koji su također značajni, osobito u slučaju aktiviranog Gαi/o-spregnutog GPCR receptora. Primarni Gβγ efektori su razni ionski kanali, kao što su G-protein-spregnuti unutrašnje-ispravljajući K+ kanali (GIRK), P/Q-, i N-tip naponski ovisni Ca2+ kanali, kao i neke AC i PLC izoforme, zajedno sa pojedinim izoformama fosfoinozitid-3-kinaze (PI3K).
Signalizacija nezavisna od G-proteina[uredi | uredi izvor]
Iako se za G receptore misli da oni mogu djelovati samo zajedno sa G proteinima, GPCR receptori mogu prenositi signale i putem mehanizama koji su nezavisniod G-proteina. Heterotrimerni G proteini isto tako imaju funkcijske uloge koje su nezavisne od GPCR receptora. GPCR receptori mogu samostalno prenositi signal, posredstvom više tipova proteina, kao što su β-arestin, GRK i Src. Osim toga, dodatni skeletni proteini, koji učestvuju u GPCR subćelijskoj lokalizaciji (npr. PDZ-domen sadržavajući proteini) mogu također djelovti u prijenosu signala. Efektori su najčešće članovi porodice MAPK.
Primjeri[uredi | uredi izvor]
Kasnih 1990. godina, počeli su se akumulirati dokazi da neki GPCR receptori mogu prenositi signala i bez G proteina. Za ERK2 mitogenom aktivirane proteinske kinaze, koje su ključni posrednici prijenosa signala nizvodno od receptorske aktivacije u mnogim putevima, bilo je pokazano da se aktiviraju u odgovoru na cAMP posredovanu aktivaciju receptora kod plijesni iz mulja (Dictyostelium discoideum), unatoć odsustvu spregnutih G proteinskih α- i β-podjedinica.[32] U ćelijama sisara, za široko proučavani β2-adreno receptor je demonstrirano da aktivira ERK2 put nakon arestinom posredovanog raskida sprege signalizacije koja je posredovana G-proteinom. Na osnovu toga je zaključeno da su neki od mehanizama za koje se ranije vjerovalo da su isključivo vezani za smanjenje osjetljivosti receptora, zapravo primjeri promjene receptorskih puteva, a ne njihovog isključivanja.
U ćelijama bubrega, za bradikinin receptor B2 je pokazano da ragira direktno sa proteinskom tirozinskom fosfatazom. Prisustvo tirozin-fosforilisane ITIM (imunoreceptor tirozin-baziranog inhibitornog motiva) sekvence u B2 receptoru je neophodno za njegovo posredovanje te interakcije i naknadno antiproliferativno djejstvo bradikinina.[33]
Nezavisna signalizacija od GPCR[uredi | uredi izvor]
Iako je ovo relativno nerazvijena oblast, postoje naznake da heterotrimerni G-proteini mogu učestvovati u GPCR-nezavisnom prijenosu signala. Postoje dokazi o njihovoj ulozi uprenosu signala kod skoro svih drugih tipova receptorski posredovane signalizacije, kao što su integrin, receptorske tirozinske kinaze (RTK), citokinskih receptora (JAK/STAT), kao i za modulaciju raznih drugih „pomoćnih“ proteina kao što su GEF, inhibitor disocijacije guanozin nukleotida (GDI) i proteinske fosfataze. Moguće je da postoje i specifični proteini iz ove klase čija je primarna funkcija u okviru GPCR-nezavisnih puteva.
Putevi cAMP i PIP2[uredi | uredi izvor]



Opisana su dva glavna načina prijenosa signala u kojima učestvuju G protein spregnuti receptori: cAMP signalni put i fosfatidilinozitolni signalni put.[5]
Signalni put cAMP-a[uredi | uredi izvor]
Signalni put cAMP sse sastoji od pet glavnih komponenti:
- stimulativni hormonski receptor (Rs) ili inhibitorni hormonski receptor (Ri);
- stimulativni regulirajući G protein (Gs) ili inhibitorni regulacijski G protein (Gi)
- Adenilil ciklaza
- Proteinska-kinaza A (PKA)
- cAMP fosfodiesteraza.
Stimulativni hormonski receptor (Rs) veže stimulativne signalne molekule, dok inhibitorni hormonski receptor (Ri) veže inhibitorne signalne molekule. Stimulativni regulirajući G-protein formira interakcije sa stimulativnim hormonskim receptorom, a njegove podjedinice, nakon aktivacije, mogu stimulirati aktivnost enzima ili drugi unutarćelijski metabolizam. Nasuprot tome, inhibitorni regulatorni G protein čini spregu sa inhibitornim hormonskim receptorom, a njegova α podjedinica, nakon aktivacije, može inhibirati aktivnost enzima ili drugi unutaćelijski metabolizam.
Adenilil-ciklaza je glukoprotein sa 12 transmembranskih heliksa. Ona katalizira prijelaz ATP-a u cAMP, uz pomoć kofaktora Mg2+ ili Mn2+. Nastali cAMP je sekundarni glasnik u ćelijskom metabolizmu i alosterni aktivator proteinske kinaze A.
Proteinska kinaza A je važan enzim ćelijskog metabolizma. Ima sposobnost regulacije ćelijskog metabolizma putem fosforilacije specifičnih namjenskih enzima u metaboličkom putu. Takođe može regulirati ispoljavanje specifičnih gena, ćelijsku sekreciju i membransku propustljivost. Ovaj enzim sadrži po dvije katalitske i regulacijske podjedinice. Kompleks je neaktivan u odsustvu cAMP-a, a kada se on veže za regulacijske podjedinice, mijenja se njihova konformacija i dolazi do disocijacije regulatornih podjedinica. Time se aktivira proteinska kinaza A i omogućavaju dalji biološki efekti. cAMP-fosfodiesteraza je enzim koji može da razgradi cAMP do 5'-AMP-a, čime se signal okončava.
Fosfatidilinozitolni signalni put[uredi | uredi izvor]
U signalnom putu fosfatidilinozitola, vanćelijska signalna molekula se veže za G protein spregnuti receptor (Gq) na ćelijskoj površini i aktivira fosfolipazu C, koja je smještena na ćelijskoj membrani. Lipaza hidrolizira fosfatidilinozitol 4,5-bisfosfat (PIP2) u dva sekundarna glasnika: inozitol 1,4,5-trisfosfat (IP3) i diacilglicerol (DAG). IP3 se veže za receptor u membrani glatkog endoplazmatskog retikuluma i mitohondrija, čime pomaže otvaranje Ca2+ kanala. DAG pomaže aktivaciju proteinske kinaze C (PKC), koja fosforilizira mnoge druge proteine, mijenjajući time njihove katalitske aktivnosti, što dovodi do ćelijskog odgovora. Također je značajno i djelovanje Ca2+ iona. Oni zajedno sa DAG-om aktiviraju PKC i mogu da dovedu do aktivacije CaM kinaznog puta, u kojem kalcijem modulirani protein kalmodulin (CaM) veže Ca2+, podliježući promeni konformacije, a aktivira CaM kinazu II. Ona ima jedinstvenu sposobnost povećanja svog afiniteta vezanja za CaM putem autofosforilacije, što CaM čini nedostupnim za aktivaciju drugih enzima. Kinaza zatim fosforilizira ciljne enzime, čime regulira njihove aktivnosti. Ova dva signalna puta povezuje Ca2+-CaM, koji je također regulacijska podjedinica adenilil ciklaze i fosfodiesteraze u cAMP signalnom putu.
Regulacija receptora[uredi | uredi izvor]
Receptori koji su spregnuti sa G proteinom, spodložni su desenzitaciji, ako su dugotrajno izloženi njihovom ligandu. Poznate su dvije forme desenzitizacije:
- homologna desenzitizacija, pri kojoj aktivirani GPCR proizvodi sanjeni odgovor, i
- heterologna desenzitizacija, kada aktivirani GPCR uzrokuje umanjenje odgovora drugih receptora.
Ključna reakcija ovog procesa je fosforilacija unutarćelijskog (ili citosolnog) receptorskog domena proteinskim kinazama.
Fosforilacija cAMP zavisnom proteinskom kinazom[uredi | uredi izvor]
Proteinske kinaze A (od cikličnog AMP-a zavisne proteinske kinaze) se aktiviraju signalnim lancom koji počinje od aktiviranog G proteina, uz posredovanje adenilat ciklaze i cikličnog AMP-a (cAMP-a). U mehanizmu povratne sprege, ove kinaze, nakon aktivacije, fosforiliziraju receptor. Što duže receptor ostaje aktivan, to se aktiviraju više kinaze, pa je utoliko više fosforiliziranih receptora. Kod β2-adrenoceptora, ta fosforilacija izaziva promjeni sprege, od Gs klase G-proteina do Gi klase.[34] PKA posredovana fosforilacija može izazvati heterologno smanjenje osjetljivosti receptora.[35]
Fosforilacija posredstvom GRK kinaza[uredi | uredi izvor]
Kinaze G protein spregnutih receptora (GRK) su proteinske kinaze koje fosforiliziraju GPCR receptore.
Fosforilacija receptora može izazvati dvije posljedice:
- Translokacija: Receptor se, zajedno sa dijelom membrane u kojoj je lociran, unosi u unutrašnjost ćelije, gdje se defosforilizira u kiselom okruženju vezikula,[36] a zatim se vraća u membranu. Ovaj mehanizam se koristi za regulaciju dugotrajnog izlaganja, na primjer hormonima. Alternativno, receptor može biti podvrgnut lizosomnoj degradaciji ili ostati internaliziran, kada se smatra da učestvuje u inicijaciji signalizacije, čija je priroda zavisna od lokalizacije internalizirane vezikule.[35]
- Vezanje arestina: Fosforilizirani receptor se može vezati za molekule arestina, čime se sprečava vezanje za G proteine, pa se efektivno isključuje tokom nekog perioda. Tom mehanizmu se podvrgava naprimjer rodopsin u ćelijama mrežnjače tokom kompenzacije za izlaganje jakom svjetlu. U mnogim slučajevima, vezanje arestina za receptor je preduvjet za premještanje. Naprimjer, beta-arestin koji je vezan za β2-adrenoreceptore, djeluje kao adapter vezanja klatrina i sa beta-podjedinicom AP2 (klatrin adapterskog molekula). Tako arestin ovdje djeluje kao osnova za montažu komponenti potrebnih za klatrinski posredovanu endocitozu β2-adrenoreceptora.[37][38]
Mehanizmi terminacije GPCR signala[uredi | uredi izvor]
Kao što je gore razrađeno, G-proteini mogu prekinuti sopstvenu aktivaciju posredstvom njihovog unutrašnjeg GTP→GDP hidroliznog djejstva. Međutim, ta reakcija teče malom brzinom (≈0,02 puta/sekundi), tako da je bez drugih faktora potrebno oko 50 sekundi da se jedan G-protein deaktivira. Postoji oko 30 izoformi RGS proteina, koj u vezi sa Gα, putem njihovog GAP domena, ubrzavaju hidrolizu na oko ≈30 puta/sekundi. Ovo povećanje brzine od oko 1.500 puta, omogućava ćeliji brzi odgovor na spoljašnje signale i proizvodi prostornu rezoluciju usljed ograničene količine sekundarnog glasnika koja se može generirati, kao i ograničenog rastojanja, na koje se G-protein može pomjeriti raspršavanjem tokom 0,03 sekunde. RGS proteini su uglavnom nespecifični u njihovoj sposobnosti da aktiviraju G proteine. Izbor RGS proteina koji učestvuje u datom signalnom putu prvenstveno zavisi od tipa tkiva i GPCR receptora. RGS proteini imaju dodatnu funkciju u povećanju brzine razmjene GTP-GDP na GPCR receptorima. Prema tome, oni djeluju poput GEF-a, čime dodatno doprinose povećanju rezolucije GPCR signalizacije.
GPCR receptori također mogu proizvediti homolognu desenzitizaciju. Do toga može doći na slijedeće načine:
- direktan rezultat dejstva liganda, kada promjena konformacije omogućava uključivanje GRK kinaza koje fosforilišu razne serinske/treoninske ostatke na IL-3 i repu C-kraja. Nakon fosforilacije GRK, afinitet GPCR receptora za β-arestin (β-arestin-1/2 u većini tkiva) se povećava. Vezanje β-arestina može sterno onemogućiti spregu G-proteina. Oni isto tako mogu inicirati proces internalizacije receptora putem klatrinom posredovane endocitoze. Do smanjenja osjetljivosti receptora na ovaj način može doći samo u prisustvu liganda, pa se ona naziva homolognom desenzitizacijom[28]
- afinitet za β-arestin se može povećati nezavisno od izlaganja ligandu i posredovanja GRK. Do toga dolazi pomoću fosforilacije različitih Ser/Thr mjesta (također na IL-3 i repu C-kraja) djejstvom PKC i PKA. Te fosforilacije su često dovoljne da spriječe formiranje sprege sa G-proteinima.
- PKC/PKA mogu fosforilirati GRK kinaze, što može izazvati dalju fosforilaciju GPCR receptora i vezanje β arestina. Taj proces je nezavisan od koncentracije liganda. Ova dva zadnja mehanizma omogućavaju slabljenje osjetljivosti GPCR receptora, pod uticajem drugih receptora (heterologna desenzitizacija). GRK kinize također mogu sadržavati GAP domene i tako doprinijeti inaktivaciji, mehanizmom koji je nezavisan od kinaza. Pojavljuju se i kombinacije ovih mehanizama.
Nakon vezivanja β-arestina za GPCR, on podliježe konformacijskoj promjeni koja mu omogućava da bude osnovni protein adapterskog kompleksa pod nazivom AP-2, a koji može da uključiti protein klatrin. Ako dovoljan broj receptora u datoj lokalnoj oblasti, na ovaj način aktivira klatrin, oni formiraju agregate i membrana se deformira ka unutrašnjosti ćelije, što je rezultat interakcije između molekula klatrina u procesu opsonizacije. Kad je udubljenje jednom formirano, ćelijska membrana, pod uticajem dva druga proteina zvana amfifizin i dinamin, formira endocitoznu vezikulu. Zatim se adapterske molekule i klatrin razdvajaju, a receptor se vraća u proteinsku membranu ili se razlaže u lizosomima.[39]
Na bilo kojoj tački ovog procesa, β-arestini mogu uključiti i druge proteine, kao što su nereceptorska tirozinska kinaza (nRTK) i c-SRC, koji mogu pokrenuti aktivaciju ERK1/2 ili drugih mitogenom aktiviranih proteinskih kinaza (MAPK). Ove prenose signal putem, naprimer, fosforilacije malih GTP-aza, Ras ili direktnog uključivanja proteina ERK kaskade (i.e., Raf-1, MEK, ERK-1/2), kada se signalizacija inicira usljed njihove prostorne kolokacije. Još jedna meta c-SRC kinaze su dinaminske molekula koji učestvuju u endocitozi. Dinamini se polimerizuju oko vrata ulazećih vezikula, a njihova fosforilacija c-SRC kinazom daje energiju koja je neophodna za konformacijsku promjenu kojom se ostvaruje finalno odvajanje od membrane.
Ćelijska regulacija GPCR[uredi | uredi izvor]
Smanjenje osjetljivosti receptora je posredovano kombinacijom fosforilacije, vezanja β-arestina i endocitoze. Do umanjenog odgovora dolazi kad se endosom koji sadrži receptor spoji sa lizosomom. Lizosomne membrane su bogate protonskim pumpama, te njihova unutrašnjost ima nizak pH (≈4.8 vs. pH≈7.2 citosola), što izaziva denaturaciju GPCR receptora. Dodatno, lizosomi sadrže mnoge degradativne enzime, uključujući proteaze, koje djeluju samo na takvim niskim pH vrijednostima, tako da može doći do razlaganja peptidnih veza GPCR receptora. Niz faktora uslovljava to da li će receptor biti razložen ili vraćen u membranu. Neki od njih su tip receptora i veličina signala.
GPCR regulacija je dodatno posredovana faktorima transkripcije gena. Ti faktori mogu povećati ili umanjiti ekspresiju gena i tako uvjete za formiranje novih receptora (tzv. povećana ili umanjena regulacija).
Oligomeracija receptora[uredi | uredi izvor]
G protein spregnuti receptori mogu formirati heterodimere kao što su homo- i heterodimeri, te kompleksnije oligomerne strukture. Direktne receptor-receptor interakcije mogu, od neaktivnih monomera, formirati funkcijske receptore. Pokazano je da je heterodimerizacija ključna za funkcioniranje receptora kao što su metabotropni GABA(B) receptori. Uloga oligomerizacija u tome nije dovoljno razjašnjena. Smatra se da taj fenomen na određen način doprinosi farmakološkoj heterogenosti GPCR receptora. Ovaj fenomen se i dalje aktivno istražuje. Eksperimentalno je pokazano da GPCR himere ili skraćeni fragmenti, koji su individualno neaktivni, postaju sposobni za vezanja i signalizacije ako se ispoljavaju u istoj membrani.[40][41] Ovo zapažanje, samo po sebi, ne identificira ulogu oligomerizacije u funkciji GPCR , ali demonstrira da receptor-receptor interakcije mogu uticati na vezanje agonista i interakcije sa G proteinima. Isto tako, može se zaključiti da su međumolekulske interakcije jednako važne kao i unutarmolekulske, koje direktno proizvode aktivaciju receptora.

Nakon publikacije ovih nalaza, izveden je znatan broj studija o GPCR dimerizaciji.[42][43][44][45][46][47][48][49][50][51] Uprkos tome razumevanje funkcionog značaja oligomerizacije je i dalje nepotpuno, a u nekim slučajevima i kontroverzno.[52] Do ovog zaključka takođe su došli Terilon i Bouvier u nedavnom pregledu GPCR dimerizacije.[49] Najbolje ispitani primjeri oligomeranih receptora su metabotropni GABAB receptori. Ovi receptori se formiraju heterodimerizacijom GABABR1 i GABABR2 podjedinica. Izražavanje GABABR1 bez GABABR2 u heterolognim sistemima izaziva zadržavanje te podjedinice u endoplazmatskom retikulumu. Ispoljavanje samo GABABR2 podjedinice, međutim, dovodi do njenog izlaska na površini ćelije, gdje nije funkcionalna (tj. receptor ne veže agonist, pa ne pokreće odgovor nakon izlaganja agonistu). Kad se obje podjedinice ispoljavaju zajedno, funkcijski receptori dospijevaju na ćelijsku površinu. Pokazano je da GABABR2 vezivanje za GABABR1 izaziva maskiranje retencionog signala[53] funkcionalnih receptora.[54][55][56][57]

U ovom slučaju je utvrđeno da se strukturna ponuda nalazi u C-kraju, gde postoji sekvenca sklona formiranju interakcija namotanog kalema.[53] Ovo je u suprotnosti s jednim drugim članom familije GPCR receptora, glutamatnim receptorom tipa 1, gdje se dimerizacija javlja na N-kraju.[58] Njegov veliki domen “muholovke“ je strukturno sličan sa veznim domenom glutamatnih receptorskih kanala, gdje oni formiraju stabilne oligomerne forme.[59] Iako su ovi primjeri specijalni slučajevi, postoje dokazi da se GPCR receptori dimerizuju da bi mogli djelovati kao molekulski pratioci, najčešće da bi katalizirali sopstveno savijanje i transport do ćelijske površine. Dokazi su najdostupniji za familiju A GPCR receptora, npr. V2 vazopresinske receptore[60][61] i hemokinski receptor CCR5.[51][62]
Uloga dimerizacije u GPCR ontogenezi ne isključuje mogućnost da onda kada jednom receptor dosegne ćelijsku površinu, njegovo oligomerno stanje ne može biti dinamički regulirano ligandom. Eksperimenti koji su zasnovani na Fluorescentno-rezonantnom energetskom transferu (FRET) i bioluminescentnom energetskom transferu (BRET) su pokazali da mnogi GPCR receptori postoje kao oligomeri ili su bar u blisko pakovanim klasterima, u membranama živih ćelija.[42][43][44][45][46][47][48][49] Međutim, oni su samo marginalno doprinijeli poboljšanju razumijevanja funkcijske relevantnosti. Pošto većina tih studija pokazuje da vezanje agonista ne proizvodi znatnu promjenu optičkog signala, može se zaključiti da su GPCR receptori konstitucijski dimeri i da se takva supramolekulska organizacija ne sprečava stanjem aktivacije proteina. Iz brojnih FRET i BRET mjerenja proizilazi da nema povećanja udjela, niti do razgradnje dimernog stanja, te da dimeri nisu neohodni za receptorski posredovanu aktivaciju G proteina. Alternativna interpretacija je da nema dokaza koji bi potvrdiliu da dimerni GPCR receptori nisu jednokratne strukture za ostvarivanje produktivne interakcije sa G proteinskim heterotrimerom. Strukturni i biohemijski dokazi sugeriraju da vezivna površina G proteinskog trimera može ući u interakciju sa dimernim GPCR receptorom,[63][64] mada se neka zapažanja mogu interpretirati kao indikacija da citosolni region monomernog GPCR receptora podleže znatnim konformacionim promenama nakon interakcije sa G proteinom.[65] Nedavno je u elegantnim eksperimentima, koji su uključivali kombinacije masene spektrometrije, nakon hemijskog povezivanja i neutronskog rasipanja u rastvoru, nedvosmileno pokazano da je kompleks između prečišćenog, aktiviranog leukotrienskog B4 receptora BLT1 i Giα2β1γ2 pentamerni sklop jednog dimernog receptora i heterotrimernog G proteina.[66]
Porijeklo i diversifikacija superfamilije[uredi | uredi izvor]
Prenos signala koji je posredovan GPCR superfamilijom datira iz razdoblja pojave prvih oblika višećelijskih organizama. Nedavna istraživanja su pokazala da su GPCR receptori, koji slični receptorima sisara prisutni u carstvu gljiva i da se mogu klasificirati na osnovu GRAFS sistema koji počiva na obilježjima GPCR.[67] Identifikacija članova superfamilije širom eukariotskog domena i upoređivanje specifičnih motiva je sugeriralo zaključak da GPCR superfamilija ima zajedničko porijeklo.[68] Na osnovu analize karakterističnih motiva, slijedi da su tri, od pet, GRAFS familija (rodopsinska, adheziona i uvojita), evoluirale iz oblika u kojima je i Dictyostelium discoideum . sa cAMP receptorima, prije razdvajanja [[taksona Opisthoconta. Kasnije je nastala sekretinska familija, iz adhezijske receptorske familije, prije nego što su se odvojili valjkasti crvi (nematode).
Dictyostelium discoideum[uredi | uredi izvor]
Kod organizma Dictyostelium discoideum je nedavno bio identificiran novi GPCR, koji sadrži lipidno kinazni domen. On regulira iskaztivanja ćelijske gustine.[69]
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ King N, Hittinger CT, Carroll SB (2003). "Evolution of key cell signaling and adhesion protein families predates animal origins". Science. 301 (5631): 361–3. doi:10.1126/science.1083853. PMID 12869759.CS1 održavanje: više imena: authors list (link)
- ^ Filmore, David (2004). "It's a GPCR world". Modern Drug Discovery. American Chemical Society. 2004 (November): 24–28.
- ^ Overington JP, Al-Lazikani B, Hopkins AL (2006). "How many drug targets are there?". Nat Rev Drug Discov. 5 (12): 993–6. doi:10.1038/nrd2199. PMID 17139284.CS1 održavanje: više imena: authors list (link)
- ^ Royal Swedish Academy of Sciences (10. 10. 2012). "The Nobel Prize in Chemistry 2012 Robert J. Lefkowitz, Brian K. Kobilka". Pristupljeno 10. 10. 2012.
- ^ a b Gilman A.G. (1987). "G Proteins: Transducers of Receptor-Generated Signals". Annual Review of Biochemistry. 56: 615–649. doi:10.1146/annurev.bi.56.070187.003151. PMID 3113327.
- ^ a b Wettschureck N, Offermanns S (2005). "Mammalian G proteins and their cell type specific functions". Physiol. Rev. 85 (4): 1159–204. doi:10.1152/physrev.00003.2005. PMID 16183910.
- ^ Bjarnadóttir TK, Gloriam DE, Hellstrand SH, Kristiansson H, Fredriksson R, Schiöth HB (septembar 2006). "Comprehensive repertoire and phylogenetic analysis of the G protein-coupled receptors in human and mouse". Genomics. 88 (3): 263–73. doi:10.1016/j.ygeno.2006.04.001. PMID 16753280.CS1 održavanje: upotreba parametra authors (link)
- ^ Alberts B.; et al. (2002). Molecular Biology of the Cell, 4th Ed. Garland Science. ISBN 0-8153-4072-9. Eksplicitna upotreba et al. u:
|author=(pomoć) - ^ Bajrović K, Jevrić-Čaušević A., Hadžiselimović R., Eds. (2005). Uvod u genetičko inženjerstvo i biotehnologiju. Institut za genetičko inženjerstvo i biotehnologiju (INGEB) Sarajevo. ISBN 9958-9344-1-8.CS1 održavanje: više imena: authors list (link)
- ^ Kapur Pojskić L. (2014). Uvod u genetičko inženjerstvo i biotehnologiju, 2. izdanje. Institut za genetičko inženjerstvo i biotehnologiju (INGEB), Sarajevo. ISBN 978-9958-9344-8-3.
- ^ Attwood TK, Findlay JB (1994). "Fingerprinting G-protein-coupled receptors". Protein Eng. 7 (2): 195–203. doi:10.1093/protein/7.2.195. PMID 8170923.
- ^ Kolakowski LF Jr (1994). "GCRDb: a G-protein-coupled receptor database". Receptors Channels. 2 (1): 1–7. PMID 8081729.
- ^ Foord SM, Bonner TI, Neubig RR, Rosser EM, Pin JP, Davenport AP, Spedding M, Harmar AJ (2005). "International Union of Pharmacology. XLVI. G protein-coupled receptor list". Pharmacol Rev. 57 (2): 279–88. doi:10.1124/pr.57.2.5. PMID 15914470.CS1 održavanje: više imena: authors list (link)
- ^ InterPro
- ^ Joost P, Methner A (2002). "Phylogenetic analysis of 277 human G-protein-coupled receptors as a tool for the prediction of orphan receptor ligands". Genome Biol. 3 (11): research0063.1–0063.16. doi:10.1186/gb-2002-3-11-research0063. PMC 133447. PMID 12429062.
- ^ Bjarnadottir TK, Gloriam DE, Hellstrand SH, Kristiansson H, Fredriksson R, Schioth HB (2006). "Comprehensive repertoire and phylogenetic analysis of the G protein-coupled receptors in human and mouse". Genomics. 88 (3): 263–73. doi:10.1016/j.ygeno.2006.04.001. PMID 16753280.CS1 održavanje: više imena: authors list (link)
- ^ Vassilatis DK, Hohmann JG, Zeng H, Li F, Ranchalis JE; et al. (2003). "The G protein-coupled receptor repertoires of human and mouse". Proc Natl Acad Sci USA. 100 (8): 4903–4908. doi:10.1073/pnas.0230374100. PMC 153653. PMID 12679517. Arhivirano s originala, 28. 8. 2020. Pristupljeno 18. 6. 2016. Eksplicitna upotreba et al. u:
|author=(pomoć)CS1 održavanje: više imena: authors list (link) - ^ Qiu JD, Huang JH, Liang RP, Lu XQ (2009). "Prediction of G-protein-coupled receptor classes based on the concept of Chou's pseudo amino acid composition: an approach from discrete wavelet transform". Anal. Biochem. 390 (1): 68–73. doi:10.1016/j.ab.2009.04.009. PMID 19364489.CS1 održavanje: više imena: authors list (link)
- ^ Gu Q, Ding YS, Zhang TL (2010). "Prediction of G-Protein-Coupled Receptor Classes in Low Homology Using Chou's pseudo amino acid composition with Approximate Entropy and Hydrophobicity Patterns". Protein Pept. Lett. 17 (5): 559–67. doi:10.2174/092986610791112693. PMID 19594431.CS1 održavanje: više imena: authors list (link)
- ^ Xuan Xiao, Pu Wang, Kuo-Chen Chou (2009). "GPCR-CA: A cellular automaton image approach for predicting G-protein-spregnuti receptor functional classes". Journal of Computational Chemistry. 30: 1414–1423.CS1 održavanje: više imena: authors list (link)[mrtav link]
- ^ Grigorieff N, Ceska TA, Downing KH, Baldwin JM, Henderson R (1996). "Electron-crystallographic refinement of the structure of bacteriorhodopsin". J. Mol. Biol. 259 (3): 393–421. doi:10.1006/jmbi.1996.0328. PMID 8676377.CS1 održavanje: više imena: authors list (link)
- ^ Kimura Y, Vassylyev DG, Miyazawa A, Kidera A, Matsushima M, Mitsuoka K, Murata K, Hirai T, Fujiyoshi Y (1997). "Surface of bacteriorhodopsin revealed by high-resolution electron crystallography". Nature. 389 (6647): 206–11. doi:10.1038/38323. PMID 9296502.CS1 održavanje: više imena: authors list (link)
- ^ Pebay-Peyroula E, Rummel G, Rosenbusch JP, Landau EM (1997). "X-ray structure of bacteriorhodopsin at 2.5 angstroms from microcrystals grown in lipidic cubic phases". Science. 277 (5332): 1676–81. doi:10.1126/science.277.5332.1676. PMID 9287223.CS1 održavanje: više imena: authors list (link)
- ^ Palczewski K, Kumasaka T, Hori T, Behnke CA, Motoshima H, Fox BA, Trong IL, Teller DC, Okada T, Stenkamp RE, Yamamoto M, Miyano M (2000). "Crystal structure of rhodopsin: A G protein-coupled receptor". Science. 289 (5480): 739–45. doi:10.1126/science.289.5480.739. PMID 10926528.CS1 održavanje: više imena: authors list (link)
- ^ Rasmussen SG, Choi HJ, Rosenbaum DM, Kobilka TS, Thian FS, Edwards PC, Burghammer M, Ratnala VR, Sanishvili R, Fischetti RF, Schertler GF, Weis WI, Kobilka BK (2007). "Crystal structure of the human β2-adrenergic G-protein-coupled receptor". Nature. 450 (7168): 383–7. doi:10.1038/nature06325. PMID 17952055.CS1 održavanje: više imena: authors list (link)
- ^ Cherezov V, Rosenbaum DM, Hanson MA, Rasmussen SG, Thian FS, Kobilka TS, Choi HJ, Kuhn P, Weis WI, Kobilka BK, Stevens RC (2007). "High-resolution crystal structure of an engineered human β2-adrenergic G protein-coupled receptor". Science. 318 (5854): 1258–65. doi:10.1126/science.1150577. PMC 2583103. PMID 17962520.CS1 održavanje: više imena: authors list (link)
- ^ Rosenbaum DM, Cherezov V, Hanson MA, Rasmussen SG, Thian FS, Kobilka TS, Choi HJ, Yao XJ, Weis WI, Stevens RC, Kobilka BK (2007). "GPCR engineering yields high-resolution structural insights into β2-adrenergic receptor function". Science. 318 (5854): 1266–73. doi:10.1126/science.1150609. PMID 17962519.CS1 održavanje: više imena: authors list (link)
- ^ a b Luttrell LM, Lefkowitz RJ (2002). "The role of beta-arrestins in the termination and transduction of G-protein-coupled receptor signals". J. Cell. Sci. 115 (Pt 3): 455–65. PMID 11861753.
- ^ Brass LF (2003). "Thrombin and platelet activation". Chest. 124 (3 Suppl): 18S–25S. doi:10.1378/chest.124.3_suppl.18S. PMID 12970120.
- ^ Rubenstein, Lester A. and Lanzara, Richard G. (1998). "Activation of G protein-coupled receptors entails cysteine modulation of agonist binding". Journal of Molecular Structure (Theochem). 430: 57–71. doi:10.1016/S0166-1280(98)90217-2.CS1 održavanje: više imena: authors list (link)
- ^ "The biophysical basis for the graphical representations".
- ^ Kim JY, Haastert PV, Devreotes PN (1996). "Social senses: G-protein-coupled receptor signaling pathways in Dictyostelium discoideum". Chem. Biol. 3 (4): 239–43. PMID 8807851.CS1 održavanje: više imena: authors list (link)
- ^ Duchene J, Schanstra JP, Pecher C, Pizard A, Susini C, Esteve JP, Bascands JL, Girolami JP (2002). "A novel protein-protein interaction between a G protein-coupled receptor and the phosphatase SHP-2 is involved in bradykinin-induced inhibition of cell proliferation". J Biol Chem. 277 (43): 40375–83. doi:10.1074/jbc.M202744200. PMID 12177051.CS1 održavanje: više imena: authors list (link)
- ^ Chen-Izu Y, Xiao RP, Izu LT, Cheng H, Kuschel M, Spurgeon H, Lakatta EG (2000). "G(i)-dependent localization of beta(2)-adrenergic receptor signaling to L-type Ca(2+) channels". Biophys. J. 79 (5): 2547–56. doi:10.1016/S0006-3495(00)76495-2. PMC 1301137. PMID 11053129.CS1 održavanje: više imena: authors list (link)
- ^ a b Tan CM, Brady AE, Nickols HH, Wang Q, Limbird LE (2004). "Membrane trafficking of G protein-coupled receptors". Annu. Rev. Pharmacol. Toxicol. 44: 559–609. doi:10.1146/annurev.pharmtox.44.101802.121558. PMID 14744258.CS1 održavanje: više imena: authors list (link)
- ^ Krueger KM, Daaka Y, Pitcher JA, Lefkowitz RJ (1997). "The role of sequestration in G protein-coupled receptor resensitization. Regulation of β2-adrenergic receptor dephosphorylation by vesicular acidification". J. Biol. Chem. 272 (1): 5–8. doi:10.1074/jbc.272.1.5. PMID 8995214.CS1 održavanje: više imena: authors list (link)
- ^ Laporte SA, Oakley RH, Holt JA, Barak LS, Caron MG (2000). "The interaction of β-arrestin with the AP-2 adaptor is required for the clustering of β2-adrenergic receptor into clathrin-coated pits". J. Biol. Chem. 275 (30): 23120–6. doi:10.1074/jbc.M002581200. PMID 10770944.CS1 održavanje: više imena: authors list (link)
- ^ Laporte SA, Oakley RH, Zhang J, Holt JA, Ferguson SS, Caron MG, Barak LS (1999). "The beta2-adrenergic receptor/betaarrestin complex recruits the clathrin adaptor AP-2 during endocytosis". Proc. Natl. Acad. Sci. U.S.A. 96 (7): 3712–7. doi:10.1073/pnas.96.7.3712. PMC 22359. PMID 10097102.CS1 održavanje: više imena: authors list (link)
- ^ Breann L. Wolfe, JoAnn Trejo (2007). "Clathrin-Dependent Mechanisms of G Protein-coupled Receptor Endocytosis". 8 (5): 462–470. doi:10.1111/j.1600-0854.2007.00551.x. journal zahtijeva
|journal=(pomoć) - ^ Maggio, R.; Vogel, Z.; Wess, J. (1993). "Coexpression studies with mutant muscarinic/adrenergic receptors provide evidence for intermolecular "cross-talk" between G-protein-linked receptors" (PDF). Proc. Natl. Acad. Sci. U.S.A. 90: 3103. Arhivirano s originala (PDF), 24. 9. 2015. Pristupljeno 18. 6. 2016.CS1 održavanje: više imena: authors list (link)
- ^ Maggio, R.; Barbier, P.; Fornai, F.; Corsini, G. U. (1996). "Functional role of the third cytoplasmic loop in muscarinic receptor dimerization". J. Biol. Chem. 271: 31055.CS1 održavanje: više imena: authors list (link)
- ^ a b Bouvier, M. (2001). "Oligomerization of G-protein-coupled transmitter receptors". Nat. Rev. Neurosci. 2: 274.
- ^ a b Milligan, G. J. Cell Sci. 2001, 114, 1265.
- ^ a b Rios, C. D.; Jordan, B. A.; Gomes, I.; Devi, L. A. Pharmacol. Ther. 2001, 92, 71.
- ^ a b George, S. R.; O’Dowd, B. F.; Lee, S. P. Nat. Rev. Drug Discovery 2002, 1, 808.
- ^ a b Agnati, L. F.; Ferre, S.; Lluis, C.; Franco, R.; Fuxe, K. Pharmacol. Rev. 2003, 55, 509.
- ^ a b Franco, R.; Canals, M.; Marcellino, D.; Ferre, S.; Agnati, L.; Mallol, J.; Casado, V.; Ciruela, F.; Fuxe, K.; Lluis, C.; Canela, E. I. (2003). "Marked changes in signal transduction upon heteromerization of dopamine D1 and histamine H3 receptors". Trends Biochem. Sci. 28: 238. doi:10.1111/j.1476-5381.2009.00152.x.CS1 održavanje: više imena: authors list (link)
- ^ a b Kroeger, K. M.; Pfleger, K. D.; Eidne, K. A. Front Neuroendocrinol. 2003, 24, 254
- ^ a b c Terrillon, S.; Bouvier, M. EMBO Rep. 2004, 5, 30.
- ^ Park, P. S.; Filipek, S.; Wells, J. W.; Palczewski, K. Biochemistry 2004, 43, 15643.
- ^ a b Maggio, R.; Novi, F.; Scarselli, M.; Corsini, G. U. FEBS J. 2005, 272, 2939.
- ^ Bulenger, S.; Marullo, S.; Bouvier, M. Trends Pharmacol. Sci. 2005, 26, 131.
- ^ a b Margeta-Mitrovic M, Jan YN, Jan LY (2000). "A trafficking checkpoint controls GABA(B) receptor heterodimerization". Neuron. 27 (1): 97–106. doi:10.1016/S0896-6273(00)00012-X. PMID 10939334.CS1 održavanje: više imena: authors list (link)
- ^ White JH, Wise A, Main MJ, Green A, Fraser NJ, Disney GH, Barnes AA, Emson P, Foord SM, Marshall FH (1998). "Heterodimerization is required for the formation of a functional GABA(B) receptor". Nature. 396 (6712): 679–82. doi:10.1038/25354. PMID 9872316.CS1 održavanje: više imena: authors list (link)
- ^ Kaupmann, K.; Malitschek, B.; Schuler, V.; Heid, J.; Froestl, W.; Beck, P.; Mosbacher, J.; Bischoff, S.; Kulik, A.; Shigemoto, R.; Karschin, A.; Bettler, B. Nature 1998, 396, 683.
- ^ Marshall, F. H.; Jones, K. A.; Kaupmann, K.; Bettler, B. Trends Pharmacol. Sci. 1999, 20, 396.
- ^ Mohler, H.; Fritschy, J. M. Trends Pharmacol. Sci. 1999, 20, 87.
- ^ Kunishima, N.; Shimada, Y.; Tsuji, Y.; Sato, T.; Yamamoto, M.; Kumasaka, T.; Nakanishi, S.; Jingami, H.; Morikawa, K. (2000). "Structural basis of glutamate recognition by a dimeric metabotropic glutamate receptor". Nature. 407: 971. doi:10.1038/35039564.CS1 održavanje: više imena: authors list (link)
- ^ Bockaert, J.; Pin, J. P. (1999). "Molecular tinkering of G protein-coupled receptors: an evolutionary success". EMBO J. 18: 1723. doi:10.1093/emboj/18.7.1723. Arhivirano s originala, 12. 11. 2013. Pristupljeno 18. 6. 2016.CS1 održavanje: više imena: authors list (link)
- ^ Zhu, X.; Wess (1998). "Truncated V2 vasopressin receptors as negative regulators of wild-type V2 receptor function". J. Biochemistry. 37: 15773.CS1 održavanje: više imena: authors list (link)
- ^ Morello, J. P.; Salahpour, A.; Laperriere, A.; Bernier, V.; Arthus, M. F.; Lonergan, M.; Petaja-Repo, U.; Angers, S.; Morin, D.; Bichet, D. G.; Bouvier, M. (2000). "Pharmacological chaperones rescue cell-surface expression and function of misfolded V2 vasopressin receptor mutants". J. Clin. Invest. 105: 887. doi:10.1172/JCI8688.CS1 održavanje: više imena: authors list (link)
- ^ Benkirane, M.; Jin, D. Y.; Chun, R. F.; Koup, R. A.; Jeang, K. T. (1997). "Mechanism of transdominant inhibition of CCR5-mediated HIV-1 infection by ccr5delta32". J. Biol. Chem. 272: 30603.CS1 održavanje: više imena: authors list (link)
- ^ Dean, M. K.; Higgs, C.; Smith, R. E.; Bywater, R. P.; Snell, C. R.; Scott, P. D.; Upton, G. J.; Howe, T. J.; Reynolds, C. A. (2001). "Dimerization of G-protein-coupled receptors". J. Med. Chem. 44: 4595.CS1 održavanje: više imena: authors list (link)
- ^ Filipek, S.; Krzysko, K. A.; Fotiadis, D.; Liang, Y.; Saperstein, D. A.; Engel, A.; Palczewski, K. (2004). "A concept for G protein activation by G protein-coupled receptor dimers: the transducin/rhodopsin interface". Photochem. Photobiol. Sci. 3: 628.CS1 održavanje: više imena: authors list (link)
- ^ Hamm, H. E. (2001). "How activated receptors couple to G proteins" (PDF). Proc. Natl. Acad. Sci. U.S.A. 98: 4819. doi:10.1073ypnas.011099798 Provjerite vrijednost parametra
|doi=(pomoć). - ^ Baneres, J. L.; Parello, J. J. (2003). "G Protein Activation by the Leukotriene B4 Receptor Dimer". Mol. Biol. 329: 815. doi:10.1074/jbc.M710419200.CS1 održavanje: više imena: authors list (link)
- ^ Krishnan A, Alme´n MS, Fredriksson R, Schiöth HB (2012). "The Origin of GPCRs: Identification of Mammalian like Rhodopsin, Adhesion, Glutamate and Frizzled GPCRs in Fungi". PLoS ONE: e29817. doi:10.1371/journal.pone.0029817. PMID 22238661.CS1 održavanje: više imena: authors list (link)
- ^ Nordström KJ, Sällman Almén M, Edstam MM, Fredriksson R, Schiöth HB (2011). "Independent HHsearch, Needleman–Wunsch-Based, and Motif Analyses Reveal the Overall Hierarchy for Most of the G Protein-Coupled Receptor Families". Mol Biol Evol: 2471–80. doi:10.1093/molbev/msr061. PMID 21402729.CS1 održavanje: više imena: authors list (link)
- ^ Bakthavatsalam D, Brazill D, Gomer RH, Eichinger L, Rivero F, Noegel AA (2007). "A G protein-coupled receptor with a lipid kinase domain is involved in cell-density sensing". Curr Biol. 17 (10): 892–7. doi:10.1016/j.cub.2007.04.029. PMID 17481898.CS1 održavanje: više imena: authors list (link)
Vanjski linkovi[uredi | uredi izvor]
- G-protein-coupled receptors na US National Library of Medicine Medical Subject Headings (MeSH)
- G protein spregnuti receptori - MAPK/Erk signalizacija
| G-protein receptor na Wikimedia Commonsu. |

