Insulinoliki faktor rasta 2
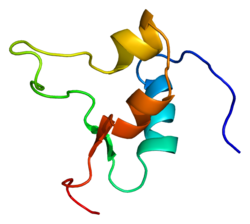
Insulinoliki faktor rasta 2 (IGF-2), jedan je od tri proteinska hormon koji imaju strukturnu sličnost sa insulinom. Definicija MeSH glasi: "Dobro karakterizirani neutralni peptid za koji se vjeruje da ga jetra luči i da cirkulira u krvi. Ima aktivnosti regulacije rasta, slične insulinu i mitogenima. Faktor rasta ima glavnu ulogu, ali ne i apsolutnu, ovisno o somatotropinu. Vjeruje se da je glavni faktor rasta i fetusa, za razliku od insulinolikog faktor rasta 1, koji je glavni faktor rasta kod odraslih"[5]
Struktura gena[uredi | uredi izvor]
Kod ljudi, gen IGF2 nalazi se na hromosomu 11, pozicija: p15.5, regionu koji sadrži brojne imprintirane gene. Kod miševa se ova homologna regija nalazi u distalnokraju hromosoma 7. U oba organizma utisnut je recesivni Igf2, s izrazom koji povoljno rezultira od očeva naslijeđenog alela. Međutim, u nekim regijama ljudskog mozga dolazi do gubitka utiskivanja što rezultira transkripcijom IGF2 i H19 iz oba roditeljska alela.[6]
Protein CTCF je uključen u potiskivanje ekspresije gena, vezujući se za H19, kontrolnu regiju za imprintiranje (ICR) zajedno sa diferencijalno-metiliranom regijom - 1 (DMR1) i regijom za pričvršćivanje matrice −3 (MAR3). Ove tri sekvence DNK vežu se za CTCF na način koji ograničava pristup nižeg pojačivača u regiju Igf2. Mehanizam u kojem se CTCF veže za ove regije još ji'nije poznat, ali može uključivati ili izravnu interakciju DNK-CTCF ili mogu biti posredovani drugim proteinima. Kod sisara (miševi, ljudi, svinje), aktivan je samo alel insulinlikog faktora rasta (IGF2), naslijeđenog od oca; ono što je naslijeđeno od majke nije - fenomen koji se naziva imprinting ili nutiskivanje. Mehanizam: alel majke ima izolator između IGF2 promotora i pojačivača. Kao i alel oca, ali u njegovom slučaju izolator je metiliran. CTCF se više ne može vezati za izolator, pa je pojačivač sada slobodan uključiti očev promotor IGF2.[7]
Funkcija[uredi | uredi izvor]
Glavna uloga IGF-2 je da djelujue kao hormon za poticanje rasta tokom gestacije.
IGF-2 vrši svoje efekte vezanjem za IGF-1 receptor i za kratku izoformu insulinskog receptora (IR-A ili egzon 11.[8] IGF2 se također može vezati za IGF-2 receptor (koji se naziva i kation-nezavisni manoza 6-fosfatni receptor), koji deluje kao signalni antagonist, odnosno spriječave IGF2 odgovore. IGF2 may also bind to the IGF-2 receptor (also called the cation-independent mannose 6-phosphate receptor), which acts as a signalling antagonist; that is, to prevent IGF2 responses.
IGF2 se također može vezati za IGF-2 receptor (koji se naziva i kation-neovisni manozni 6-fosfatni receptor), koji deluje kao signalni antagonist; odnosno spriječiti IGF2 odgovore.
U procesu folikulogeneze, teka-ćelije stvaraju IGF-2 da djeluje na autokrini način na same ćelije-teka, a na parakrini način na ćelije granuloze u jajniku.[nedostaje referenca] IGF2 promovira proliferaciju granuloznih ćelija tokom folikulske faze menstruacijskog ciklusa, djelujući zajedno s folikul-stimulirajućim hormonom (FSH).[9] Nakon ovulacije, IGF-2 pospješuje lučenje progesterona, tokom luteusne faze menstrucijskosđg ciklusa , zajedno sa luteinizirajućim hormonom (LH). Dakle, IGF2 djeluje kao ko-hormon zajedno s FSH i LH.[10]
Studija na Medicinskom fakultetu Mount Sinai (Mount Sinai School of Medicine), otkrila je da IGF-2 može biti povezan sa pamćenjem i reprodukcijom.[11][12]
Klinička relevantnost[uredi | uredi izvor]
Ponekad se proizvodi u prekomjernoj količini u otočićnim ćelijama tumora i neotočnih hipoglikemijskih tumora, uzrokujući hipoglikemiju. Doege-Potterov sindrom je paraneoplazijski sindrom[13] kod kojeg je hipoglikemija povezana sa prisustvom jednog ili više vlaknastih tumora, koji nisu na otočićima u pleuraskoj šupljini. Gubitak utiskivanja IGF2 je uobičajena karakteristika tumora viđenih u poremaćaju zvanom Beckwith-Wiedemannov sindrom. .Kako IGF2 pospješuje razvoj beta-ćelija fetusne gušterače, vjeruje se da je povezan sa nekim oblicima dijabetes melitusa. Preeklampsija inducira smanjenje nivoa metilacije u IGF2 demetiliranoj regiji, a to bi mogao biti jedan od mehanizama koji stoje iza povezanosti između intrauterine izloženosti preeklampsiji i visokog rizika za metaboličke bolesti u kasnijem životu dojenčadi.[14]
Interakcije[uredi | uredi izvor]
Pokazano je da insulinoliki faktor rasta interakcija protein-proteinu intrakciji sa IGFBP3.[15][16][17][18] i transferinom.[15]
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ a b c GRCh38: Ensembl release 89: ENSG00000167244 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000048583 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Insulin-Like Growth Factor II". MeSH. NCBI.
- ^ Pham NV, Nguyen MT, Hu JF, Vu TH, Hoffman AR (Nov 1998). "Dissociation of IGF2 and H19 imprinting in human brain". Brain Research. 810 (1–2): 1–8. doi:10.1016/s0006-8993(98)00783-5. PMID 9813220.
- ^ Russell, Peter J. (2009). iGenetics: A Molecular Approach (3rd izd.). Upper Saddle River, N.J.: Pearson Education. str. 533. ISBN 978-0-321-61022-5. Nepoznati parametar
|name-list-format=zanemaren (prijedlog zamjene:|name-list-style=) (pomoć) - ^ Frasca F, Pandini G, Scalia P, Sciacca L, Mineo R, Costantino A, Goldfine ID, Belfiore A, Vigneri R (1999). "Insulin receptor isoform A, a newly recognized, high-affinity insulin-like growth factor II receptor in fetal and cancer cells". Molecular and Cellular Biology. 19 (5): 3278–88. doi:10.1128/MCB.19.5.3278. PMC 84122. PMID 10207053.
- ^ Neidhart, M (2016). DNA Methylation and Complex Human Disease (1st izd.). San Diego: Academic Press. str. 222. ISBN 9780124201941.
- ^ Neidhart, M (2016). DNA Methylation and Complex Human Disease (1st izd.). San Diego: Academic Press. str. 22. ISBN 978-0124201941.
- ^ Chen DY, Stern SA, Garcia-Osta A, Saunier-Rebori B, Pollonini G, Bambah-Mukku D, Blitzer RD, Alberini CM (Jan 2011). "A critical role for IGF-II in memory consolidation and enhancement". Nature. 469 (7331): 491–7. doi:10.1038/nature09667. PMC 3908455. PMID 21270887.
- ^ Agis-Balboa RC, Arcos-Diaz D, Wittnam J, Govindarajan N, Blom K, Burkhardt S, Haladyniak U, Agbemenyah HY, Zovoilis A, Salinas-Riester G, Opitz L, Sananbenesi F, Fischer A (Oct 2011). "A hippocampal insulin-growth factor 2 pathway regulates the extinction of fear memories". The EMBO Journal. 30 (19): 4071–83. doi:10.1038/emboj.2011.293. PMC 3209781. PMID 21873981.
- ^ Balduyck B, Lauwers P, Govaert K, Hendriks J, De Maeseneer M, Van Schil P (Jul 2006). "Solitary fibrous tumor of the pleura with associated hypoglycemia: Doege-Potter syndrome: a case report". Journal of Thoracic Oncology. 1 (6): 588–90. doi:10.1097/01243894-200607000-00016. PMID 17409923.
- ^ He J, Zhang A, Fang M, Fang R, Ge J, Jiang Y, Zhang H, Han C, Ye X, Yu D, Huang H, Liu Y, Dong M (12. 7. 2013). "Methylation levels at IGF2 and GNAS DMRs in infants born to preeclamptic pregnancies". BMC Genomics. 14: 472. doi:10.1186/1471-2164-14-472. PMC 3723441. PMID 23844573.
- ^ a b Storch S, Kübler B, Höning S, Ackmann M, Zapf J, Blum W, Braulke T (Dec 2001). "Transferrin binds insulin-like growth factors and affects binding properties of insulin-like growth factor binding protein-3". FEBS Letters. 509 (3): 395–8. doi:10.1016/S0014-5793(01)03204-5. PMID 11749962.
- ^ Buckway CK, Wilson EM, Ahlsén M, Bang P, Oh Y, Rosenfeld RG (Oct 2001). "Mutation of three critical amino acids of the N-terminal domain of IGF-binding protein-3 essential for high affinity IGF binding". The Journal of Clinical Endocrinology and Metabolism. 86 (10): 4943–50. doi:10.1210/jcem.86.10.7936. PMID 11600567.
- ^ Twigg SM, Baxter RC (Mar 1998). "Insulin-like growth factor (IGF)-binding protein 5 forms an alternative ternary complex with IGFs and the acid-labile subunit". The Journal of Biological Chemistry. 273 (11): 6074–9. doi:10.1074/jbc.273.11.6074. PMID 9497324.
- ^ Firth SM, Ganeshprasad U, Baxter RC (Jan 1998). "Structural determinants of ligand and cell surface binding of insulin-like growth factor-binding protein-3". The Journal of Biological Chemistry. 273 (5): 2631–8. doi:10.1074/jbc.273.5.2631. PMID 9446566.
Dopunska literatura[uredi | uredi izvor]
- O'Dell SD, Day IN (Jul 1998). "Insulin-like growth factor II (IGF-II)". The International Journal of Biochemistry & Cell Biology. 30 (7): 767–71. doi:10.1016/S1357-2725(98)00048-X. PMID 9722981.
- Butler AA, Yakar S, Gewolb IH, Karas M, Okubo Y, LeRoith D (Sep 1998). "Insulin-like growth factor-I receptor signal transduction: at the interface between physiology and cell biology". Comparative Biochemistry and Physiology B. 121 (1): 19–26. doi:10.1016/S0305-0491(98)10106-2. PMID 9972281.
- Kalli KR, Conover CA (maj 2003). "The insulin-like growth factor/insulin system in epithelial ovarian cancer". Frontiers in Bioscience. 8 (4): d714–22. doi:10.2741/1034. PMID 12700030.
- Wood AW, Duan C, Bern HA (2005). Insulin-like growth factor signaling in fish. International Review of Cytology. 243. str. 215–85. doi:10.1016/S0074-7696(05)43004-1. ISBN 9780123646477. PMID 15797461.
- Fowden AL, Sibley C, Reik W, Constancia M (2006). "Imprinted genes, placental development and fetal growth". Hormone Research. 65 Suppl 3 (3): 50–8. doi:10.1159/000091506. PMID 16612114.
Vanjski linkovi[uredi | uredi izvor]
- Insulin-Like Growth Factor II na US National Library of Medicine Medical Subject Headings (MeSH)
| Commons ima datoteke na temu: Insulinoliki faktor rasta 2 |