Litij
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Litij u periodnom sistemu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Hemijski element, Simbol, Atomski broj | Litij, Li, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serija | Alkalni metali | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa, Perioda, Blok | 1, 2, s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izgled | srebreno-bijeli, sivi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Zastupljenost | 0,006[1][2] % | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomske osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomska masa | 6,941[3] u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomski radijus (izračunat) | 145 (167) pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentni radijus | 128 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsov radijus | 182 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronska konfiguracija | [He] 2s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Broj elektrona u energetskom nivou | 2, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izlazni rad | 2,9[4] eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. energija ionizacije | 520,2 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fizikalne osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Agregatno stanje | čvrsto | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohsova skala tvrdoće | 0,6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristalna struktura | kubična, prostorno orjentirana | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gustoća | 534 (pri 20 °C)[5][6] kg/m3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetizam | paramagnetičan (= 1,4 · 10−5)[7] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tačka topljenja | 453,69 K (180,54 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tačka ključanja | 1603[8] K (1330 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molarni volumen | 13,02 • 10-6 m3/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplota isparavanja | 136[8] kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplota topljenja | 3 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pritisak pare | 1,63 Pa pri 453,7 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brzina zvuka | 6000 m/s pri 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Specifična toplota | 3482[2] J/(kg · K) kod 298 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Specifična električna provodljivost | 10,6 • 106 S/m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Toplotna provodljivost | 85 W/(m · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hemijske osobine | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidacioni broj | +1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksid | Li2O | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrodni potencijal | −3,04 V | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativnost | 0,98 (Pauling-skala) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sigurnosno obavještenje | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oznake upozorenja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Obavještenja o riziku i sigurnosti | R: 14/15-34 S: (1/2-)8-43-45 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ako je moguće i u upotrebi, koriste se osnovne SI jedinice. Ako nije drugačije označeno, svi podaci dobijeni su mjerenjima u normalnim uvjetima. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Litij (izvedeno iz grč. λίθος, líthos, kamen) jeste hemijski element sa simbolom Li i rednim (atomskim) brojem 3. On je alkalni metal u drugoj periodi periodnom sistemu elemenata. Litij je vrlo lahak metal i ima najmanju gustoću među svim čvrstim elementima (u standardnim uslovima).
Zbog svoje velike reaktivnosti, u prirodi se ne nalazi u elementarnom stanju. Na sobnoj temperaturi, samo na potpuno suhom zraku je postojan duže vrijeme, ali vrlo sporo reagira dajući litij nitrid. U vlažnom zraku, na površini litija vrlo brzo se formira mat sivi sloj litij-hidroksida. Kao i svi alkalni metali, elementarni litij reagira odmah već pri dodiru sa vlagom na koži te tako može prouzrokovati teške opekotine i ozljede zbog nagrizanja. Mnogi spojevi litija, koji u vodenim rastvorima daju ione litija smatraju se opasnim za zdravlje, za razliku od analognih spojeva natrija i kalija.
Kao mikroelement, litij u obliku svojih soli je često sastavni dio mineralnih voda. U ljudskom organizmu nalaze se vrlo malehne količine ovog elementa. Ne smatra se neophodnim za život i nema poznate biološke funkcije u organizmu. Međutim, neke soli litija pokazuju medicinsko djelovanje i upotrebljavaju se u litijskoj terapiji pri liječenju bipolarnih poremećaja, manija, depresija i drugih sličnih bolesti.
Historija[uredi | uredi izvor]

Smatra se da je litij otkrio švedski naučnik Johan August Arfwedson, koji je 1817. primijetio prisustvo nekog nepoznatog elementa u mineralu petalitu (Li[4]Al[4][Si4O10]) a nedugo poslije također i u mineralima spodumenu (LiAl[Si2O6]) i lepidolitu (K(Li,Al)3[(Al,Si)4O10](F,OH)2), nakon analize mineralnih uzoraka sa ostrva Utö u Švedskoj. Njegov akademski učitelj Jacob Berzelius predložio je naziv lithion, izvedenicu iz grčkog λίθος líthos‚ kamen, ime koje je izvedeno iz materijala iz kojeg je izoliran, slično kao i kod drugih, do tada poznatih, alkalnih metala natrija i kalija, a kasnije se to ime ustalilo u svojoj latiniziranoj formi lithium. [9] Njemački hemičar Christian Gottlob Gmelin primijetio je 1818. godine da soli litija boje plamen u crvenu boju. Oba naučnika su narednih godina pokušavali dobiti ovaj element u čistom stanju. Ovo je uspjelo iste godine Brandeu i Davyu pomoću postupka elektrolize litij oksida (Li2O).
Robert Bunsen i Augustus Matthiessen uspjeli su 1855. pomoću elektrolize litij-hlorida (LiCl) dobiti još veće količine elementarnog litija. Prva komercijalna proizvodnja počela je 1923. u njemačkoj kompaniji "Metallgesellschaft" (danas Chemetall GmbH), gdje se dobijao pomoću elektrolize istopljene smjese litij- (LiCl) i kalij-hlorida (KCl). Wilhelm Schlenk je 1917. sintetizirao prvi litijorganski spoj iz organskih spojeva žive.[10] Sve do kraja Drugog svjetskog rata, osim upotrebe kao sredstvo za podmazivanje (mineralno ulje sa dodatkom litij-stearata) i u industriji stakla (litij-karbonat ili litij-oksid), gotovo da i nisu postojae aplikacije u kojima se koristio litij. Međutim, to se promijenilo nakon što je SAD-u zatrebao tricij za pravljenje hidrogenske bombe, a koji se može dobiti iz litija. Počela je znatna proizvodnja litija, a jedno od najizdašnijih nalazišta bio je rudnik u blizini gradića Kings Mountain u Sjevernoj Karolini.[11] Pošto tricij ima vrlo kratko vrijeme poluraspada, neophodne količine litij su konstantno rasle, pa je SAD u periodu od 1953. do 1963. nagomilao ogromne zalihe ovog metala, koje su tek nakon završetka Hladnog rata 1993. dospjele na svjetsko tržište.[11]
Osim klasičnog rudarenja, jeftinije dobijanje litija je moguće i iz slanih voda. Danas se litij koristi u velikim količinama za razne svrhe kao što je proizvodnja baterija, za polimerizaciju elastomera, u građevinarstvu te za organske sinteze u farmaciji i argohemijskoj industriji. Od 2007. najvažniji segment upotrebe litija su primarne (takozvane "litijske") baterije i akumulatori (sekundarne ili litij-ionske baterije).[12]
Osobine[uredi | uredi izvor]
Fizičke[uredi | uredi izvor]
Elementarni litij je srebreno-bijeli, mehki i lahki metal. Na sobnoj temperaturi je najlakši među svim čvrstim elementima (gustoća 0,534 g/cm3[14]). Samo vodik u čvrstom stanju pri temperaturi od −260 °C ima manju gustoću od 0,0763 g/cm3.[14]
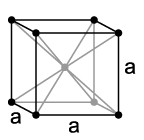
Poput drugih alkalnih metala, i litij se kristalizira u kubičnom, prostorno centriranom, gusto pakovanom kristalnom sistemu u prostornoj grupi Im3m sa parametrom rešetke a = 351 pm i dvije formulske jedinice po elementarnoj ćeliji. Na izuzetno niskim temperaturama od 78 K mijenja se kristalna struktura spontanim prijelazom bilo u heksagonalnu strukturu tipa magnezija sa parametrima rešetke a = 311 pm i c = 509 pm ili izmjenom u izobličenu kubičnu strukturu tipa bakra (kubična plošno centrirana) sa parametrom rešetke a = 438 pm. Tačan uzrok zbog čega se javlja jedna od ovih struktura nije poznat.[13]
Litij među ostalim alkalnim metalima ima najviše tačke topljenja i ključanja kao i najveći specifični toplotni kapacitet. Iako on ima najveću tvrdoću od svih alkalnih metala, može se rezati nožem a njegova Mohsova tvrdoća iznosi 0,6.[6][15] Kao tipičan metal, dobar je provodnik struje (provodljivost oko 18% od provodljivosti bakra[1]) kao i toplote.
Litij ispoljava veliki broj sličnosti sa magnezijem, što se, između ostalog, iskazuje i i činjenici javljanja heterotipskih miješanih kristala od litija i magnezija, a koji imaju osobinu izodimorfije. Iako se magnezij najgušće kristalizira heksagonalno, dok se nasuprot njega litij kristalizira u kubičnu prostorno centriranu kuglastu rešetku, oba metala se mogu heterotipski miješati.[16] Međutim, ovo se dešava samo u vrlo ograničenom rasponu koncentracija, pri čemu kod suviška neke od komponenti, jedna od njih nameće (prisiljava da promijeni) kristalnu rešetku drugoj.
Ion litija sa −520 kJ/mol[17] ima najvišu entalpiju hidratacije među svim ionima alkalnih metala. Stoga se on u vodi u potpunosti hidratizira i snažno privlači molekule vode. Ion litija gradi dvije hidratne ljuske, jednu unutrašnju sa četiri molekule vode, koja je izuzetno snažno povezana sa litijevim ionom preko svojih atoma kisika, te jednu vanjsku ljusku, koja je povezana sa ionom Li[H2O]4+ preko "vodikovog mosta" sa drugim molekulima vode. Zbog toga je ionski radijus hidratiziranih iona litija veoma velik, veći čak i od nekih iona teških alkalnih metala kao što su rubidij i cezij, koji u vodenim rastvorima ne grade takvu vrstu snažno vezanih hidratnih ljuski.

U gasovitom stanju, litij se ne nalazi u vidu pojedinačnih atoma, već u molekularnom stanju kao dilitij Li2. Na taj način jednovalentni litij dostiže popunjenu s-atomsku orbitalu a time i energetski povoljniju situaciju. Dilitij ima dužinu veze od 267,3 pm i energiju veze od 101 kJ/mol.[18]
Hemijske[uredi | uredi izvor]

Litij je, kao i svi drugi alkalni metali, vrlo reaktivan i vrlo lahko reagira sa mnogim elementima i spojevima (poput vode dajući toplotu). Među svim alkalnim metalima, on je najviše reaktivan. Posebnost, po kojoj se litij razlikuje od drugih alkalnih metala je njegova reakcija sa molekularnim dušikom gradeći litij nitrid, reakcija koja se polahko odvija već i na sobnoj temperaturi:
- .
Ovo je moguće zbog velike gustoće naboja iona litija Li+ te tako i velike energije rešetke litij nitrida. Litij sa -3,04 V[17] ima najniži elektrodni potencijal u cijelom periodnom sistemu, te je stoga i najmanje plemeniti element od svih. Kao i svi alkalni metali, elementarni litij se može čuvati u kerozinu (petroleumu) ili parafinskom ulju, jer u suprotnom reagira sa dušikom i kisikom iz zraka.
Pošto su radijusi iona litija Li+ i magnezija Mg2+ slični po veličini, također postoje i određene sličnosti u osobinama litija odnosno njegovih spojeva sa magnezijem ili spojevima magnezija. Ova sličnost u osobinama između dva elementa iz susjednih grupa periodnog sistema poznata je i kao dijagonalna veza (dijagonalni efekt). Tako litij, za razliku od natrija, gradi mnoge metalnoorganske spojeve (organolitijske spojeve), poput butil-litija ili metil-litija. Ista sličnost uočena je i između berilija i aluminija, kao i između bora i silicija.
Izotopi[uredi | uredi izvor]
U prirodi se javljaju oba stabilna izotopa litija 6Li (7,6 %) i 7Li (92,4 %). Osim njih, poznato je još nekoliko nestabilnih izotopa počev od 4Li preko 8Li do 12Li, koji se mogu dobiti samo vještačkim putem. Njihova vremena poluraspada iznose samo nekoliko milisekundi.[19]

Izotop 6Li ima vrlo važnu ulogu u tehnologiji nuklearne fuzije. Pored uloge u nuklearnim fuzijskim reaktorima, služi i kao polazni materijal za dobijanje tricija u hidrogenskoj bombi, koji je neophodan za fuziju sa deuterijem kojom se proizvodi enormna količina energije. Tricij nastaje u plaštu fuzijskog reaktora (takozvanom blanketu) ili unutar hidrogenske bombe pored helija bombardiranjem litija 6Li neutronima, koji nastaju tokom fuzije, a prema sljedećoj nuklearnoj reakciji:
- .
Također, moguća je i reakcija
ali je ona manje pogodna.
Iz ovog razloga, izotop 6Li se izdvaja pri proizvodnji litija.[20] Razdvajanje izotopa se može vršiti naprimjer putem razmjene izotopa litijamalgama i nekog rastvorenog litijevog spoja (poput litij-hlorida u etanolu). Pri tome se može dostići prinos od oko 50%.[21]
Izotop 7Li nastaje u neznatnim količinama u nuklearnim centralama putem nuklearne reakcije izotopa bora 10B (korišten kao usporivač neutrona) sa neutronima.[22]
Oba izotopa litija 6Li i 7Li korištena su u eksperimentima sa ultrahladnim kvatnim gasovima. Tako je načinjen i prvi Bose-Einsteinov kondenzat sa (bozon) izotopom 7Li.[23] Međutim 6Li je fermion[24][25] te su naučnici 2003. godine uspjeli molekulu ovog izotopa pretvoriti u superfluid.[26]
Rasprostranjenost[uredi | uredi izvor]

Zemljina kora sadrži oko 0,006 % litija.[1] Time je nešto rjeđi od cinka, bakra i volframa, a u Zemljinoj kori je otprilike rasprostranjen kao i kobalt, kalaj i olovo. Iako je litij rasprostranjen otprilike kao i olovo, njegova proizvodnja je vrlo teška zbog malehne koncentracije i velike raspršenosti.[27] Procijenjene i identificirane količine litija na Zemlji iznose više od 29 miliona tona, dok sirovinska baza iznosi oko 13 miliona tona (stanje 2011).[28] Procijenjene dostupne rezerve u 2009. godine iznosile su oko 4,1 miliona tona.[29]
Litij se nalazi i u vodi za piće kao i nekim prehrambenim namirnicama poput mesa, ribe, jaja i mliječnih proizvoda. Tako naprimjer 100 grama mesa sadrži oko 100 μg litija.[30]
Primarna nalazišta[uredi | uredi izvor]
Litij se nalazi u sastavu nekih minerala kao litij-pegmatit. Neki od najvažnijih minerala su ambligonit (LiAl[PO4]F), lepidolit (K(Li,Al)3[(Al,Si)4O10](F,OH)2), petalit (kastor, LiAl[Si4O10]) i spodumen (trifan; LiAl[Si2O6]). Ovi minerali imaju sadržaj litij do najviše 9% (kod ambligonita). Druge, mnogo rjeđe, rude litija su kriolitionit (Li3Na3[AlF6]2), u kojem je pronađen najveći udio litija među svim mineralima, trifilin (Li(FeII,MnII)[PO4]) i cinvaldit (K(Li,Fe,Al)3[(Al,Si)4O10](F,OH)2).
Litijevi minerali se nalaze u sastavu mnogih silikatnih stijena, ali uglavnom u veoma niskim koncentracijama. Ne postoje njegova velika nalazišta. Pošto je izdvajanje litija iz ovih minerala uslovljeno velikim troškovima, danas ono za dobijanje litija ili njegovih spojeva igra manju ulogu, ali se to može promijeniti zbog očekivanog porasta potražnje za njim. Također, vrše brojna istraživanja širom svijeta u oblasti lakšeg i isplativijeg dobijanja litija. Među najvećim rudnicima litija su rudnici Greenbushes[31] i Mt. Cattlin u Zapadnoj Australiji, u kojima se kopa mineral pegmatit sa velikom koncentracijom litija, a litij se dobija i kao sporedni proizvod pri proizvodnji metala tantala. I u drugim zemljama kao što su Kanada i Rusija, te do 1998. u SAD kod grada Bassemer City, Sjeverna Karolina, iskopava se mineral spodumen iz kojeg se izdvaja litij.[32]
Za najveće nalaziše litija u Evropi smatra se okrug Wolfsberg u austrijskoj pokrajini Koruška. Nakon završetka probnih bušenja krajem 2013. godine, australijski Global Strategic Metals planira u Wolfsbergu početi sa kopanjem litijeve rude počev od 2016. godine.[33] Međutim, neki kritičari naglašavaju da je takav projekat neisplativ, jer se ruda nalazi duboko u stijenama, te da su troškovi kopanja u usporedbi sa površinskim kopovima u Čileu ogromni.
Sekundarna nalazišta[uredi | uredi izvor]
| Država | Proizvodnja | Rezerve[35] |
|---|---|---|
| 3.200 | 850.000 | |
| 9.260 | 970.000 | |
| 160 | 64.000 | |
| 480 | 180.000 | |
| 12.600 | 7.500.000 | |
| 5.200 | 3.500.000 | |
| 820 | 10.000 | |
| 470 | 23.000 | |
| Ukupno svijet | 34.000 | 13.000.000 |
Litijeve soli, naročito litij-hlorid, nalaze se u sastavu mnogih slanih depozita, uglavnom isušenih mora i slanih jezera. Njegova koncentracija na tim mjestima može iznositi i do jedan postotak. Za kvalitet slanih naslaga, osim koncentracije litija, važni su i omjeri količina magnezija i litija. Danas se litij dobija uglavnom u Čileu (Salar de Atacama), (gdje su pronađene naslage sa sadržajem litija od 0,16% što je među najvišim u svijetu[27]), Argentini (Salar de Hombre Muerto), SAD (Silver Peak, Nevada) i Kini (jezero Zhabuye, Tibet, jezero Taijinaier, Qinqhai). Postoje i druga slana jezera sa velikim sadržajem litija, ali se ona trenutno ne eksploatiraju, naprimjer u Kini, Argentini, Afganistanu i naročito u Boliviji, gdje je u slanom jezeru Salar de Uyuni procijenjeno da se nalazi oko 5,4 miliona tona litija, što možda predstavlja najveće nalazište.[29]
Kao povezani i nusproizvodi pri proizvodnji litija često se javljaju kalij-karbonat (potaša), boraks, cezij i rubidij.
Razne biljke kao što su duhan ili vrste iz roda Ranunculus uzimaju litijeve spojeve iz zemljišta i skladište ih u sebi. Prosječni udio litijevih spojeva u suhoj masi tih biljaka iznosi između 0,5 ppm i 3 ppm. U vodama svjetskih mora nalazi se i litij u srednjoj koncentraciji od 180 ppb dok se u tekučim vodama nalazi u koncentraciji do 3 ppb.
Zbog očekivanog porasta potražnje za litijem za potrebe proizvodnje baterija i akumulatora za vozila na električni pogon, danas mnoge kompanije istražuju isplative načine dobijanja minerala i slanih naslaga u kojima ima dovoljno litija u mnogim regijama svijeta, uključujući i Evropu.[36]
U svemiru[uredi | uredi izvor]
Nakon Velikog praska, osim izotopa vodika i helija, nastale su i znatne količine izotopa litija 7Li. Međutim, najveći dio od ovog litija danas ne postoji, jer je on u zvijezdama fuzionirao sa vodikom u procesu proton-proton reakcije II te je tako potrošen.[37]
U smeđim patuljcima masa i temperatura zvijezde nisu dovoljno visoke za fuziju vodika, jer njena masa ne doseže neophodnu veličinu od otprilike 75 mâsa Jupitera. Tako litij nastao tokom Velikog praska ostaje u smeđim patuljcima sadržan u velikim količinama. Iz ovih razloga, litij je također relativno rijedak element i u svemiru, ali njegovo prisustvo može poslužiti kao dokaz postojanja smeđih patuljaka.[38]
Udio litija u raznim zvijezdama je dosta različita, čak i kada su njihove mase, starost ili metalicitet vrlo slični. Vjerovalo se da planete mogu imati utjecaj na sadržaj litija neke zvijezde. Ukoliko naprimjer neka zvijezda nema planeta koje kruže oko nje, smatralo se da je udio litija u njoj vrlo visok, dok zvijezde poput Sunca koje su okružene brojnim planetama, sadrže vrlo malo litija u sebi. Uzrok tome se prepostavlja da planete svojim gravitacijskim utjecajima doprinose na snažno miješanje vanjskih i unutrašnjih slojeva u zvijezdi, tako da više litija dospijeva u područja unutar zvijezde gdje je dovoljno visoka temperatura za odvijanje procesa fuzije.[39]
Dobijanje[uredi | uredi izvor]
Iz slanih rastvora koji sadrže litij, može se istaložiti litij-karbonat razblaživanjem vodom i dodavanjem natrij-karbonata (sode). Zatim se uparava slana voda u zraku sve dok udio litija ne pređe 0,5%. Dodavanje natrij karbonata iz nje se počinje taložiti teško rastvorljivi litij karbonat:
- .
Neračunajući proizvodnju u SAD, tokom 2008. godine u svijetu je proizvedeno oko 27.400 tona litija,[29] a uglavnom se na tržištu prodavao u obliku litij karbonata (Li2CO3). Od ove količine 12.000 tona otpada na čileansku Salar de Atacama, a gotovo 7.000 tona na australijski rudnik Greenbushes.
Da bi se dobio metalni litij, prvo se litij karbonatu mora dodati hlorovodična kiselina. Pri tome nastaje ugljik dioksid koji se izdvaja kao gas, te preostaje rastvoreni litij-hlorid. Ovaj rastvor se stavlja u vakuumski isparivač gdje isparava, sve dok se hlorid ne iskristalizira:
Uređaji i oprema koja se koristi za dobijanje litij-hlorida moraju biti načinjeni iz posebnih vrsta čelika ili legura nikla, jer slani rastvor djeluje izuzetno korozivno. Metalni litij se dobija elektrolizom topivim elektrodama pri temperaturi od 352 °C iz istopljene eutektične smjese iz 52 masena postotka litij-hlorida i 48 masena postotka kalij-hlorida:
odnosno:
- .
Međutim, u procesu elektrolize, kalij se ne izdvaja jer u istopljenom hloridu on ima niži elektrodni potencijal. Za razliku od njega, tragovi natrija se izdvajaju, te čine litij izuzetno reaktivnim (što je prednost u organskoj hemiji, ali ne i za Li-baterije). Tečni litij se skuplja na površini elektrolita, te se relatno lahko može izdvojiti iz elektrolitičke ćelije. Litij je također moguće dobiti i elektrolizom litij-hlorida u piridinu. Ova metoda je posebno pogodna za laboratorijsko dobijanje manjih količina litija.
Upotreba[uredi | uredi izvor]

Najveći dio proizvedenih soli litija se ne reducira do metalnog litija, već se koristi bilo direktno kao litij-karbonat, litij-hidroksid, litij-hlorid, litij-bromid ili se prevodi u neki drugi spoj litija. Kao metal, on je neophodan u određenom broju aplikacija, među kojima je najviše u industriji baterija i industriji stakla i keramike. Najvažniji vidovi upotrebe njegovih spojeva navedeni su u odjeljku „spojevi“.
Kao metal[uredi | uredi izvor]
Dio proizvedenog metalnog litija koristi se za dobijanje njegovih spojeva, koji se ne mogu direktno dobiti iz litij karbonata. To su, u prvom redu, organolitijski spojevi poput butil-litija, spojeva litija i vodika kao litij-hidrida (LiH) ili litij aluminij-hidrida kao i litij-amida. Zbog mogućnosti litija da reagira direktno sa dušikom, koristi se i za uklanjanje tog gasa tamo gdje je to neophodno.
Metalni litij je izuzetno snažno redukcijsko sredstvo. On reducira mnoge materijale, koji inače ne reagiraju sa drugim redukcijskim sredstvima. Upotrebljava se i za djelomično hidriranje aromatskih spojeva (Birchova redukcija). U metalurgiji, koristi se za odstranjivanje sumpora iz istopljenog željeza, dezoksidaciju i uklanjanje ugljika iz istopljenih metala.
Pošto litij ima veoma nizak normni potencijal, može se upotrebljavati u baterijama kao anoda. Takve litijske baterije imaju vrlo veliku gustoću energije a mogu proizvesti posebno visok električni napon. Treba razlikovati litijske baterije koje se ne mogu ponovno puniti sa punjivim litij-ionskim baterijama (akumulatorima), kod kojih se kao katoda koristi metalni oksid litija kao naprimjer litij kobalt oksid a na strani anode koristi se grafit ili neki spoj na kojem interkaliraju ioni litija.[40]
Sastojak legura[uredi | uredi izvor]
Litij se ponekad dodaje drugim metalima pri njihovom legiranju, radi poboljšanja njihovih osobina. Često za u te svrhe budu dovoljne i vrlo malehne količine litija. Mnogim supstancama dodavanje litija poboljšava otpornost na izvlačenje, tvrdoću i mehaničku elastičnost. Jedan od primjera legura sa litijem je takozvani Bahnmetall (njem. željeznički metal), legura olova sa oko 0,04% litija, koja se koristi u Njemačkoj kao materijal za izradu valjkastih ležaja na željeznicama. Također i u magnezijskim i aluminijskim legurama, litij se dodaje za poboljšanje mehaničkih osobina. Istovremeno, legure litija su vrlo lahke i stoga se često koriste i u avionskoj i svemirskoj tehnici.
Istraživanje (atomska fizika)[uredi | uredi izvor]
U oblasti atomske fizike, litij se vrlo često upotrebljava, jer je kao 6Li jedini među alkalnim metalima sa stabilnim fermionskim izotopom, zbog čega je pogodan za istraživanje efekata u ultrahladnim fermionskim kvantnim gasovima. Istovremeno, iskazuje veoma široku Feshbach rezonancu, koja omogućava da se dužina raspršenja između atoma podešava po želji, pri čemu se ne mora posebno precizno održavati magnetno polje zbog širine rezonance.
Medicina[uredi | uredi izvor]
Već od 1850. litij se počeo koristiti u medicini zapadnoevropskih zemalja kao sredstvo protiv gihta. Međutim, nije se pokazao djelotvoran. I drugi vidovi upotrebe litijevih soli u medicini su također ostali bezuspješni, između ostalih i kao sredstvo protiv infektivnih bolesti.
Tek 1949. australijski fizijatar John Cade opisao je moguću oblast upotrebe litijevih soli. On je zamorcima ubrizgavao različite hemijske spojeve, između ostalih i soli litija, od čega su oni mnogo slabije reagirali na vanjske podražaje, te su bili mnogo mirniji ali ne i pospani.[41] Tek nakon što je isto isprobao i na sebi između 1952. i 1954. Cade je podržao upotrebu litij karbonata kao lijeka u terapiji depresivnih, shizofrenih i maničnih pacijenata, a nakon provedene opsežne studije na psihijatrijskoj bolnici u Risskovu (Danska).[42] Time su postavljeni budući temelji današnje terapije litijem.
Spojevi[uredi | uredi izvor]
Litij je veoma reaktivan i sa većinom nemetala gradi spojeve u kojima se uvijek nalazi u oksidacijskom stanju +I. Ovi spojevi su uglavnom načinjeni ionskom vezom, ali za razliku od spojeva drugih alkalnih metala imaju veliki kovalentni udio. To se iskazuje između ostalog i po tome što su mnoge soli litija, za razliku od odgovarajućih natrijevih i kalijevih soli, dobro rastvorljive u organskim rastvaračima poput acetona i etanola.
Neki od neorganskih spojeva litija su:
- Litij-hidrid LiH
- Litij bor-hidrid LiBH4
- Litij aluminij-hidrid LiAlH4
- Litij-oksid Li2O
- Litij-peroksid Li2O2
- Litij-hidroksid LiOH
- litijevi halogenidi: litij-fluorid, litij-hlorid, litij-bromid i litij-jodid
- Litij-karbonat Li2CO3
- Litij-perhlorat LiClO4
- Litij-sulfat Li2SO4
- Litij-nitrat LiNO3
- Litij-nitrid Li3N
Za razliku od većine drugih alkalnometalnih organskih spojeva, litijevi organski spojevi imaju značajnu ulogu naročito u organskoj hemiji. Od posebnog značaja su n-butil-litij, tert-butil-litij, metil-litij i fenil-litij.
Reference[uredi | uredi izvor]
- ^ a b c dtv-Atlas Chemie. 1 (9 izd.). dtv. 2000. ISBN 9783423032179.
- ^ a b Harry H. Binder (1999). Lexikon der chemischen Elemente. Stuttgart: S. Hirzel Verlag. ISBN 3-7776-0736-3.
- ^ Michael E. Wieser, Tyler B. Coplen (2010). "Atomic weights of the elements 2009 (IUPAC Technical Report)". Pure and Applied Chemistry: 1. doi:10.1351/PAC-REP-10-09-14.
- ^ Ludwig Bergmann, Clemens Schaefer, Rainer Kassing (2005). Lehrbuch der Experimentalphysik, Band 6: Festkörper (2 izd.). Walter de Gruyter. str. 361. ISBN 978-3-11-017485-4.CS1 održavanje: više imena: authors list (link)
- ^ N. N. Greenwood, A. Earnshaw (1988). Chemie der Elemente (1 izd.). Weinheim: VCH. str. 97. ISBN 3-527-26169-9.
- ^ a b ""Lithium". The Gale Encyclopedia of Science. Gale. 2008. ISBN 978-1578516803. Pristupljeno 5. 9. 2014.
- ^ Robert C. Weast, ured. (1990). CRC Handbook of Chemistry and Physics. Boca Raton: CRC (Chemical Rubber Publishing Company). str. E-129 do E-145. ISBN 0-8493-0470-9.
- ^ a b Yiming Zhang, Julian R. G. Evans, Shoufeng Yang (2011). "Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks". Journal of Chemical & Engineering Data. 56: 328–337. doi:10.1021/je1011086.CS1 održavanje: više imena: authors list (link)
- ^ N. Figurowski (1981). Die Entdeckung der chemischen Elemente und der Ursprung ihrer Namen. Köln: Aulis-Verlag Deubner. str. 135. ISBN 3-7614-0561-8.
- ^ C. Elschenbroich (2009). Organometallchemie (6 izd.). Leipzig: Teubner B.G. Gmbh. str. 16. ISBN 9783835192232.
- ^ a b Jessica Elzea Kogel (2006). Industrial minerals & rocks: commodities, markets, and uses (7 izd.). SME. str. 599. ISBN 978-0-87335-233-8.
- ^ United States Geological Survey: Minerals Yearbook 2007: Lithium. (PDF), 2007.
- ^ a b K. Schubert: Ein Modell für die Kristallstrukturen der chemischen Elemente u: Acta Crystallographica 30, 1974, str. 193–204, doi:10.1107/S0567740874002469.
- ^ a b Arnold F. Holleman, Egon Wiberg, Nils Wiberg (1985). Lehrbuch der Anorganischen Chemie (91–100 izd.). Berlin: de Gruyter. str. 928–931. ISBN 3-11-007511-3.CS1 održavanje: više imena: authors list (link)
- ^ Litij na stranici webelements.com, fizičke osobine.
- ^ H. Malissa: Die Trennung des Lithiums vom Magnesium in Lithium-Magnesium-Legierungen. u: Fresenius’ Journal of Analytical Chemistry. 171, br. 4, 1959, str. 281–282, doi:10.1007/BF00555410.
- ^ a b M. Binnewies (2004). Allgemeine und Anorganische Chemie (1 izd.). Spektrum Verlag. str. 241. ISBN 978-3827402080.
- ^ Mark J. Winter (1994). Chemical Bonding. Oxford University Press. ISBN 0-19-855694-2.
- ^ The Nubase evaluation of nuclear and decay properties Arhivirano 24. 7. 2013. na Wayback Machine (PDF, engl.).
- ^ ABC oružje.
- ^ Richard Bauer (1985). "Lithium – wie es nicht im Lexikon steht". Chemie in unserer Zeit. 19 (5): 167–173. doi:10.1002/ciuz.19850190505.
- ^ Martin Volkmer (2007). Kernenergie Basiswissen (PDF). Inforum. str. 39. ISBN 3-926956-44-5. Arhivirano s originala (pdf), 17. 6. 2012. Pristupljeno 29. 11. 2014.
- ^ C. C. Bradley, C. A. Sackett, J. J. Tollett, R. G. Hulet: Evidence of Bose-Einstein Condensation in an Atomic Gas with Attractive Interactions. u: Physical Review Letters 75, br. 9, 1995, str. 1687–1690, doi:10.1103/PhysRevLett.75.1687 (PDF[mrtav link]).
- ^ Fermionic Studies in 6Lithium
- ^ A. V. Ling (2006). Focus on Boson Research. Nova Publishers. str. 184. ISBN 9781594545207.
- ^ S. Jochim, M. Bartenstein, A. Altmeyer, G. Hendl, S. Riedl, C. Chin, J. Hecker Denschlag, R. Grimm: Bose-Einstein Condensation of Molecules. u: Science. 302, br. 5653, 2003, str. 2101–2103, doi:10.1126/science.1093280
- ^ a b VDI nachrichten: Lithium – ein Spannungsmacher auf Kreislaufkurs Arhivirano 7. 4. 2020. na Wayback Machine. 7. januar 2011, str. 3.
- ^ USGS 2011 (PDF).
- ^ a b c Lithium na USGS Mineral Resources, 2009 (PDF).
- ^ Onmeda Nährstoff-Lexikon, stanje 10. juni 2009.
- ^ "Greenbushes Lithium". Arhivirano s originala, 10. 12. 2014. Pristupljeno 26. 11. 2014.
- ^ Meridian International Research: The trouble with Lithium 2. (PDF) Martainville, maj 2008.
- ^ ORF.at: Lithiumabbau in der Zielgeraden, 22. septembar 2014. (de)
- ^ U.S. Geological Survey, 2012, commodity summaries 2011: U.S. Geological Survey
- ^ Dodaci; Po definicijama USGS, bazne rezerve obuhvataju one dijelove resursa koji imaju dovoljan potencijal da postanu ekonomski dostupne u okviru planiranih nivoa a izvan onih koji pretpostavljaju dokazane tehnologije i trenutne ekonomije. Bazna rezerva uključuje one resurse koji su trenutno ekonomični (rezerve), granično ekonomični (granične rezerve) i neke od onih koji su trenutno neekonomični (subekonomski resursi).
- ^ Die weiße Hoffnung. u: FAZ.27. januar 2011, str. 19.
- ^ Wo das ganze Lithium geblieben ist. na stranici: wissenschaft.de
- ^ Über braune Zwerge.
- ^ Garik Israelian, Elisa Delgado Mena, Nuno C. Santos, Sergio G. Sousa, Michel Mayor, Stephane Udry, Carolina Domínguez Cerdena, Rafael Rebolo, Sofia Randich (2009). "Enhanced lithium depletion in Sun-like stars with orbiting planets". Nature (462): 189–191. doi:10.1038/nature08483.CS1 održavanje: više imena: authors list (link)
- ^ O litijskim baterijama Arhivirano 24. 1. 2009. na Wayback Machine na stranici TU Graz (PDF).
- ^ J. Cade (1949). "Lithium salts in the treatment of psychotic excitement". Med. J. Australia. 36: 349–352. PMID 18142718.
- ^ M. Schou (2001). Lithiumbehandlung der manisch-depressiven Krankheit. Thieme. ISBN 3-13-593304-0.
Vanjski linkovi[uredi | uredi izvor]
| Commons ima datoteke na temu: Litij |
- Bauer Michael; et al. (2006). Lithium in Neuropsychiatry (1 izd.). Informa Healthcare. ISBN 9781841845159. Eksplicitna upotreba et al. u:
|author=(pomoć) - Hobbs, L. M.; Thorburn, J. A. (juni 1994): Lithium isotope ratios in six halo stars, The Astrophysical Journal, vol. 428, no. 1, pt. 1, str. L25-L28, doi:10.1086/187384
- Litij na stranici Lenntech










![{\displaystyle \mathrm {Li^{+}+\mathrm {e} ^{-}\ {\xrightarrow[{elektroliza}]{352\,^{\circ }C}}\ Li} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/9c4f392667eae5fea5bd062050b0b8883488c53c)
![{\displaystyle \mathrm {KCl+LiCl\ {\xrightarrow[{elektroliza}]{352\,^{\circ }C}}\ K+Li+Cl_{2}} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/cacbb963ddc07c91454983764f2376c1e594a01e)
